Clear Sky Science · pl
Celowanie w zależność od użycia tyrozyny zależnej od tRNA ujawnia podatność metaboliczną w raku wątrobowokomórkowym
Odmowa komórkom nowotworowym powszechnego budulca
Komórki raka wątroby, jak wszystkie szybko dzielące się komórki, potrzebują stałej dostawy aminokwasów — małych cegiełek białek. Badanie to ujawnia, że rak wątrobowokomórkowy, najczęstsza postać raka wątroby, ma niespodziewaną słabość: silnie polega na aminokwasie tyrozynie zarówno w produkcji energii, jak i w przetrwaniu. Poprzez selektywne ograniczenie sposobu, w jaki komórki nowotworowe wykorzystują tyrozynę, badacze byli w stanie spowolnić wzrost guza, uszkodzić „elektrownie” komórek nowotworowych i wywołać formę śmierci komórkowej, którą można by wykorzystać w nowych terapiach.
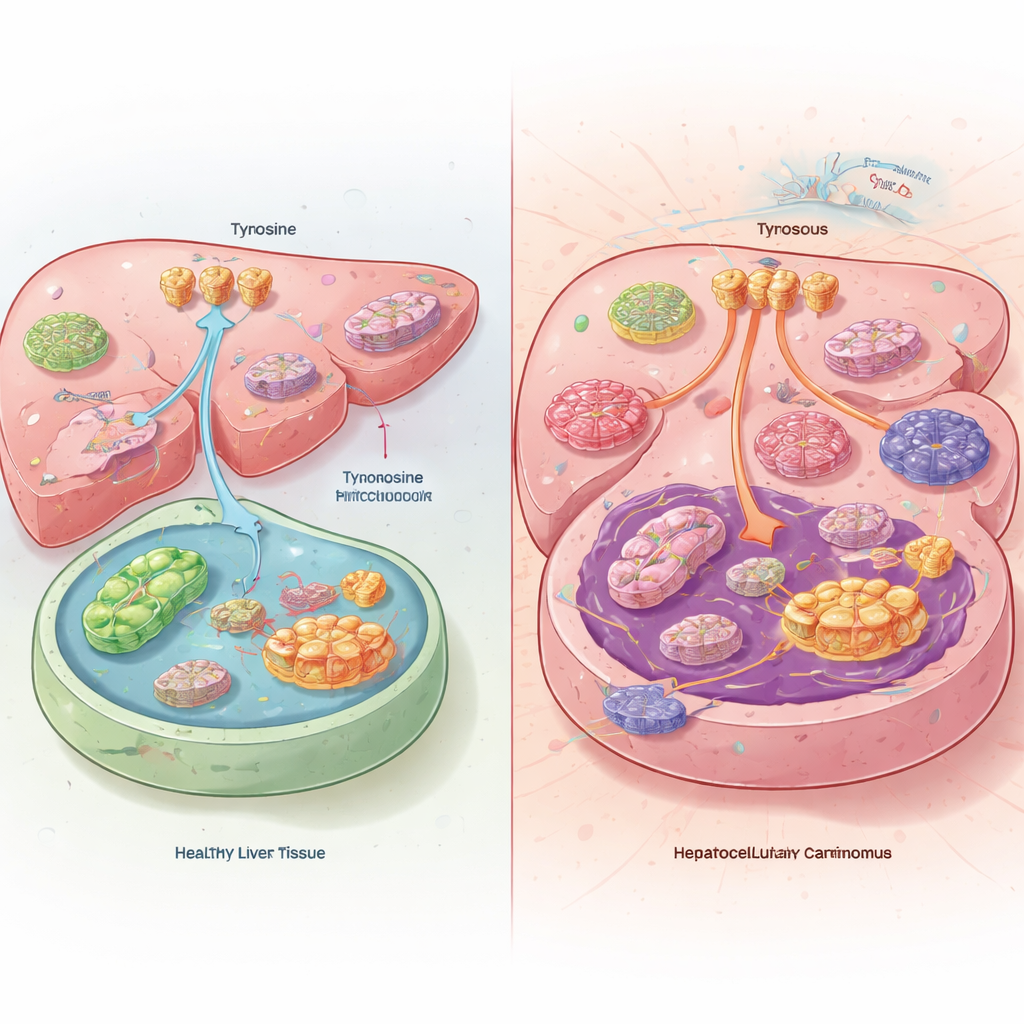
Ukryta nierównowaga w guzach wątroby
Gdy zespół porównał guzy wątroby z prawidłową tkanką wątrobową od pacjentów i myszy, odkryli coś zaskakującego. W komórkach nowotworowych poziomy tyrozyny były faktycznie niskie, mimo że guzy pobierały z krwi więcej tyrozyny i rozkładały jej mniej. Zamiast spalać tyrozynę jako paliwo, guzy wątroby przekierowywały ją do produkcji białek. Nowotwory osiągały to przez zwiększenie aktywności transporterów tyrozyny na powierzchni komórki i obniżenie działania enzymów, które normalnie rozkładają tyrozynę w wątrobie. Myszy karmione dietą pozbawioną tyrozyny rozwijały mniejsze guzy i żyły dłużej, podczas gdy dodatkowa tyrozyna w diecie powodowała szybszy wzrost nowotworów.
Jak nowotwór przebudowuje produkcję białek
Badacze powiązali to „głodowanie” w kierunku tyrozyny z silnym onkogennym genem MYC. W guzach wątroby MYC włącza białko zwane YARS1, które przyłącza tyrozynę do specyficznego tRNA (tRNA-TyrGUA). To naładowane tRNA jest tym, czego rybosomy potrzebują do budowy białek bogatych w tyrozynę. Badanie wykazało, że raki wątrobowe zwiększają zarówno poziom YARS1, jak i odpowiadającego mu tRNA, zapewniając uprzywilejowany dopływ tyrozyny do syntezy białek. Zakłócenie tej „linii zaopatrzenia” — poprzez obniżenie poziomów tyrozyny, wyciszenie YARS1 lub tRNA-TyrGUA albo zablokowanie ładowania tyrozyny — znacząco osłabiało komórki raka wątrobowokomórkowego in vitro i in vivo, ujawniając podatność metaboliczną ściśle związaną z ich wysokimi potrzebami na produkcję białek.
Uszkodzenie „elektrowni” i równowagi lipidowej
Poprzez połączenie pomiarów na poziomie całego genomu RNA, produkcji białek i metabolitów, zespół zidentyfikował dwa szczególnie wrażliwe cele ograniczenia tyrozyny. Pierwszy, NDUFB8, jest składnikiem kompleksu I mitochondrialnego, kluczowej części maszynerii generującej energię w komórce. Drugi, SCD1, uczestniczy w przekształcaniu tłuszczów nasyconych w jednonienasycone, które bezpieczniej magazynuje się w błonach komórkowych i kropelkach lipidowych. Gdy tyrozyna do translacji była ograniczona, produkcja NDUFB8 i SCD1 spadła, podczas gdy ich poziomy RNA pozostały w dużej mierze niezmienione — to wyraźny dowód, że uderzono w translację, a nie w transkrypcję. Doprowadziło to do źle złożonego kompleksu I, obniżonego oddychania komórkowego, nadmiaru reaktywnych form tlenu i przesunięcia profilu tłuszczów od jednonienasyconych ku bardziej kruchej formie wielonienasyconej, łatwo ulegającej utlenianiu.
Wypychanie komórek nowotworowych w stronę żelazozależnej śmierci
Połączone uszkodzenie mitochondriów i niestabilne lipidy skierowały komórki raka wątrobowokomórkowego w stronę ferroptozy, żelazozależnej formy śmierci komórkowej napędzanej peroksydacją lipidów. Guzy próbowały się bronić przez zwiększenie naturalnych blokujących ferroptozę mechanizmów, takich jak GPX4 i powiązane cząsteczki, ale duży ekran edycji genów CRISPR pokazał, że wyłączenie tych zabezpieczeń czyni ograniczenie tyrozyny jeszcze bardziej śmiertelnym. W modelach komórkowych i mysich łączenie strategii ograniczających tyrozynę z lekami hamującymi GPX4 lub BCL2 — albo z istniejącymi lekami przeciw rakowi wątroby, takimi jak sorafenib i wenetoklaks — przyniosło silniejszą kontrolę guza, mniejsze obciążenie nowotworowe i wydłużone przeżycie.
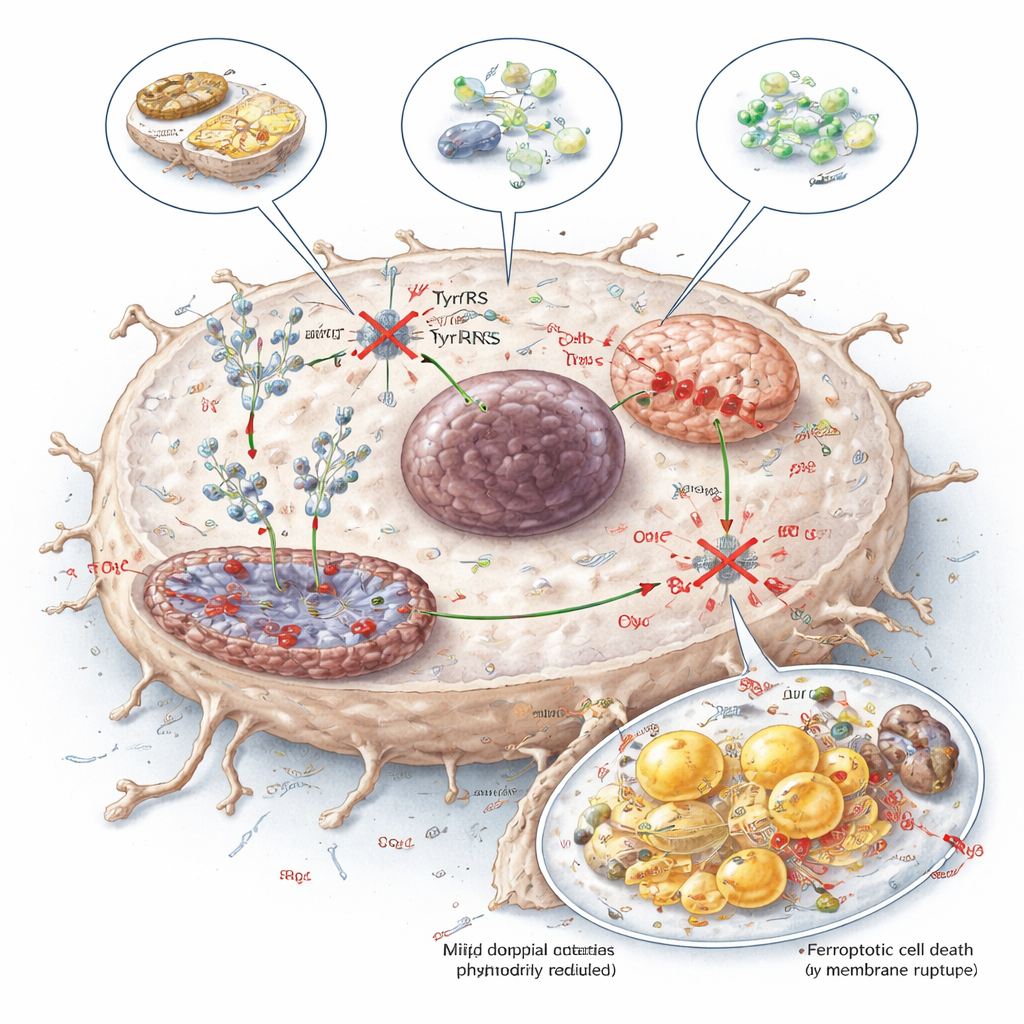
Przekształcanie słabości metabolicznej w terapię
Aby zbadać praktyczne sposoby wykorzystania tej słabości, badacze przetestowali trzy podejścia: dietę ograniczającą tyrozynę, enzym (TAL) enzymatycznie degradujący tyrozynę oraz małą cząsteczkę zwaną tyrozinolem, która konkuruje z tyrozyną o wiązanie z YARS1. Wszystkie trzy zmniejszały dostępność tyrozyny do syntezy białek, obniżały poziomy NDUFB8 i SCD1, uszkadzały funkcję mitochondrialną i zwiększały ferroptozę w guzach wątroby, przy wykazywaniu kontrolowalnych efektów w normalnych tkankach u myszy. Dla laika przesłanie jest takie, że raki wątroby wydają się być uzależnione od tyrozyny nie tylko jako składnika odżywczego, ale jako precyzyjnego paliwa dla swojej maszynerii do wytwarzania białek. Celowanie w to uzależnienie — poprzez dietę, enzymy lub leki — oferuje obiecującą nową drogę osłabienia guzów i zwiększenia skuteczności istniejących terapii.
Cytowanie: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Słowa kluczowe: rak wątroby, metabolizm aminokwasów, tyrozyna, mitochondria, ferroptoza