Clear Sky Science · pl
Systematyczna identyfikacja interakcji między strukturami RNA wariant-specyficznymi a małymi cząsteczkami na przykładzie G-kwadrupleksów RNA
Dlaczego drobne zmiany w RNA mają znaczenie dla przyszłych leków
Większość z nas dziedziczy drobne różnice w DNA, które czynią nas unikalnymi. Te niewielkie zmiany mogą subtelnie przekształcać fałdy cząsteczek RNA w komórkach. Nowe badanie przedstawia metodę, która pokazuje, jak takie genetyczne poprawki zmieniają przyczepność eksperymentalnych leków celujących w RNA. Ma to znaczenie, ponieważ ten sam lek może zachowywać się bardzo różnie u różnych osób, zwłaszcza w przypadku nowotworów lub chorób genetycznych.
Nowy sposób na zobaczenie, gdzie leki dotykają RNA
Wielu twórców leków zwraca obecnie uwagę na RNA, a nie tylko na białka, jako cele terapeutyczne. Małe cząsteczki mogą przyczepiać się do specyficznych kształtów RNA i wpływać na odczyt genów, ale do tej pory większość metod działała tylko na pojedynczej „referencyjnej” sekwencji RNA. W dużej mierze pomijały one niezliczone jedno-literowe zmiany występujące u rzeczywistych pacjentów. Autorzy stworzyli wysokoprzepustowe podejście nazwane BIVID-MaP, które jednocześnie testuje tysiące wariantów RNA i precyzyjnie określa, gdzie mała cząsteczka wiąże się z każdym z nich, z rozdzielczością pojedynczego nukleotydu. 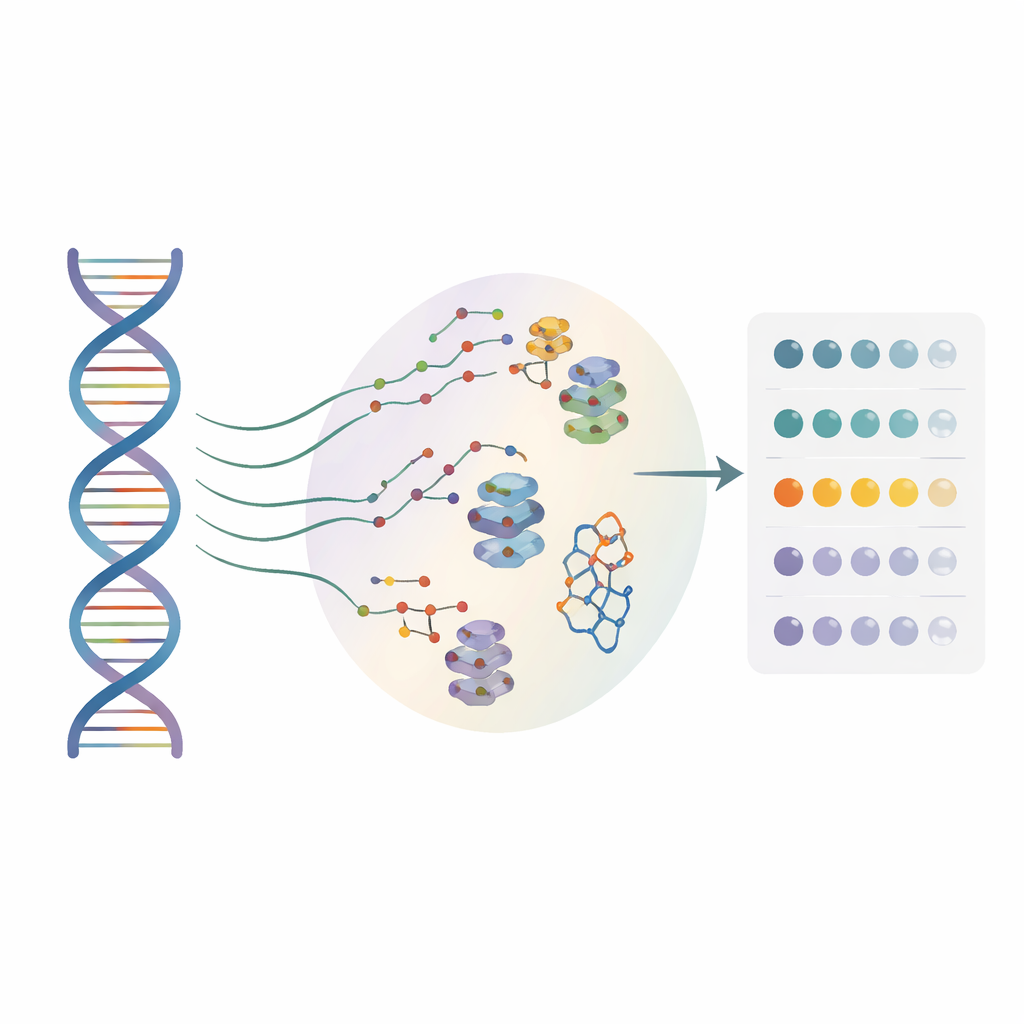
Przekształcanie chemicznych znaków w czytelny sygnał
BIVID-MaP działa w trzech głównych krokach. Najpierw zespół dołącza reaktywny znacznik do małej cząsteczki wiążącej RNA. Gdy znakowana cząsteczka zagnieżdża się w preferowanej strukturze RNA, takiej jak zwarte G-kwadrupleksy tworzone przez guaninowo-bogate sekwencje, znacznik tworzy trwały wiązanie chemiczne z pobliską zasadą RNA. Po drugie, specjalny enzym kopiuje zmodyfikowane RNA na DNA. Napotykając taki chemiczny ślad, enzym ma tendencję do „ominięcia” pojedynczej zasady, tworząc niewielkie delecje w kopii. Po trzecie, głębokie sekwencjonowanie odczytuje te sygnatury delecji w milionach cząsteczek. Ponieważ niemal cały otaczający fragment sekwencji jest zachowany, delecje można dokładnie przypisać do konkretnych wariantów genetycznych w mieszanej puli.
Weryfikacja metody na kontrolowanym modelu
Aby potwierdzić, że BIVID-MaP rzeczywiście wykrywa wiązanie specyficzne dla wariantu, badacze zbadali fragment RNA z genu CD44, który normalnie tworzy G-kwadrupleks. Pojedyncza zamiana G na A zaburza tę strukturę. W mieszaninie zawierającej obie wersje jedynie forma nienaruszona wykazywała silne sygnały delecji w pobliżu złożonego regionu po ekspozycji na sondę opartą na berberynie, a niezależne testy potwierdziły tam silniejsze wiązanie. Mutant, który nie może uformować tego samego kształtu, generował znacznie mniej delecji i słabsze wiązanie. Inne powszechne techniki mapowania albo nie wychwyciły tej różnicy, albo dały mylące tło, co podkreśla lepszą czułość i specyficzność nowego podejścia.
Przeszukiwanie mutacji związanych z rakiem w wielu genach
Zespół następnie zwiększył skalę badań. Zbudowali bibliotekę RNA regionów 5′ nieprzetłumaczonych (5′ UTR) z 283 genów związanych z rakiem, z których każdy był sparowany z rzeczywistymi somatycznymi mutacjami zgłoszonymi w guzach. Używając sondy rozpoznającej struktury podobne do G-kwadrupleksów, BIVID-MaP ujawnił liczne mutacje, które albo wzmacniały, albo osłabiały wiązanie małych cząsteczek. W genach takich jak DAXX i ING2 pojedyncze zamiany w guaninowo-bogatych odcinkach znacząco zmieniały wiązanie, zgodnie z niezależnymi testami biofizycznymi formowania G-kwadrupleksów i bezpośrednimi pomiarami wiązania masową spektrometrią. W niektórych przypadkach mutacje poza oczywistymi odcinkami G nadal przesuwały wiązanie przez subtelne zmiany w skłonności pobliskich zasad do parowania, przekształcając „ensemble” struktur bez radykalnej zmiany przewidywanego ogólnego fałdu. 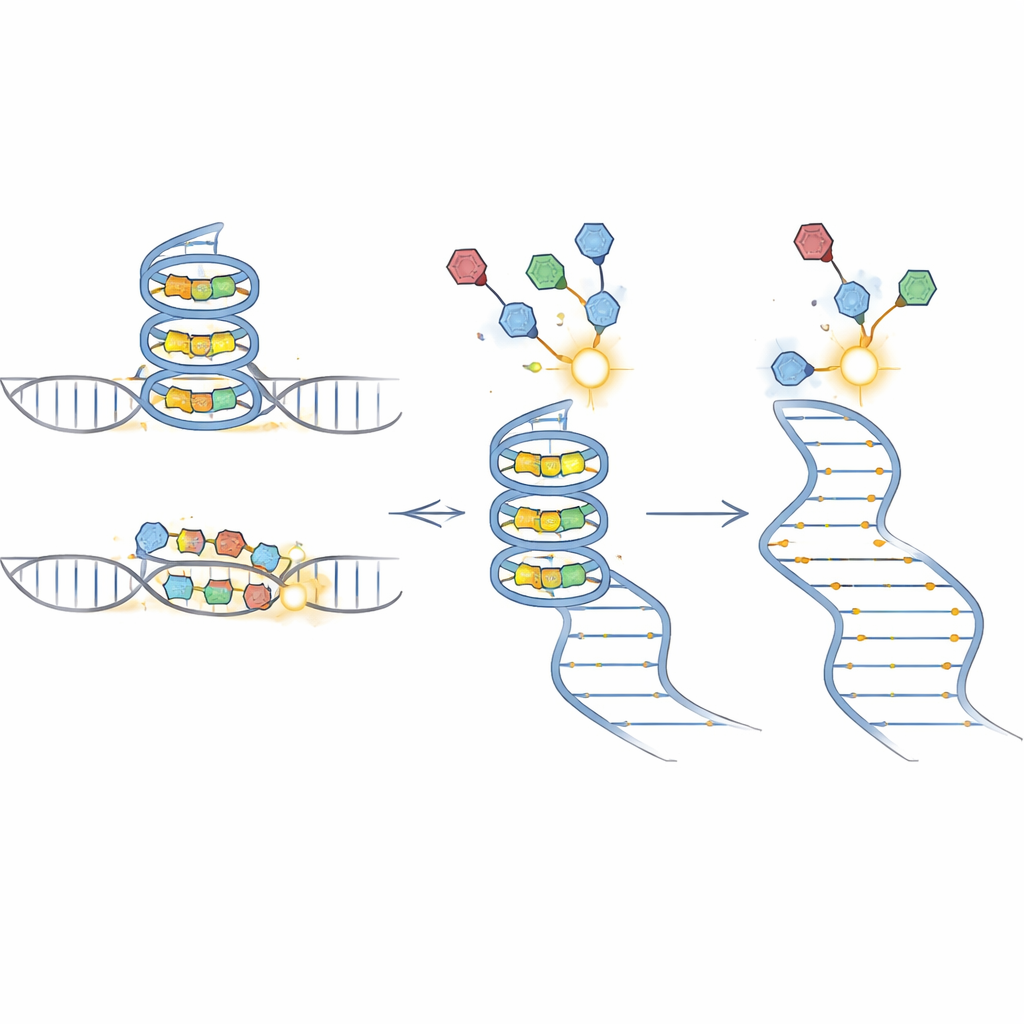
Co przepowiednie komputerowe pomijają
Co ważne, istniejące narzędzia do przewidywania struktur RNA i G-kwadrupleksów często nie przewidywały zmian ujawnionych przez BIVID-MaP. Niektóre warianty, które niemal nie zmieniały wyników obliczeń, powodowały duże rzeczywiste różnice we wiązaniu. Inne wydawały się wpływać na wiązanie w całej rodzinie związków celujących w G-kwadrupleksy, podczas gdy pewne mutacje miały efekty specyficzne dla danego leku. To pokazuje, że pojedyncze nukleotydowe warianty mogą dostrajać krajobraz fałdowania RNA i kontaktów z lekami w sposób, który trudno wywnioskować jedynie ze sekwencji.
Znaczenie dla spersonalizowanych leków celujących w RNA
Autorzy wnioskują, że BIVID-MaP oferuje potężną drogę mapowania, w jaki sposób indywidualne różnice genetyczne przekształcają struktury RNA i ich interakcje z małymi cząsteczkami. Przekształcając lokalne modyfikacje chemiczne w precyzyjne sygnatury delecji, metoda może równolegle przeszukać tysiące wariantów i wskazać te, które istotnie zmieniają wiązanie leku. W dłuższej perspektywie takie mapy mogłyby kierować projektowaniem leków celujących w RNA, które będą skuteczniejsze i bezpieczniejsze dla zróżnicowanych pacjentów, oraz ujawniać dotąd ukryte struktury RNA, które mogłyby służyć jako nowe cele terapeutyczne.
Cytowanie: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Słowa kluczowe: leki celujące w RNA, G-kwadrupleks, warianty genetyczne, wiążenie małych cząsteczek, mutacje nowotworowe