Clear Sky Science · pl
Optymalizacja organizacji przestrzennej pierścieni FtsZ dla dużoskalowego zwężania w komórkach syntetycznych
Dlaczego małe pierścienie mają znaczenie przy budowie komórek syntetycznych
Wyobraź sobie skonstruowanie prostej, sztucznej komórki, która potrafi samodzielnie rosnąć i dzielić się na dwie. Aby to osiągnąć, naukowcy muszą nauczyć się kontrolowanie zasysania miękkiej, przypominającej mydlaną błony, używając zaledwie kilku elementów biologicznych. Badanie to pokazuje, jak białko bakteryjne można wspomóc w tworzeniu dużych, stabilnych pierścieni na olbrzymich pęcherzykach tłuszczu, pozwalając tym modelowym „komórkom” zwężać się niemal do stadium podziału. Ujawnia, jaka architektura białkowa jest potrzebna, by wygiąć i przekształcić błonę w skali całej komórki.
Zap借czenie narzędzi podziałowych natury
Wiele bakterii dzieli się przy udziale białka o nazwie FtsZ, dalekiego krewnego tubuliny, która buduje wewnętrzny szkielet naszych własnych komórek. FtsZ składa się w filamenty, które gromadzą się w pierścień w połowie komórki, wyznaczając miejsce jej podziału. W żywych bakteriach tłum białek pomocniczych przytwierdza ten pierścień do wewnętrznej błony, ustawia go na środku komórki i łączy z enzymami przebudowującymi ścianę komórkową. Poprzednie próby laboratoryjne odtworzenia tej machiny w dużych, wielkości komórki pęcherzykach zdołały wytworzyć pierścienie i wywołać niewielkie wgniecenia błony, ale nie płynne, postępujące zwężanie, które przeformowałoby olbrzymi pęcherzyk w dwie prawie oddzielne połówki.
Minimalistyczne podejście do dzielącej się powłoki
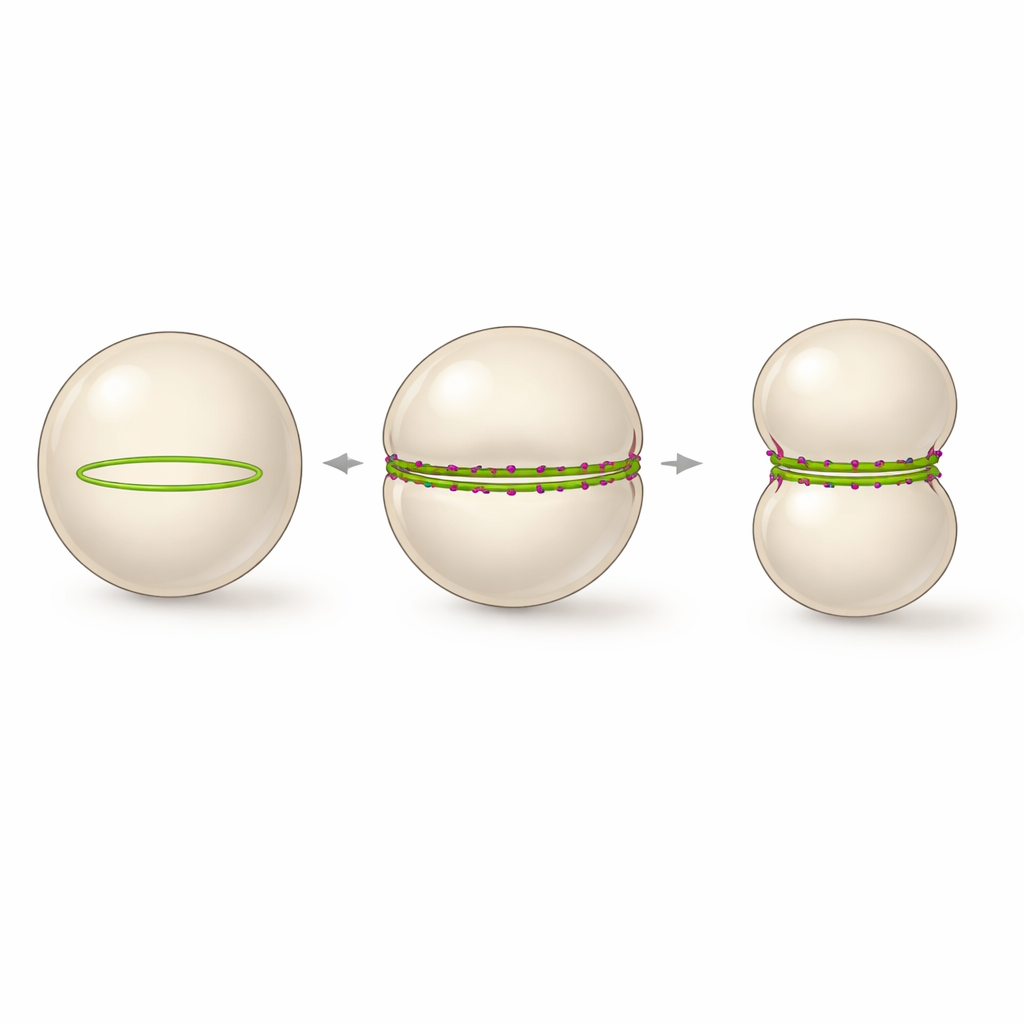
Autorzy zapytali, czy można zredukować ten system do zaledwie dwóch składników: wariantu FtsZ, który może bezpośrednio przylegać do błon, oraz krótkiego dodatnio naładowanego ogonka z innego białka podziałowego, FtsN. Zamknęli te komponenty wewnątrz olbrzymich, jednowarstwowych pęcherzyków — pustych kulek lipidowych przypominających uproszczone komórki — i dostarczyli im cząsteczkę energii GTP oraz wolno działający jej substytut, by stroić dynamikę białek. Bez ogonka FtsN FtsZ tworzył wiele małych pierścieni i plam, które powodowały jedynie lokalne wgniecenia. Przy nadmiarze fragmentu FtsN (nazwanego cytoFtsN) te małe pierścienie przeorganizowały się w pojedynczy, duży pierścień owijający pęcherzyk w pobliżu jego równika i zdolny do zwężania przez kilka godzin.
Z poplątanej sieci do pojedynczego pierścienia kurczliwego
Aby zrozumieć, jak ten mały peptyd zmienia zachowanie w tak dramatyczny sposób, zespół obserwował filamenty FtsZ na płaskich, podpartych błonach za pomocą mikroskopii o wysokiej rozdzielczości. Zwykle FtsZ na takich powierzchniach tworzy wirowe, zakrzywione wiry. Dodawanie rosnących ilości cytoFtsN stopniowo usuwało te spirale i zastępowało je prostszymi, bardziej uporządkowanymi pęczkami. Ilościowa analiza obrazów potwierdziła, że sieć stawała się bardziej spójna i uporządkowana wraz ze wzrostem stężenia peptydu. Eksperymenty z odzyskiwaniem fluorescencji wykazały, że podjednostki w tych pęczkach wymieniały się wolniej, co wskazuje, że peptyd stabilizuje filamenty i redukuje ich dynamiczne mieszanie.

Elektrostatyczne „rzepy”, które blokują filamenty razem
Pomiary biochemiczne wykazały, że cytoFtsN i FtsZ wchodzą w interakcję przede wszystkim poprzez przeciwne ładunki elektryczne: FtsZ jest ogólnie ujemny, podczas gdy peptyd niesie skupiska ładunków dodatnich. Przy niższym stężeniu soli peptyd wiązał się silniej, sprzyjał tworzeniu grubszych pęczków FtsZ w roztworze i spowalniał rozpad filamentów, tłumiąc aktywność GTP-owej hydrolizy białka. Gdy badacze zmienili kluczowe dodatnio naładowane reszty w peptydzie lub zwiększyli stężenie soli, by ekranować przyciąganie elektrostatyczne, efekty pęczkowania i przeorganizowania znikały. Wskazuje to na prosty mechanizm fizyczny, w którym dodatnio naładowany peptyd działa jak molekularne „rzepy”, zmniejszając odpychanie między filamentami FtsZ, dzięki czemu mogą one ustawiać się obok siebie w sztywne pęczki.
Jak pojedynczy pierścień przekształca olbrzymi pęcherzyk
Wewnątrz pęcherzyków takie stabilizowane przez peptyd pęczkowanie ma uderzające konsekwencje. Zamiast wielu małych zakrzywionych pierścieni, wyprostowane pęczki FtsZ są zmuszone podążać za dużą krzywizną pęcherzyka, assemblując się w jeden ciągły pierścień obejmujący cały obwód. Obrazowanie w czasie pokazało, że gdy taki w pełni zamknięty pierścień powstawał, pęcherzyk wiarygodnie deformował się ze sfery w kształt hantli, z wąską talerzem tam, gdzie siedział pierścień. Proces można było śledzić w czasie rzeczywistym, gdy średnica pęcherzyka malała, a zwężenie pogłębiało się, niemal rozdzielając przegrodę na dwie części, chociaż ostateczne rozerwanie nie zostało osiągnięte. Autorzy proponują, że stabilny pierścień FtsZ rozciągający się wzdłuż równika, z wolniejszym, ale nadal aktywnym obrotem podjednostek, jest minimalną architekturą potrzebną do napędzenia dużoskalowego zwężania błony w komórce syntetycznej.
Co to znaczy dla przyszłego życia syntetycznego
Pokazując, że wariant FtsZ przytwierdzony do błony oraz krótki kationowy peptyd mogą przekształcić olbrzymie liposomalne pęcherzyki niemal do stadium podziału, praca ta definiuje jasną zasadę projektową dla sztucznych komórek: pojedynczy, spójny pierścień białkowy dopasowany do rozmiaru komórki i mechanicznie stabilny w czasie wystarcza, by zacisnąć miękką granicę w skali komórkowej. Do całkowitego przecięcia błony mogą być potrzebne jeszcze bardziej złożone czynniki, ale badanie pokazuje, że kontrolowane zwężanie na dużą skalę nie wymaga całego zestawu bakteryjnych białek podziałowych. Zamiast tego staranne dostrojenie organizacji filamentów i ich dynamiki może przekształcić prosty szkielet białkowy w efektywny pierścień kurczliwy, przybliżając prawdziwie samodzielnie dzielące się komórki syntetyczne o kolejny krok.
Cytowanie: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Słowa kluczowe: synteza podziału komórkowego, pierścień FtsZ, zwężanie błony, minimalny divizom, samorganizacja cytoszkieletu