Clear Sky Science · pl
Proteomika subkomórkowa ujawnia plan integracji endosymbionta w trypanosomatydzie Angomonas deanei
Ukryci partnerzy we wnętrzu jednokomórkowego życia
Wiele organizmów jednokomórkowych nie żyje naprawdę samotnie. Niektóre z nich goszczą bakterie, które żyją wewnątrz nich jako stałe lokatorki, wymieniając pokarm i usługi w relacjach przypominających pochodzenie naszych własnych mitochondriów. Badanie to analizuje taką współpracę u Angomonas deanei, mikroskopijnego pasożyta owadów, aby ukazać, jak kiedyś wolno żyjąca bakteria stała się głęboko wpleciona w wewnętrzne mechanizmy komórki gospodarza.
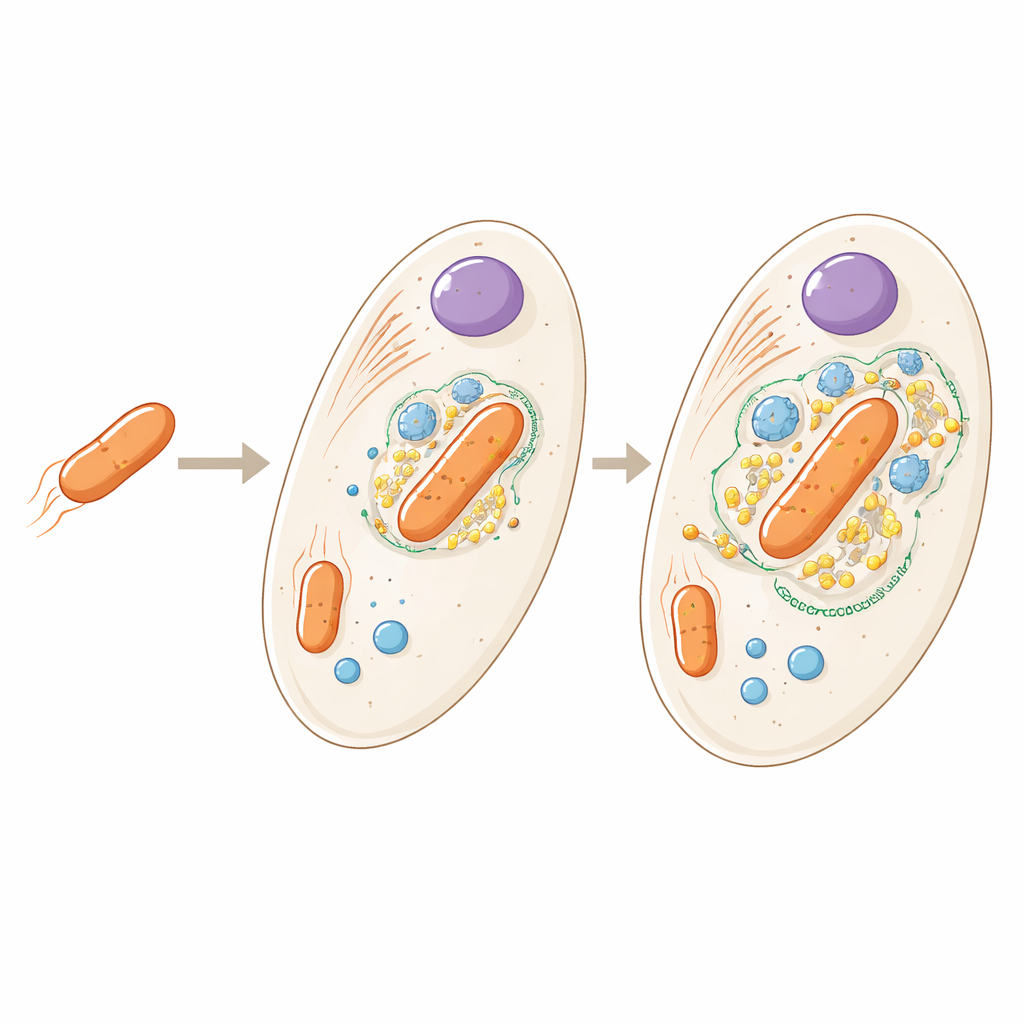
Od gościa do wbudowanej części
Bakteria żyjąca wewnątrz Angomonas deanei jest odległym krewnym wolno żyjących mikroorganizmów glebowych, lecz tutaj występuje jako pojedyncza kopia na komórkę gospodarza i nie potrafi już przetrwać samodzielnie. Wcześniejsze prace wykazały, że gospodarz produkuje specjalne białka, które trafiają do bakterii i nawet pomagają kontrolować jej podział. Nowe badanie stawia szersze pytanie: jeśli przyjrzymy się całej komórce, gdzie dokładnie znajdują się wszystkie białka gospodarza i bakterii i co to mówi o stopniu integracji obu partnerów?
Mapowanie wewnętrznego miasta komórki
Aby to ustalić, badacze delikatnie rozbili dużą liczbę komórek, tak aby struktury wewnętrzne pozostały w większości nienaruszone. Następnie rozdzielili te fragmenty przez wirówkowanie z różnymi prędkościami i zidentyfikowali tysiące białek w każdej frakcji przy użyciu wysokorozdzielczej spektrometrii mas. Porównując, jak białka grupowały się w różnych frakcjach i weryfikując to znacznikami i mikroskopią fluorescencyjną, stworzyli szczegółowy „spis adresów” komórki, przypisując niemal 3 000 białek do 21 odrębnych regionów, takich jak jądro, mitochondrium, wyspecjalizowane magazyny i sam endosymbiont bakteryjny.
Narzędzia gospodarza skierowane do zamieszkującej bakterii
W ramach tego atlasu zespół odkrył zestaw białek wytwarzanych przez gospodarza, które konsekwentnie towarzyszyły endosymbiontowi, poszerzając znany katalog tzw. białek kierowanych do endosymbionta. Jeden nowo potwierdzony przykład, nazwany ETP10, pokrywa bakterię podobnie jak wcześniej opisane białko, co sugeruje rusztowanie czynników gospodarza otulające partnerski mikroorganizm. Inna niewielka grupa białek wykazała nietypowe zachowanie fizyczne wspólne z białkiem podobnym do dynaminy, już znanym z uszczypywania bakterii podczas podziału. Razem te odkrycia sugerują istnienie wyspecjalizowanej, zbudowanej przez gospodarza maszyny dedykowanej pozycjonowaniu, kształtowaniu i rozmnażaniu endosymbionta wewnątrz komórki.
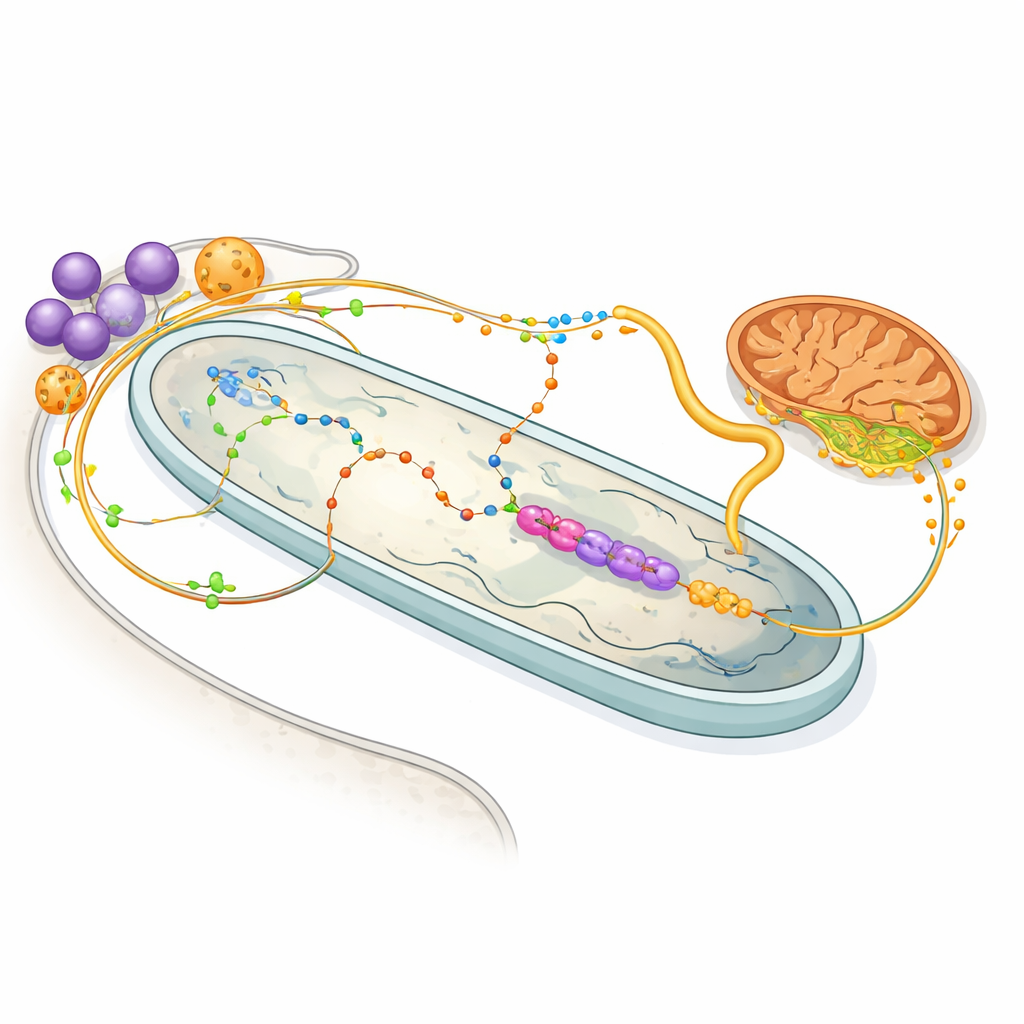
Współdzielenie energii i chemiczne szlaki handlowe
Mapa białek rzuca również światło na tętniący wymianą cząsteczek handel między gospodarzem a bakterią. Enzymy w glikosomach gospodarza — organellach zajmujących się metabolizmem cukrów i aminokwasów — wydają się być dostrojone do zasilania bakterii aminokwasem prolina i związkiem 2‑okoglutaranem, obydwoma wartościowymi źródłami energii. Wewnątrz bakterii odchudzone zestawy enzymów wykorzystują 2‑okoglutaran do generowania NADH, który napędza minimalny łańcuch oddechowy, a następnie przekazują bursztynian z powrotem do mitochondrium gospodarza. Inne szlaki pokazują, że bakteria wykonuje większość kroków syntezy hemu, istotnego barwnika potrzebnego gospodarzowi, jednocześnie dostarczając ważnych bloków budulcowych dla nukleotydów. W efekcie każdy z partnerów oddelegował określone zadania metaboliczne drugiemu, tworząc wspólny, współzależny system.
Nowe linie komunikacji wewnątrz komórki
Ponad metabolizmem, badanie ujawnia fizyczne i prawdopodobnie sygnałowe powiązania między endosymbiontem a innymi organellami. Odmienne grupy białek gospodarza tworzą to, co autorzy nazywają klastrem „miejsc kontaktu”, wzbogaconym w składniki otoczki jądrowej i siateczki śródplazmatycznej, które fizycznie współosadzają się z bakterią. Dwa typy organelli magazynujących — glikosomy i acidokalcysomy — występują w dwóch populacjach: niektóre pozostają wolne w cytoplazmie, podczas gdy inne konsekwentnie podróżują z bakterią. Mikroskopia potwierdza, że podzbiory tych organelli przylegają ściśle do endosymbionta. Acidokalcysomy są znane jako rezerwuary wapnia i fosforanów, więc ich bliskie przyleganie sugeruje dwukierunkową ścieżkę sygnałową i ruch jonów łączącą bakterię, te magazyny i pobliską siateczkę śródplazmatyczną.
Plan życia zlanego z życiem
Sumarycznie praca ta dostarcza bogatego, komórkowego planu pokazującego, jak bakteria może stać się funkcjonalnie zrośnięta ze swoim gospodarzem, nie przekształcając się jeszcze w pełnoprawną organellę jak mitochondrium. Angomonas deanei polega na swoim endosymbioncie w kwestii kluczowych składników odżywczych, podczas gdy bakteria z kolei zależy od białek gospodarza i bogatych w energię cząsteczek oraz jest przywiązana do organelli gospodarza dla komunikacji i kontroli. Dla osób niebędących specjalistami wniosek jest taki, że ewolucja może stopniowo utrwalać współpracę między bardzo różnymi formami życia, krok po kroku, aż ich rozdzielenie stanie się niemożliwe. System ten oferuje żywe migawki tego procesu w działaniu, pomagając naukowcom lepiej zrozumieć, jak z prostszych początków wyłoniły się złożone komórki, takie jak nasze własne.
Cytowanie: Hammond, M., Chmelová, Ľ., van Geelen-Kuenzel, N.A. et al. Subcellular proteomics reveals a blueprint for endosymbiont integration in trypanosomatid Angomonas deanei. Nat Commun 17, 2241 (2026). https://doi.org/10.1038/s41467-026-70084-0
Słowa kluczowe: endosymbioza, metabolizm komórkowy, ewolucja organelli, biologia protistów, interakcje gospodarza z mikrobiem