Clear Sky Science · pl
Dynamiczny rozkład tandemowych amplifikacji genowych w heteroopornych populacjach Escherichia coli ujawniony dzięki ultra-głębokiemu sekwencjonowaniu długich odczytów
Ukryte enklawy przetrwania
Kiedy lekarze leczą infekcje bakteryjne za pomocą antybiotyków, zakładają, że cała populacja drobnoustrojów zareaguje jednakowo. Czasem jednak niewielka frakcja populacji cicho opiera się leczeniu, przeżywa i przygotowuje grunt pod niepowodzenie terapii lub nawrót choroby. Badanie to ujawnia, jak pojawiają się tacy rzadcy ocalańcy i jak zmieniają się w czasie w Escherichia coli, oraz prezentuje potężną metodę pozwalającą śledzić te zmiany genetyczne komórka po komórce.
Małe powtórzenia genetyczne, wielkie konsekwencje
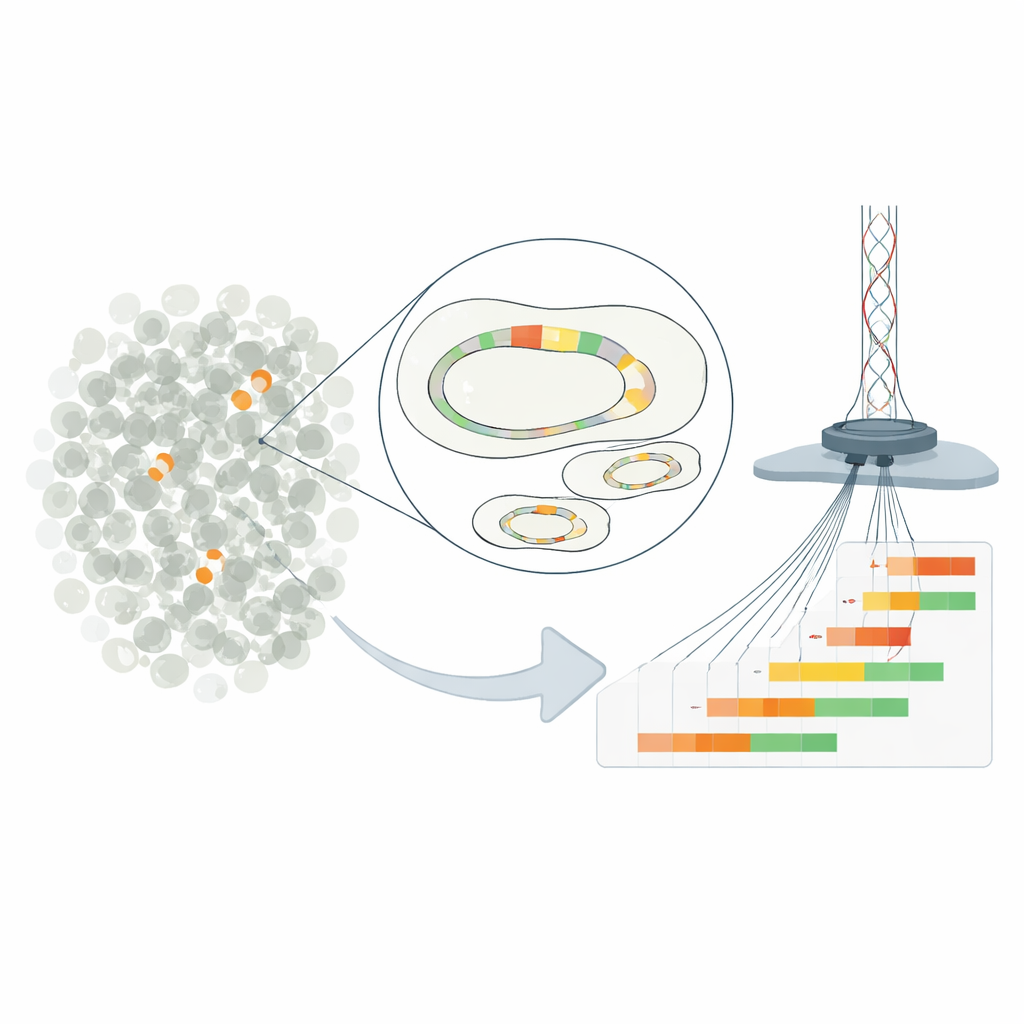
Praca koncentruje się na „heterooporności” — sytuacji, w której większość bakterii próbki wydaje się wrażliwa na lek, lecz niewielka mniejszość potrafi znieść znacznie wyższe dawki. W badanym szczepie E. coli zachowanie to wynika z powielonych kopii genu oporności przenoszonego na plazmidzie — małym kolistym fragmencie DNA niezależnym od chromosomu. Poprzez duplikację krótkiego odcinka DNA zawierającego gen beta-laktamazy bakterie mogą zwiększyć produkcję enzymu rozkładającego antybiotyk piperacylinę z tazobaktamem. Im więcej powtórzeń nosi komórka, tym więcej enzymu wytwarza i tym większe ma szanse przetrwać w obecności leku.
Odczytywanie kolistych DNA w bezprecedensowej rozdzielczości
Tradycyjne metody potrafią jedynie oszacować średnią liczbę kopii genu w całej populacji bakteryjnej, maskując bogactwo różnorodności między pojedynczymi komórkami. Aby temu zaradzić, badacze zmodyfikowali kliniczny plazmid tak, by można go było przeciąć w precyzyjnym miejscu i następnie odizolować od reszty genomu. Wykorzystali ultra-głębokie sekwencjonowanie długich odczytów metodą Nanopore, by czytać pełne cząsteczki plazmidu od końca do końca, dokładnie licząc, ile powtórzonych jednostek oporności zawiera każda z nich. Podejście to osiągnęło czułość rzędu jednej komórki na 100 000, ujawniając plazmidy z zerem aż do ponad tuzina kopii genu współistniejące w tej samej hodowli. Kontrole innymi technikami potwierdziły, że średnio nowa metoda podaje poprawne liczby kopii.
Jak antybiotyki przekształcają populację
Dysponując tym narzędziem, zespół obserwował, co się dzieje, gdy eksponowano kultury E. coli na rosnące dawki piperacyliny z tazobaktamem, a następnie usunięto lek. W miarę wzrostu stężeń antybiotyku ogólny rozkład przesuwał się w kierunku plazmidów niosących więcej kopii genu oporności, jednak komórki z mniejszą liczbą kopii nigdy nie zniknęły całkowicie. Po wycofaniu leku i hodowaniu bakterii przez setki pokoleń populacja jedynie stopniowo dryfowała z powrotem ku niższym liczbom kopii i nigdy w pełni nie wróciła do stanu wyjściowego. Oddzielne testy wzrostu wykazały, że każda dodatkowa kopia genu przynosiła mierzalny wzrost tolerancji na lek, ściśle łącząc obserwowane rozkłady genetyczne z widocznym wzorem heterooporności w standardowych testach laboratoryjnych.

Ochrona od sąsiadów i ukryte koszty
Aby wyjaśnić, dlaczego komórki o niskiej liczbie kopii przetrwały nawet pod silnym leczeniem, autorzy zbudowali model matematyczny łączący wzrost bakterii, rozkład antybiotyku i losowe zdarzenia dodawania lub usuwania kopii genu. Symulacje wykazały, że „pośrednia oporność” odgrywa kluczową rolę: silnie oporne komórki wydzielają tyle beta-laktamazy, że obniżają stężenie leku we wspólnym środowisku, przypadkowo chroniąc mniej opornych sąsiadów. Dopóki dodatkowe kopie genu wiążą się jedynie z niewielkim kosztem wzrostu przy braku leku, ten efekt ochronny pomaga utrzymać szerokie spektrum liczby kopii, spowalniając powrót do całkowicie wrażliwej populacji. Model pokazał też, jak zwykła adaptacja do podłoża — niezwiązane mutacje poprawiające wzrost — może utrwalić konkretne stany liczby kopii, czyniąc niektóre subpopulacje bardziej wydajnymi od innych.
Dlaczego to ma znaczenie dla pacjentów i nie tylko
Dla osób niebędących specjalistami przekaz jest taki: hodowla bakteryjna nie jest jednolitym wrogiem, lecz ciągle zmieniającą się mieszaniną osobników o różnej zdolności przetrwania antybiotyków. Poprzez bezpośrednie liczenie kopii genów na tysiącach pojedynczych cząsteczek DNA badanie to ilościowo łączy tę ukrytą różnorodność z opornością istotną dla leczenia. Takie spostrzeżenia mogą poprawić wykorzystanie sekwencjonowania genomów do przewidywania trudnej do wykrycia heterooporności, pomóc identyfikować szczepy bakterii szczególnie narażone na wywołanie niepowodzenia terapii oraz ukierunkować lepsze testy diagnostyczne. Ponieważ tandemowe amplifikacje genów napędzają też szybką adaptację wirusów, nowotworów i innych organizmów, ta sama strategia może być zastosowana daleko poza E. coli, oferując nowe spojrzenie na to, jak powtarzające się fragmenty DNA pomagają życiu unikać zagrożeń.
Cytowanie: Jonsson, S., Guliaev, A., Berryhill, B.A. et al. The dynamic distribution of genetic tandem amplifications in a heteroresistant Escherichia coli population revealed by ultra-deep long read sequencing. Nat Commun 17, 2113 (2026). https://doi.org/10.1038/s41467-026-70044-8
Słowa kluczowe: heterooporność na antybiotyki, amplifikacja genów, Escherichia coli, sekwencjonowanie długich odczytów, beta-laktamaza