Clear Sky Science · pl
Ruchy pojedynczych cząsteczek ujawniają, że samo związanie ATP napędza translokację substratu przez transporter ABC
Dlaczego małe pompki komórkowe mają znaczenie
Każda komórka w twoim ciele polega na mikroskopijnych maszynach, które przemieszczają cząsteczki przez błony, kształtując wszystko, od pobierania składników odżywczych po obronę immunologiczną. Jedna z głównych klas tych maszyn, zwana transporterami ABC, wykorzystuje chemiczne paliwo komórki — ATP — aby przepychać ładunek pod górę, wbrew naturalnym gradientom. Przez dekady naukowcy spierali się o podstawowe pytanie: czy prosty akt związania ATP napędza etap transportu, czy energia uwalniana jest dopiero podczas rozkładu ATP? W tym badaniu skupiono się na pojedynczym transporterze, cząsteczka po cząsteczce, aby rozstrzygnąć tę debatę.
Obserwowanie jednego transportera naraz
Zamiast mierzyć zbiorcze zachowanie milionów cząsteczek, badacze zbudowali układ pozwalający śledzić indywidualne zdarzenia transportowe w czasie rzeczywistym. Skoncentrowali się na TmrAB, bakteryjnym krewniaku ludzkiego transportera TAP, który ładuje peptydy immunologiczne do prezentacji komórkom zabójczym T. TmrAB osadzony jest w błonie i przenosi krótkie fragmenty białek (peptydy) z jednej strony na drugą, wykorzystując ATP. Aby zobaczyć każdy krok transportu, zespół uwięził pojedynczą cząsteczkę TmrAB w sztucznej pęcherzyku błonowym (liposomie) i umieścił wewnątrz specjalnie zaprojektowane „czujnikowe” białko, które zmienia fluorescencję po złapaniu peptydu. Przy użyciu wysoce czułego mikroskopu mogli następnie obserwować, jako krótkie skoki sygnału świetlnego, dokładne momenty, gdy kolejny peptyd trafiał do wnętrza pęcherzyka.
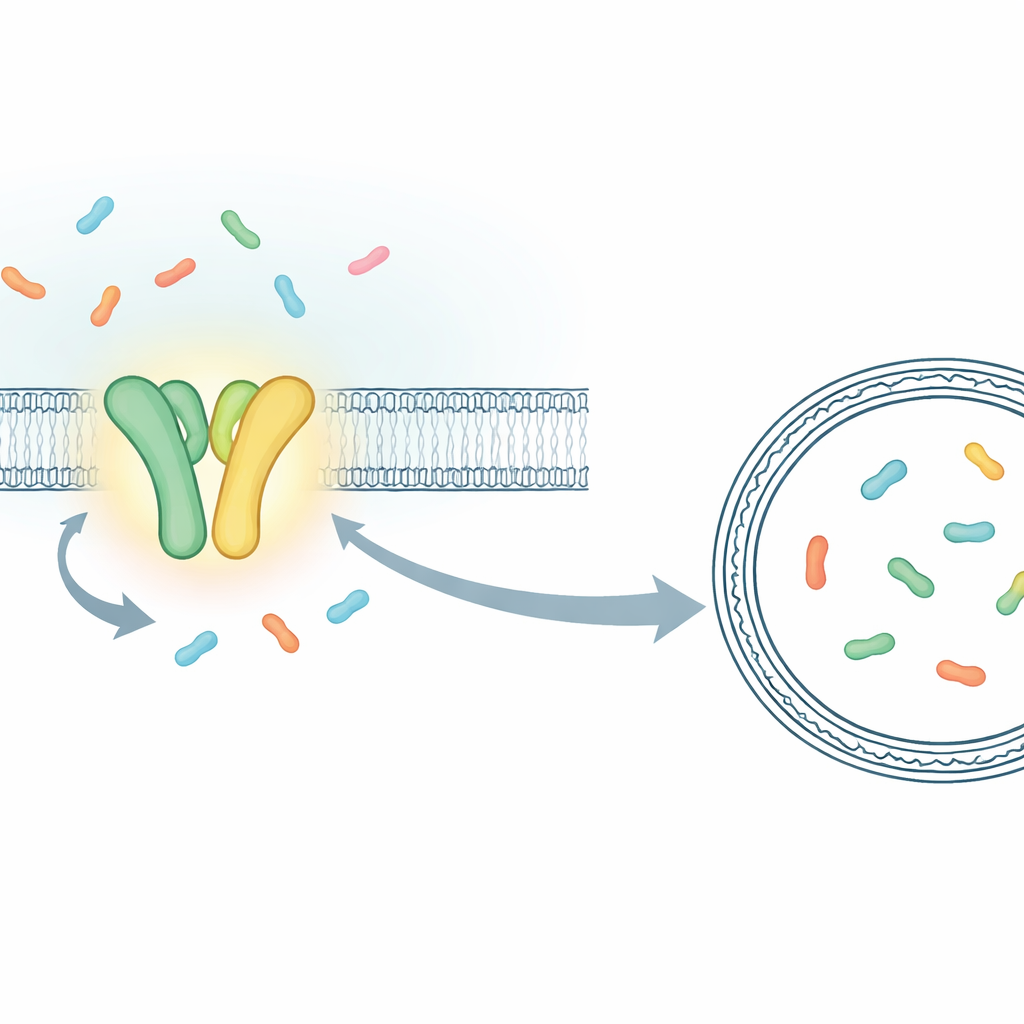
Dowód, że jedno związanie ATP przesuwa jeden peptyd
Dysponując tym układem pojedynczej cząsteczki, badacze porównali normalny TmrAB z zmodyfikowaną, wolniej działającą wersją, której cykle były wydłużone w czasie. Wolny wariant umożliwił rozróżnienie pojedynczych zdarzeń, które w przeciwnym razie zlałyby się w jedną całość. Wykazali, że gdy obecne były zarówno ATP, jak i peptydy, czujnik wewnątrz liposomu przechodził ze stanu „pustego” do stanu „naładowanego” w dyskretnych skokach, z których każdy odpowiadał transportowi jednego peptydu. Analizując tempo zamykania się czujnika wokół peptydów i szacując maleńką objętość każdego liposomu, mogli nawet przeliczyć te zmiany światła na przybliżone stężenia peptydów. Liczby zgadzały się z oczekiwaniami, jeśli w pęcherzykach o średnicy około 100 nanometrów gromadziłby się po jednym, a potem po dwóch peptydach, co potwierdziło, że rzeczywiście zliczali zdarzenia transportowe jedno po drugim.
Samo związanie ATP przełącza molekularny przełącznik
Kluczowa kontrowersja dotyczy jonów magnezu (Mg2+), które zwykle towarzyszą ATP w komórkach i są konieczne do wydajnego rozkładu ATP. Niektóre modele sugerowały, że Mg2+ może być również potrzebny do związania ATP lub do zamknięcia transportera. Aby rozdzielić te role, badacze usunęli Mg2+ przy pomocy środka chelatującego, ale nadal dostarczyli ATP. W tych warunkach zarówno normalny, jak i wolny transporter mogły wykonać dokładnie jeden krok transportu peptydu na cząsteczkę, a potem się zatrzymywały. Takie zachowanie wskazuje, że ATP wciąż może związać się i wymusić przełączenie transportera z konformacji skierowanej do wnętrza na konformację skierowaną na zewnątrz oraz przesunąć peptyd, nawet bez Mg2+. Jednak bez Mg2+ transporter nie potrafi efektywnie rozłożyć ATP i w konsekwencji nie może się zresetować do kolejnego cyklu.
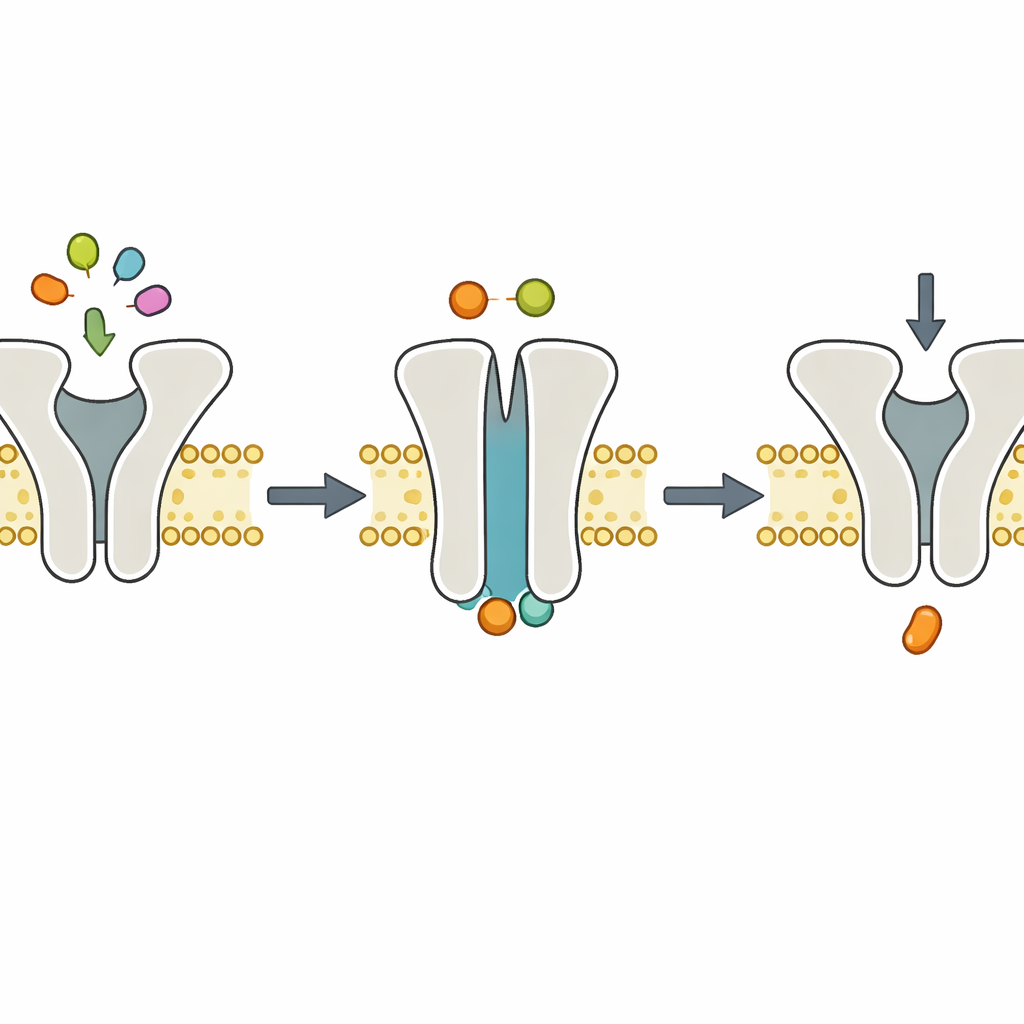
Strukturalne migawki potwierdzają dynamikę
Aby zobaczyć, jak maszyna wygląda podczas tego etapu bez Mg2+, zespół sięgnął po krio-elektronową mikroskopię, która pozwala obrazować szybko zamrożone cząsteczki z niemal atomową szczegółowością. Rekonstytuowali TmrAB w nanodyskach lipidowych, dodali ATP bez Mg2+ i zamrozili kompleksy. Powstałe struktury pokazały TmrAB w konformacji skierowanej na zewnątrz, „zablokowanej” z ATP wciśniętym w oba wewnętrzne miejsca wiążące, lecz bez widocznego Mg2+. Te migawki były zasadniczo nieodróżnialne od wcześniej uzyskanych struktur z obecnym ATP i Mg2+. W połączeniu z badaniami biochemicznymi pokazującymi, że rozkład ATP całkowicie ustaje bez Mg2+, obrazy te wspierają prosty podział zadań: związanie ATP napędza zmianę konformacyjną przesuwającą peptyd, podczas gdy hydroliza ATP zależna od Mg2+ odpowiada za krok przywracający transporter do stanu wyjściowego.
Czytelniejszy obraz działania pompek komórkowych
Obserwując pojedyncze transportery i rozwiązując ich struktury, to badanie rozstrzyga długo toczoną debatę dotyczącą transporterów ABC: mechaniczny „uderzenie” napędzające przesunięcie peptydu jest wywoływane przez samo związanie ATP, a nie przez późniejszy chemiczny rozkład ATP. Mg2+ odgrywa tu główną rolę w umożliwieniu rozszczepienia ATP, co z kolei resetuje transporter i pozwala mu działać ponownie. Poza wyjaśnieniem fundamentalnej kwestii biologii komórki, podejście pojedynczej cząsteczki oferuje też plan działania do rozkładania innych maszyn błonowych leżących u podstaw odporności, oporności na leki i wielu chorób — cząsteczka po cząsteczce i krok transportu po kroku transportu.
Cytowanie: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Słowa kluczowe: Transportery ABC, Związanie ATP, FRET pojedynczej cząsteczki, transport przez błonę, TAP i TmrAB