Clear Sky Science · pl
Nanocząstki błękitu pruskiego celujące w wielotorowy PANoptosom pośredniczący w PANoptozie w terapii urazu niedokrwienno-reperfuzyjnego mięśnia sercowego
Dlaczego ochrona gojącego się serca ma znaczenie
Kiedy osoba doznaje zawału serca, lekarze spieszą się, aby ponownie udrożnić zablokowaną tętnicę i przywrócić przepływ krwi. Ten ratujący życie krok ma jednak ukryty koszt: nagły powrót tlenu może sam w sobie uszkodzić serce, prowadząc do obumierania komórek i stwarzając podłoże do niewydolności serca. W tej pracy badano pomysłową nanomedycynę, której celem jest ochrona serca w tym wrażliwym oknie poprzez jednoczesne blokowanie kilku splecionych ścieżek prowadzących do śmierci komórkowej, co potencjalnie może skutkować łagodniejszym powrotem do zdrowia po zawale.
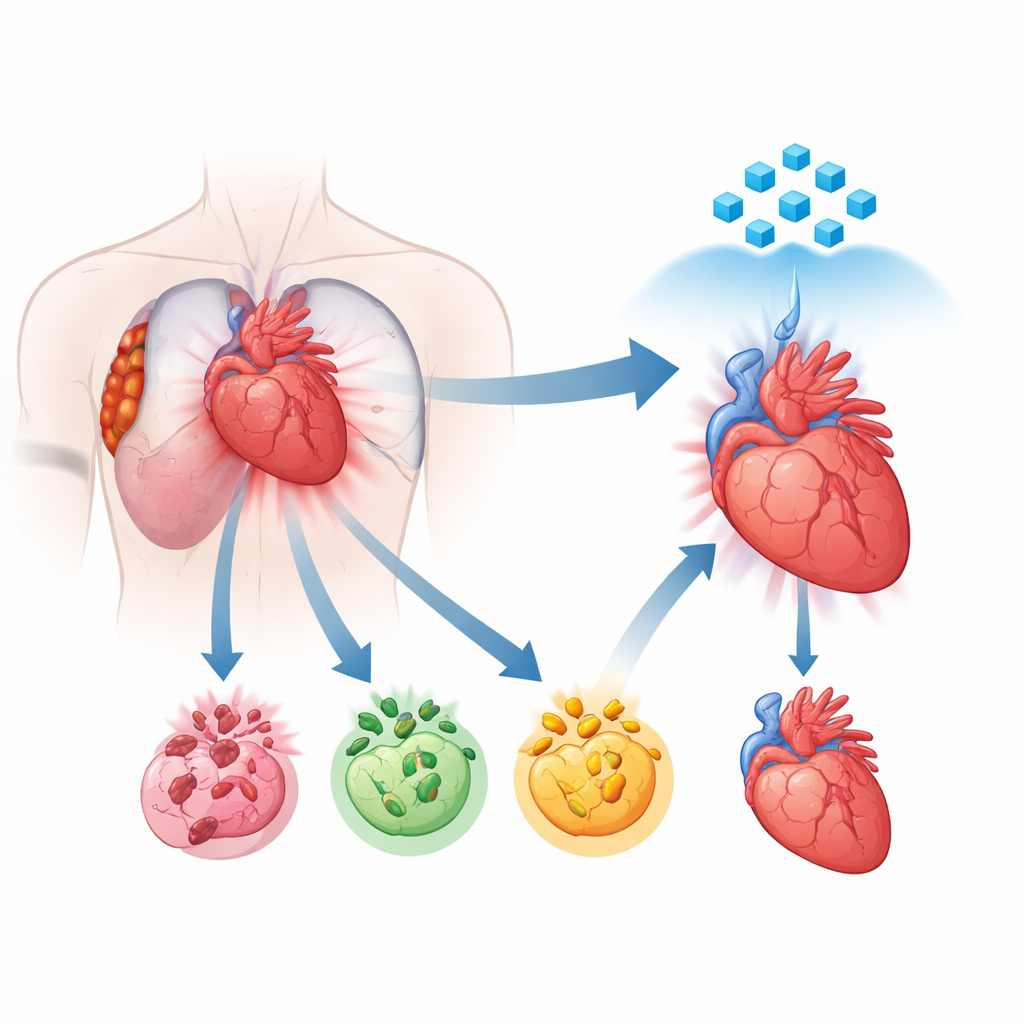
Nowe spojrzenie na to, jak umierają komórki serca
Przez lata naukowcy wiedzieli, że uszkodzone komórki mięśnia sercowego mogą ginąć różnymi zaprogramowanymi drogami, w tym apoptozą, nekroptozą i pyroptozą. Każda ma swój molekularny scenariusz, ale coraz więcej dowodów wskazuje, że te ścieżki nie działają w izolacji. Zamiast tego komunikują się ze sobą i mogą łączyć się w połączony, wymykający się spod kontroli proces zwany PANoptozą. W takim stanie kilka programów śmierci uruchamia się jednocześnie, co sprawia, że terapie blokujące tylko jedną drogę są często nieskuteczne. Autorzy zastosowali sekwencjonowanie RNA z pojedynczych jąder komórkowych tkanek serca ludzkiego od pacjentów po niedawnym zawale, aby zmapować, gdzie i jak silnie te programy śmierci są włączone. Stwierdzili, że w najbardziej uszkodzonych obszarach komórki mięśnia sercowego wykazywały silne przesunięcie w stronę tego połączonego trybu śmierci, wskazując PANoptozę jako centralnego sprawcę urazu.
Projektowanie maleńkiego narzędzia wielofunkcyjnego dla uszkodzonego serca
Aby sprostać tak złożonemu procesowi, zespół zwrócił się ku błękitowi pruskiemu, długo zatwierdzonemu związkowi medycznemu, znanemu przede wszystkim jako antidotum na zatrucia niektórymi metalami. W skali nanometrycznej cząstki błękitu pruskiego zachowują się jak maleńkie katalityczne roboty, które potrafią wygaszać szkodliwe molekuły i wpływać na zachowanie komórek. Dzięki symulacjom komputerowym badacze wykazali, że te nanocząstki mogą bezpośrednio przyłączać się do trzech kluczowych węzłów białkowych — RIPK1, ZBP1 i AIM2 — które pomagają składać molekularną maszynerię PANoptozy. Poprzez wiązanie się z tymi węzłami w różny sposób, przewidywano, że cząstki będą zakłócać budowę kompleksów indukujących śmierć, które koordynują trzy ścieżki prowadzące do obumierania komórek.
Skierowanie nanocząstek bezpośrednio do uszkodzonej tkanki serca
Nanocząstki działają tylko wtedy, gdy dotrą we właściwe miejsce, dlatego zespół otoczył cząstki błękitu pruskiego naturalnymi błonami pozyskanymi z płytek krwi — komórek krwi, które kierują się ku uszkodzonym naczyniom. To powleczenie stworzyło PB@PM, biomimetyczny nośnik krążący jak płytka krwi, ale dostarczający terapeutyczny ładunek. U myszy poddanych kontrolowanemu zawałowi i ponownemu udrożnieniu tętnicy obrazowanie wykazało, że PB@PM kumulowały się znacznie silniej w uszkodzonym obszarze serca niż cząstki niepowlekane, przy jednoczesnym unikaniu zdrowych narządów. Co ważne, powlekane cząstki były dobrze tolerowane: badania krwi i analizy tkanek nie ujawniły oczywistej toksyczności, co wspiera ich potencjał do dalszego rozwoju.
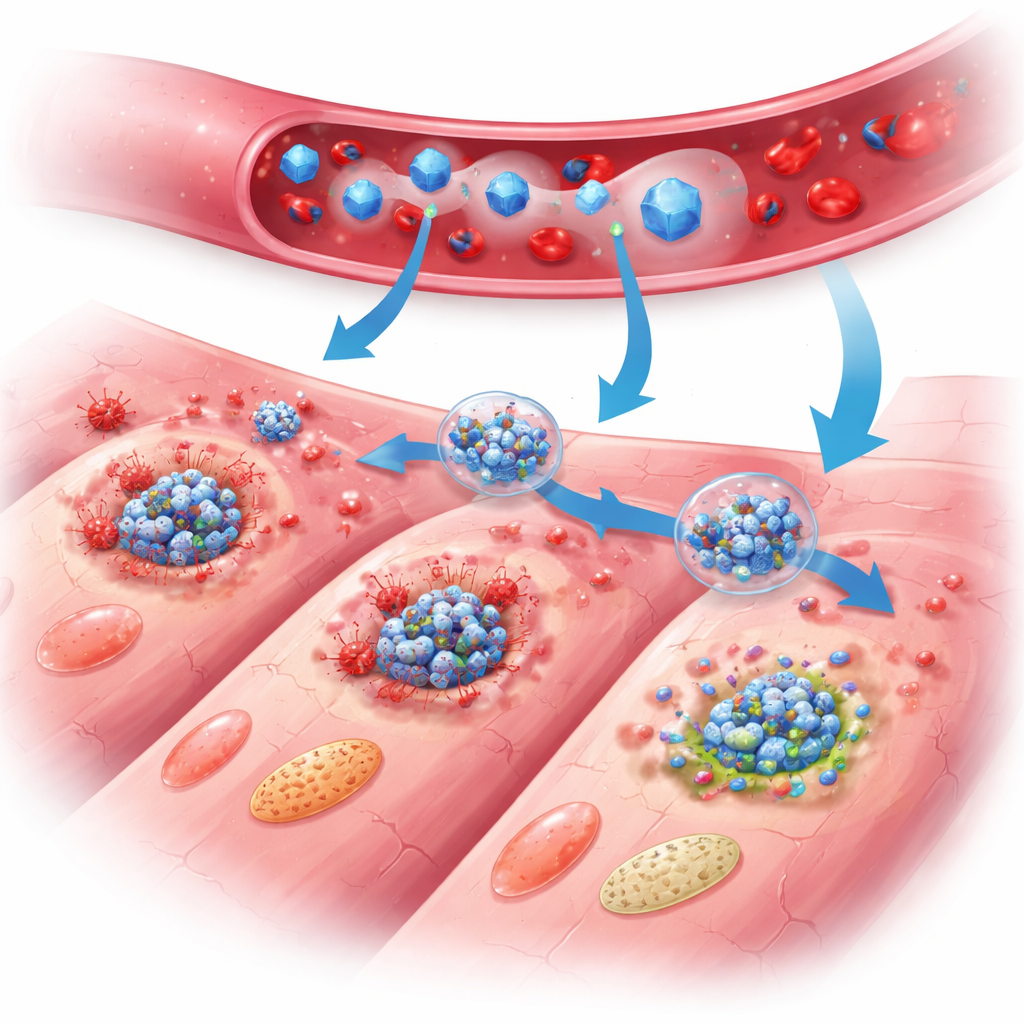
Jak nano-tarcza chroni serce
U leczonych myszy korzyści płynące z PB@PM stały się widoczne w ciągu dni i tygodni. Funkcja pompująca serce poprawiła się, rozmiar blizny zmniejszył się, a ściana serca ulegała mniejszemu przerzedzeniu w porównaniu z nieleczonymi zwierzętami. Szczegółowe badania tkanek ujawniły mniej umierających komórek mięśnia sercowego, spokojniejsze komórki zapalne oraz lepiej zorganizowaną tkankę naprawczą z zdrowszym wzrostem naczyń krwionośnych i mniejszym nieprawidłowym powiększeniem się ocalałych komórek. Na poziomie molekularnym szerokie profilowanie ekspresji genów i pomiary białek wykazały, że PB@PM jednocześnie wyciszały trzy główne ścieżki zaprogramowanej śmierci, zakłócały składanie wielobiałkowych kompleksów PANoptozy i obniżały poziomy cząsteczek sygnalizacyjnych napędzających zapalenie. Cząstki również usuwały szkodliwe reaktywne formy tlenu, stabilizowały mitochondria — elektrownię komórki — i przywracały bardziej normalny metabolizm energetyczny, usuwając kluczowe wyzwalacze, które w przeciwnym razie popychałyby komórki ku autodestrukcji.
Co to może znaczyć dla przyszłej opieki po zawale
Mówiąc wprost, praca pokazuje, że sprytnie zaprojektowana nanocząstka może działać jak wielotorowa tarcza dla serca, tłumiąc splot destrukcyjnych sygnałów śmierci zamiast ścigać jedną ścieżkę po kolei. Dzięki ukierunkowaniu na uszkodzoną tkankę serca, wiązaniu kluczowych białek kontrolnych oraz łagodzeniu stresu oksydacyjnego i zapalnego, PB@PM zdecydowanie ograniczały reakcję łańcuchową utraty komórek i bliznowacenia, która często następuje po przywróceniu przepływu w zablokowanej tętnicy. Choć przed zastosowaniem u pacjentów wymaga to jeszcze wielu badań, badanie stanowi dowód koncepcji, że celowanie w PANoptozę jako całość — i robienie tego za pomocą inteligentnych, inspirowanych biologicznie cząstek — może otworzyć nowy rozdział w ochronie serca po zawale.
Cytowanie: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Słowa kluczowe: niedokrwienno-reperfuzjne uszkodzenie mięśnia sercowego, terapia nanopartikularna, zaprogramowana śmierć komórki, zapalenie serca, ochrona mitochondriów