Clear Sky Science · pl
RPA bezpośrednio stymuluje procesywność helikazy Mer3, zapewniając prawidłowe powstawanie crossing‑over w mejozie
Jak komórki przetasowują DNA, by tworzyć zdrowe jajeczka i plemniki
Za każdym razem, gdy roślina, zwierzę czy człowiek wytwarza jajeczka lub plemniki, komórki muszą przetasować chromosomy, tak aby każde potomstwo otrzymało świeżą mieszankę DNA od rodziców. To genetyczne przetasowanie zależy od starannie rozmieszczonych wymian DNA, czyli crossing‑overów, między parami chromosomów. Opisywane badanie ujawnia, jak dwa kluczowe białka — Mer3 i RPA — współdziałają jak mikroskopijna maszyna, aby zapewnić efektywne i bezpieczne tworzenie tych crossing‑overów. Ma to znaczenie dla płodności, ewolucji, a być może także dla badań nad rakiem.
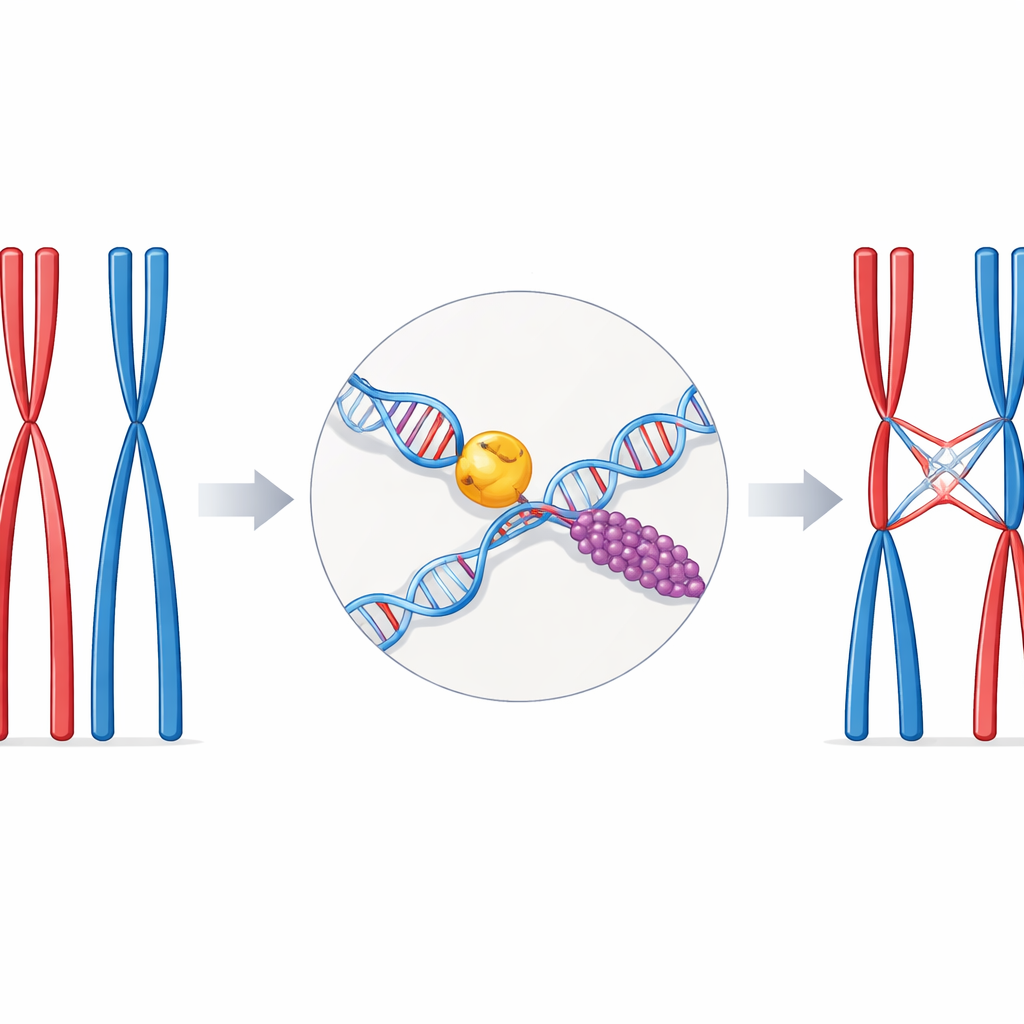
Delikatna równowaga w rozmnażaniu płciowym
Podczas specjalnego podziału komórkowego zwanego mejozą chromosomy występują w dopasowanych parach, po jednym od każdego z rodziców. Aby te pary mogły się prawidłowo rozdzielić, muszą być fizycznie połączone w kilku dobrze dobranych miejscach wzdłuż swojej długości. Te połączenia to crossing‑overy — odcinki, w których nici DNA jednego chromosomu są wymieniane z niciami jego partnera. Zbyt mało crossing‑overów zwiększa ryzyko nieprawidłowego rozdziału chromosomów i niepłodności; zbyt wiele lub źle rozmieszczonych może uszkodzić genom. Komórki polegają więc na wyspecjalizowanych ścieżkach naprawczych i białkach pomocniczych, które przekształcają niebezpieczne pęknięcie DNA w kontrolowany crossing‑over.
Poznaj Mer3 i RPA, zespół rozwijający DNA
Naukowcy skupili się na Mer3, molekularnym silniku, który rozwija DNA i wspiera powstawanie crossing‑overów. Jego ludzki odpowiednik, HFM1, jest znany jako ważny dla płodności. Odkryli, że Mer3 wiąże się bezpośrednio z RPA — kompleksem białkowym, który zazwyczaj osłania jednoniciowe DNA, chroniąc je i rekrutując inne czynniki naprawcze. Dzięki testom biochemicznym, modelowaniu strukturalnemu i badaniom interakcji zmapowano konkretne miejsce dokowania, gdzie krótki „ogon” Mer3 wpasowuje się w szczelinę jednej podjednostki RPA. To miejsce interakcji jest konserwowane od drożdży po ssaki, co sugeruje, że ewolucja wielokrotnie wykorzystywała to rozwiązanie do kontroli naprawy DNA podczas mejozy.
Obserwowanie pojedynczego silnika DNA w akcji
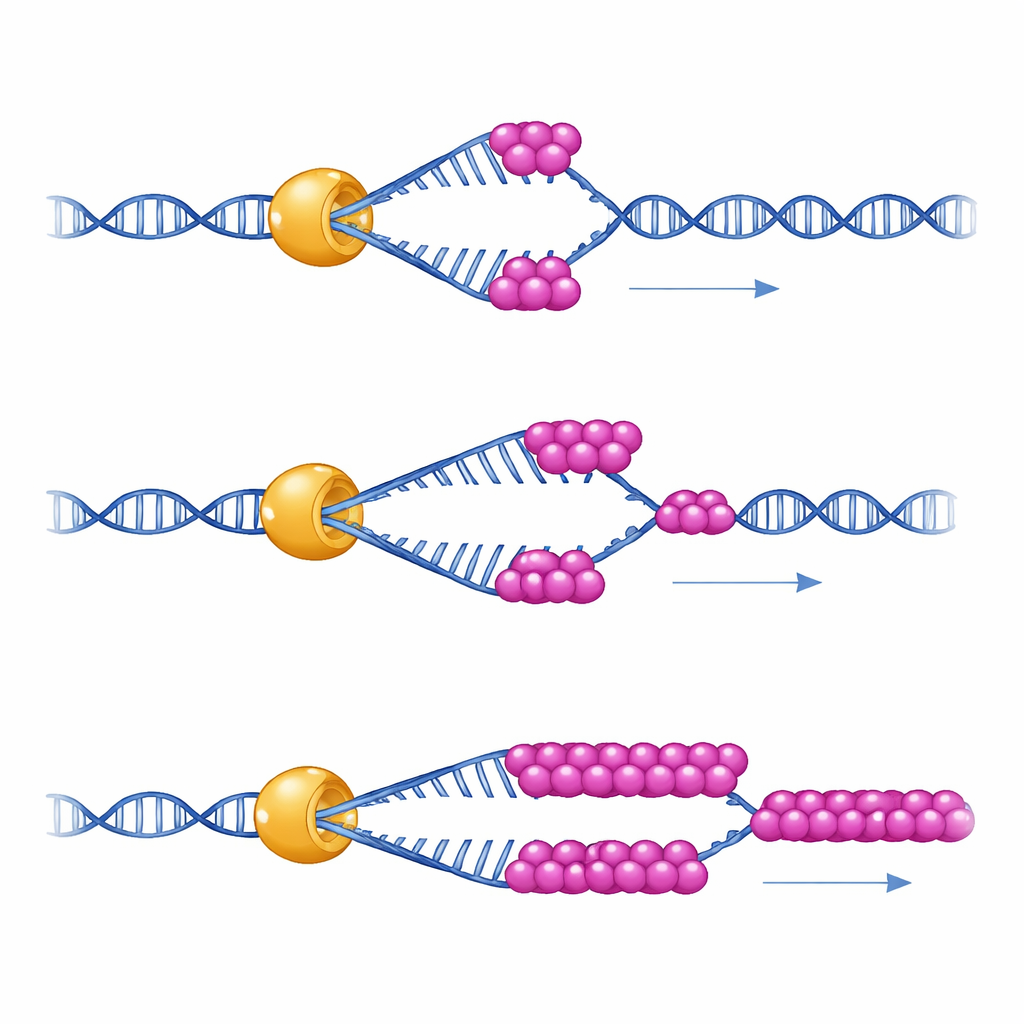
Aby zobaczyć, co faktycznie robi to partnerstwo, badacze użyli pojedynczocząsteczkowych pęset magnetycznych — instrumentu, który trzyma pojedynczą spinkę DNA jak maleńką sprężynę i mierzy, jak pojedyncza cząsteczka Mer3 ją rozwija w czasie. Stwierdzili, że Mer3 porusza się po DNA z równomierną prędkością nawet samodzielnie. Jednak w warunkach imitujących względnie niskie naprężenia fizyczne panujące w komórkach, Mer3 ma tendencję do odpuszczania DNA po rozwinięciu tylko krótkiego odcinka. Gdy obecna jest niewielka ilość RPA, Mer3 nagle staje się znacznie bardziej wytrwały: może rozwijać dużo dłuższe odcinki DNA bez odpadania, szczególnie gdy DNA ma skłonność do ponownego zaginania się. Mutant Mer3 zaprojektowany tak, by zaburzyć ogon wiążący RPA, nie zyskuje tej dodatkowej wytrzymałości, co ujawnia, że to bezpośredni kontakt z RPA zwiększa procesywność Mer3.
Konsekwencje dla crossing‑overów w żywych komórkach
Następnie zespół sprawdził, co dzieje się w rzeczywistych komórkach drożdży, gdy Mer3 nie może właściwie chwytać RPA. Zastąpili normalny gen MER3 mutantem nieprawidłowo wiążącym RPA i obserwowali mejozę. Komórki te nadal mogły dzielić się i tworzyć spory, ale ich płodność spadła, a ogólna liczba crossing‑overów w niektórych rejonach chromosomów zmniejszyła się. Szczegółowa analiza DNA wykazała więcej zdarzeń naprawczych kończących się jako non‑crossovers oraz gromadzenie się nierozwiązanych pośrednich produktów rekombinacji. Mapowanie rozmieszczenia Mer3 w całym genomie ujawniło, że mutant był słabiej rekrutowany do miejsc zaprogramowanych pęknięć DNA, choć jego wczesne wiązanie z osiami chromosomowymi wyglądało normalnie. Innymi słowy, bez silnego wiązania z RPA Mer3 nie utrzymuje się wystarczająco długo w miejscach pęknięć, by niezawodnie skierować je na drogę prowadzącą do crossing‑overów.
Co to oznacza dla płodności i stabilności genomu
Podsumowując, badanie pokazuje, że RPA robi więcej niż tylko pokrywa odsłonięte DNA; bezpośrednio modulując zachowanie kluczowej helikazy mejozy. Poprzez dokowanie do RPA Mer3 staje się bardziej zdecydowanym rozwijaczem DNA, zdolnym wydłużać i stabilizować połączone struktury DNA, które dojrzewają do crossing‑overów. Gdy ta interakcja słabnie, komórki przesuwają się w stronę bezpieczniejszych, lecz mniej użytecznych ścieżek naprawczych i pozostawiają więcej nierozwiązanych pośredników, co subtelnie podważa prawidłowy rozdział chromosomów. Ponieważ te same cząsteczki występują u ludzi — a mutacje w HFM1 wiąże się z niepłodnością — praca ta dostarcza mechanistycznej ramy dla zrozumienia, jak niewielkie zmiany na styku białek mogą mieć dalekosiężne skutki dla zdrowia reprodukcyjnego i różnorodności genetycznej przyszłych pokoleń.
Cytowanie: Altmannova, V., Orlić, L., Carrasco, C. et al. RPA directly stimulates Mer3 helicase processivity to ensure normal crossover formation in meiosis. Nat Commun 17, 2621 (2026). https://doi.org/10.1038/s41467-026-69985-x
Słowa kluczowe: mejoza, rekombinacja genetyczna, helikaza DNA, płodność, crossing‑over chromosomów