Clear Sky Science · pl
Zakłócenie odpowiedzi na uszkodzenia DNA przez fosforotio-oksydowane antysensowe oligonukleotydy
Kiedy pomocne terapie genowe wprowadzają załogę naprawczą komórki w błąd
Antysensowe oligonukleotydy, w skrócie ASO, to rosnąca klasa leków precyzyjnych zaprojektowanych do wyłączania lub uruchamiania pojedynczych genów. Są już stosowane w leczeniu niektórych rzadkich chorób genetycznych i testowane w wielu kolejnych wskazaniach. Badanie to ujawnia nieoczekiwaną wadę jednej powszechnej modyfikacji chemicznej stosowanej, by zwiększyć trwałość tych leków: w określonych warunkach może ona oszukać komórkę, sprawiając, że ta „uwierzy”, iż jej DNA jest uszkodzone, blokując mechanizmy naprawcze i zagrażając długoterminowej stabilności genomu.
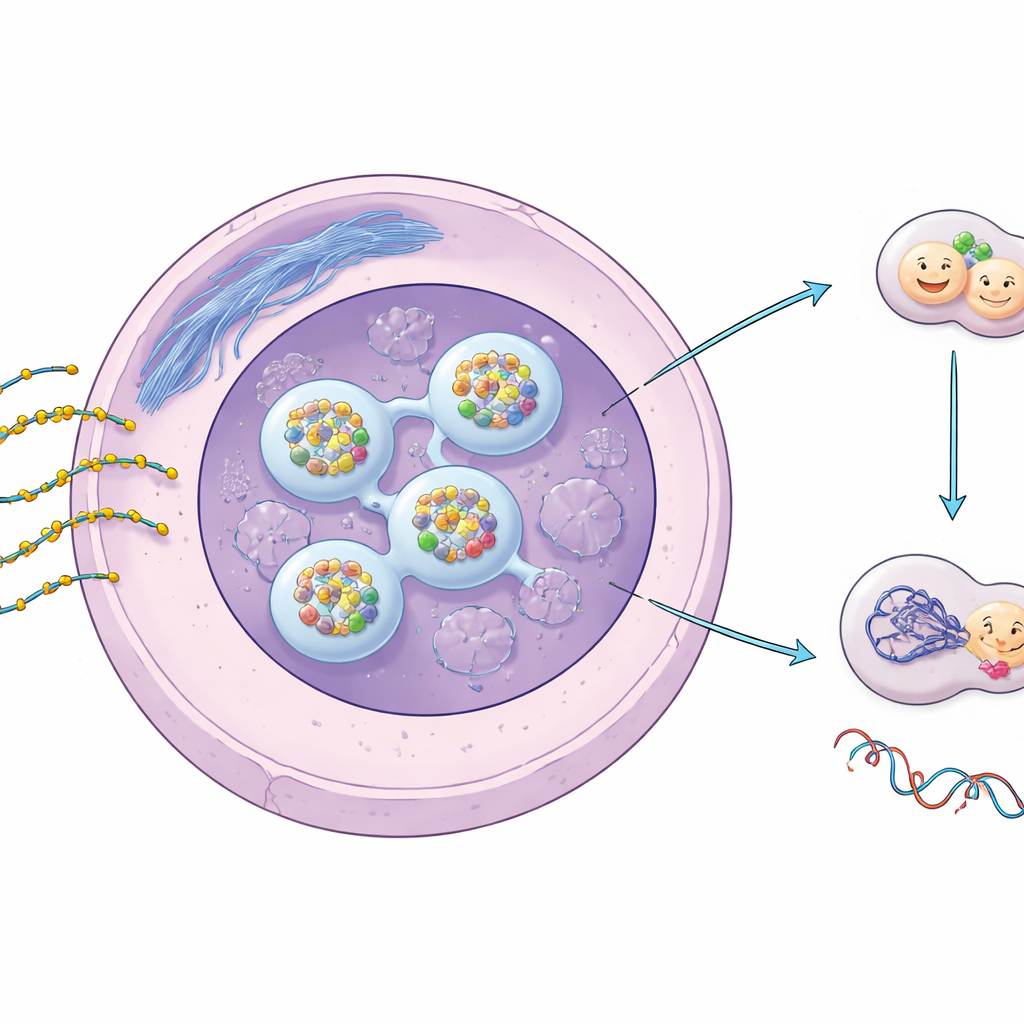
Projektowane przełączniki genowe i ich chemiczne ulepszenie
ASO to krótkie, jednoniciowe cząsteczki materiału genetycznego zaprojektowane do rozpoznawania i wiązania konkretnych komunikatów RNA w komórce, dzięki czemu je wyciszają lub modyfikują. Aby przetrwać w organizmie i efektywnie wnikać do komórek, większość terapeutycznych ASO zawiera modyfikację fosforotio- (PS), w której atom siarki zastępuje atom tlenu w szkielecie łańcucha. Ta niewielka zmiana znacząco zwiększa ich trwałość i skłonność do oddziaływań z białkami. Wcześniejsze prace wykazały, że PS‑ASO gromadzą się w odrębnych punktach w jądrze komórkowym i mogą stresować określone struktury jądrowe, ale konsekwencje dla naprawy DNA i bezpieczeństwa długoterminowego pozostawały niejasne.
Sztuczne krople naśladujące prawdziwe miejsca naprawy DNA
Autorzy śledzili fluorescencyjnie znakowane PS‑ASO w komórkach ludzkich i stwierdzili, że przy powszechnie stosowanych dawkach eksperymentalnych szybko kumulują się w jądrze i inicjują powstawanie nowych sferycznych struktur zwanych ciałami PS. Ciała te tworzą się zależnie od stężenia i zachowują się jak krople ciekłe, które łączą się, rozpuszczają i zależą od słabych sił międzycząsteczkowych — cechy charakterystyczne separacji fazowej ciecz–ciecz. Co istotne, nie znajdują się tam, gdzie występują faktyczne pęknięcia DNA, i nie zawierają typowych markerów złamanej nici. Zamiast tego badanie pokazuje, że kluczowe enzymy naprawy DNA — w tym DNA‑PKcs, ATM, ATR i PARP1 — wiążą się bezpośrednio z PS‑ASO i są silnie wzbogacone wewnątrz tych sztucznych kropli, mimo że podstawowe DNA pozostaje nienaruszone.
Fałszywe alarmy uruchamiają sygnały uszkodzeń komórki
Po zmontowaniu, krople inicjowane przez ASO robią więcej niż biernie uwięzić białka: aktywują te enzymy naprawcze. W ciągu godziny od wejścia ASO enzymy w tych kroplach ulegają aktywacji i zaczynają modyfikować pobliską chromatynę, znakując białka histonowe chemicznymi modyfikacjami zwykle obserwowanymi po prawdziwych uszkodzeniach DNA. To uruchamia pełną odpowiedź na uszkodzenia DNA — rekrutuje dodatkowe czynniki naprawcze, włącza sygnalizację punktów kontrolnych i ogranicza aktywność kinaz cyklu komórkowego zwanych CDK. W efekcie komórki spowalniają lub zatrzymują przejście przez kluczowe fazy cyklu komórkowego, szczególnie tam, gdzie zwykle sprawdzają integralność DNA przed podziałem. W mózgach myszy poddanych klinicznie istotnemu sposobowi podania ASO badacze zaobserwowali również nasilone sygnalizowanie uszkodzeń DNA w obszarach o wyższym wychwycie ASO, co wskazuje, że efekty te nie ograniczają się do hodowli komórkowych.
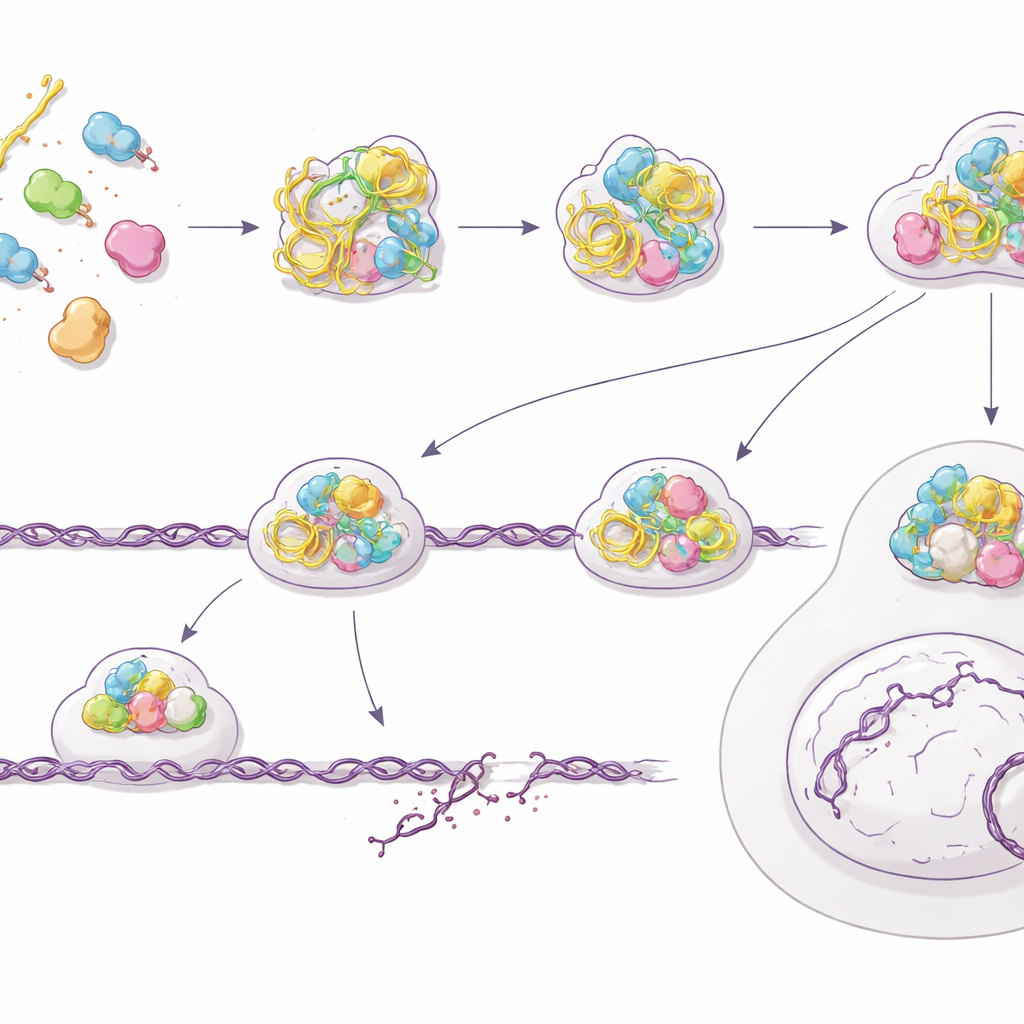
Naprawa idąca źle i narastające obciążenie złamaniami DNA
Paradoksalnie, podczas gdy system alarmowy komórki jest uruchomiony, jej rzeczywista zdolność do naprawy groźnych pęknięć DNA pogarsza się. Zespół wykazał, że komórki wstępnie traktowane PS‑ASO mają trudności z usuwaniem uszkodzeń po napromieniowaniu i nawet kumulują więcej spontanicznych złamań, mierzone testami typu comet i utrzymującymi się ogniskami naprawczymi. Dokładniejsza analiza jednej z najdokładniejszych ścieżek naprawy — rekombinacji homologicznej — ujawniła problem: kluczowe białka takie jak BRCA2 i RAD51 nie potrafią prawidłowo zgromadzić się przy końcach złamanej nici DNA, podczas gdy wcześniejsze markery przetwarzania tych końców nadal się pojawiają. Z użyciem systemu raportującego autorzy oszacowali około 60% spadek wydajności rekombinacji homologicznej po ekspozycji na PS‑ASO. Komórki stają się ogólnie mniej żywotne i znacznie bardziej wrażliwe na promieniowanie, co jest zgodne z sytuacją, w której system naprawczy jest sygnalizowany, ale nieprawidłowo wdrażany.
Co to oznacza dla przyszłości leków celujących w geny
Podsumowując, badanie sugeruje, że modyfikowane fosforotio‑ASO mogą nukleować sztuczne krople ciekłe w jądrze, które koncentrują i aktywują enzymy naprawy DNA nawet wtedy, gdy nie ma uszkodzeń do naprawy. Ten przewlekły fałszywy alarm zaburza normalne wybory naprawcze, zwłaszcza dokładną rekombinację homologiczną, prowadząc do utrwalonych uszkodzeń DNA, aktywacji punktów kontrolnych i śmierci komórek. Choć najsilniejsze efekty zaobserwowano przy wysokich poziomach jądrowych ASO typowych dla eksperymentów translacyjnych, subtelna aktywacja sygnalizacji uszkodzeń jest wykrywalna nawet przy niższych, przypominających dawki lekowe. Dla pacjentów i deweloperów leków przesłanie jest jasne: cechy chemiczne, które czynią ASO skutecznymi lekami, w niektórych kontekstach mogą zakłócać najfundamentalniejszą ochronę komórki — jej zdolność do utrzymania stabilnego genomu — podkreślając potrzebę projektowania bezpieczniejszych szkieletów i monitorowania ścieżek naprawy DNA podczas terapii.
Cytowanie: Hjelmgren, L., Zhou, Q., Schmidli, S. et al. Dysregulation of the DNA damage response by phosphorothioate antisense oligonucleotides. Nat Commun 17, 2111 (2026). https://doi.org/10.1038/s41467-026-69980-2
Słowa kluczowe: antysensowe oligonukleotydy, odpowiedź na uszkodzenia DNA, separacja fazowa ciecz–ciecz, rekombinacja homologiczna, stabilność genomu