Clear Sky Science · pl
Chiralne peptydoglikanowe naśladownictwa celują w biosyntezę ściany komórkowej bakterii w celu interwencji przeciw patogenom
Nowy sposób polowania na szkodliwe zarazki
Zakażenia odporne na antybiotyki rosną na całym świecie, a lekarzom wciąż brakuje narzędzi, które potrafiłyby precyzyjnie wykrywać i atakować groźne bakterie, nie szkodząc przy tym naszym komórkom. W tym badaniu przedstawiono sprytny molekularny „wabik”, który naśladuje kluczowy element budulcowy ściany komórkowej bakterii. Zaprojektowane cząsteczki mogą zarówno uwidaczniać infekcje do celów obrazowania, jak i dostarczać antybiotyki bezpośrednio do drobnoustrojów, oferując nową strategię walki z trudnymi do leczenia patogenami.
Naśladując bakteryjną zbroję
Bakterie otoczone są wytrzymałą siecią zwaną ścianą komórkową, zbudowaną z cukrów i nietypowych aminokwasów w formie lustrzanej, których nasze komórki w dużej mierze nie używają. Badacze wykorzystali tę różnicę, tworząc długie łańcuchy oparte na cukrach, ozdobione specyficzną lustrzaną formą alaniny. Te łańcuchy, nazywane chiralnymi naśladownictwami peptydoglikanu, zaprojektowano tak, by ściśle przypominały naturalne składniki wykorzystywane przez bakterie do budowy ściany, a jednocześnie nie występowały w tkankach ssaków. Poprzez precyzyjne dostrojenie ilości przyłączonej alaniny w formie D zespół uzyskał wersje, które zdecydowanie preferowały bakterie nad komórkami ludzkimi.
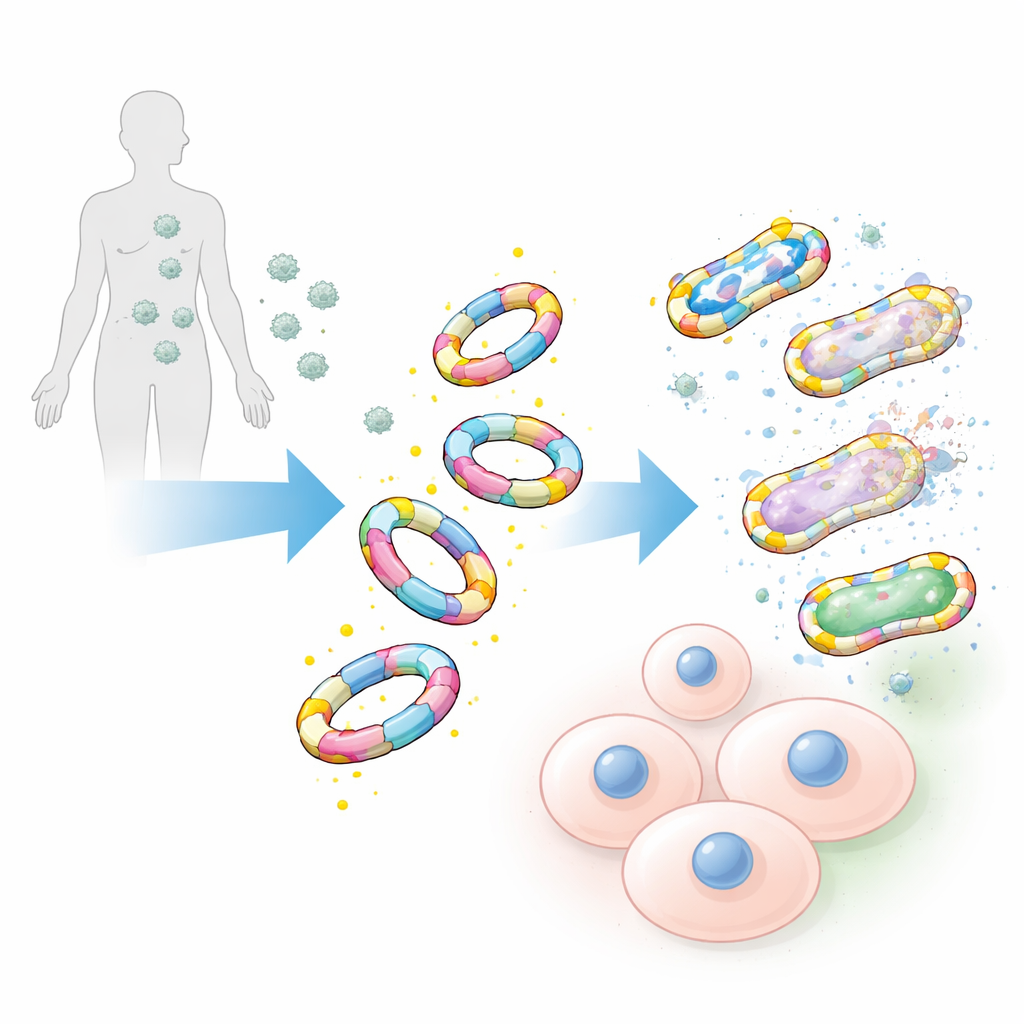
Przyczepiają się do bakterii, nie do naszych komórek
W testach przeciw szerokiemu zakresowi patogenów, w tym znanym szczepom szpitalnym takim jak metycylinooporny Staphylococcus aureus i innym bakteriom z grupy ESKAPE, naśladownictwa ozdobione D-alaniną wiązały się z powierzchnią bakterii z uderzającą skutecznością. Ich lustrzane odpowiedniki zbudowane z formy L alaniny oraz same łańcuchy cukrowe wykazywały tylko słabe lub znikome wiązanie. Zespół porównał też te duże naśladownictwa z tradycyjnymi małymi sondami chemicznymi opartymi na pojedynczych cząsteczkach D-alaniny. Nawet gdy małe sondy były bardzo jasne, nadal znakowały znacznie mniej bakterii i dawały słabsze sygnały, co podkreśla przewagę większego, bardziej zbliżonego do naturalnego projektu.
Przejmując linię montażową ściany komórkowej
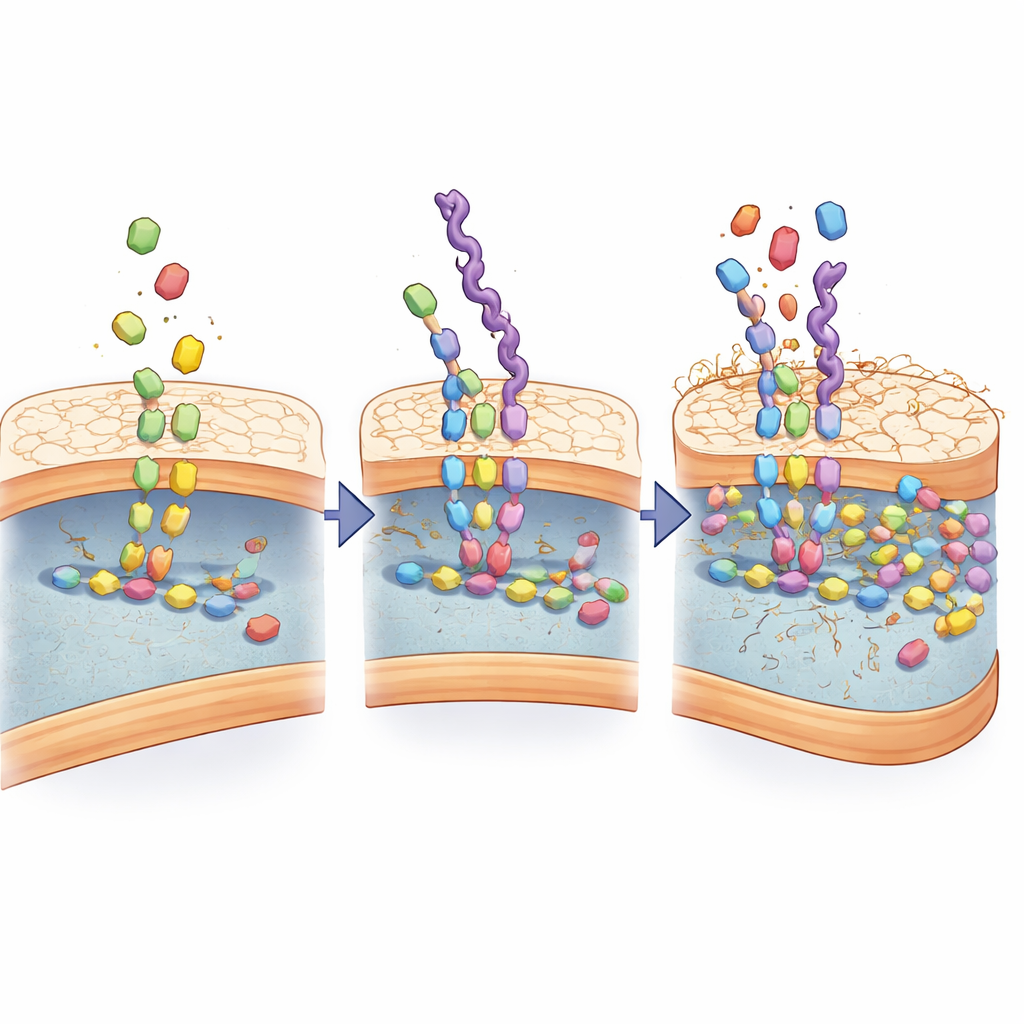
Aby zrozumieć, dlaczego rozpoznawanie jest tak silne, naukowcy zbadali, jak naśladownictwa oddziałują z maszynerią budującą ścianę komórkową bakterii. Odkryli, że łańcuchy oparte na D-alaninie nie tylko przylegają z zewnątrz; są pobierane, jakby były autentycznymi blokami budulcowymi i włączane w te same enzymatyczne etapy, które normalnie łączą składniki ściany. Analiza chemiczna wykryła nowe pośrednie cząsteczki, które pojawiają się tylko w obecności tych naśladownictw, a symulacje komputerowe pokazały, że kluczowe enzymy budujące ścianę chwytają naśladownictwa jeszcze mocniej niż naturalne substraty. W kolejnych cyklach wzrostu bakterii naśladownictwa kumulowały się w ścianie, stopniowo zniekształcając jej strukturę i czyniąc ją bardziej przepuszczalną.
Zmiana naśladownictw w inteligentne nośniki leków
Ponieważ te łańcuchy naturalnie tworzą w wodzie maleńkie cząstki i niosą wiele miejsc chemicznych do modyfikacji, zespół wykorzystał je jako rusztowania dla barwników obrazujących i antybiotyków. Fluorescencyjne wersje wyraźnie obrysowywały bakterie w hodowlach komórkowych, przy minimalnej interakcji z komórkami ssaczymi hodowanymi obok. Następnie badacze załadowali antybiotyk tetracyklinę do cząstek opartych na naśladownictwach. W testach laboratoryjnych takie opakowanie uczyniło tetracyklinę wielokrotnie skuteczniejszą, zabijając nawet szczepy oporne przy znacznie niższych dawkach niż lek wolny. Mikroskopia wykazała, że nośniki z antybiotykiem zgromadziły się na bakteriach, penetrowały ich otoczki i wywoływały rozległą śmierć komórek w porównaniu z nieukierunkowanymi formułami.
Walcząc z infekcjami wewnątrz organizmu
Najtrudniejsze testy przeprowadzono na modelach mysich z zakażeniami miejscowymi ran skórnych i zagrażającymi życiu infekcjami jamy brzusznej. W zakażonych ranach fluorescencyjne naśladownictwa lokowały się przy bakteriach głęboko w tkance i, przenosząc tetracyklinę, niemal całkowicie oczyszczały drobnoustroje. To prowadziło do szybszego gojenia, grubszego nowego naskórka, bardziej uporządkowanego odkładania kolagenu i bogatszego rozwoju naczyń włosowatych. W modelach ogólnoustrojowych naśladownictwa kumulowały się specyficznie w zakażonych narządach, takich jak śledziona i płuca, gdzie w połączeniu z antybiotykiem znacząco zmniejszały liczbę bakterii. Co ważne, wysokie dawki samych naśladownictw wykazały dobrą tolerancję, bez oczywistych uszkodzeń głównych narządów ani zmian w parametrach krwi.
Co to może oznaczać dla przyszłych terapii
Tworząc bliskie chemiczne podobieństwo do składników własnych ściany komórkowej bakterii, ta praca demonstruje nowy sposób „wtopienia się” w metabolizm patogenu zamiast jedynie atakować go z zewnątrz. Te chiralne naśladownictwa służą zarówno jako precyzyjne wskaźniki do obrazowania, jak i inteligentne pojazdy kierujące antybiotyki bezpośrednio do docelowych drobnoustrojów, w tym szczepów opornych, oszczędzając komórki ssaków. Jeśli uda się je przekształcić w narzędzia kliniczne, takie biomimetyczne platformy mogłyby pomóc lekarzom dokładnie zobaczyć, gdzie kryją się infekcje, i leczyć je skuteczniej przy niższych dawkach leków, oferując obiecującą broń przeciw rosnącemu problemowi oporności mikroorganizmów na leki.
Cytowanie: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Słowa kluczowe: oporność na antybiotyki, ściana komórkowa bakterii, ukierunkowane dostarczanie leków, obrazowanie molekularne, nanomedycyna