Clear Sky Science · pl
Komórki Th17 wymagają sensora naprawy DNA xeroderma pigmentosum uzupełnienie Grupa C, by kontrolować utleniające uszkodzenia DNA w modelu myszy
Strażnicy naszych obrońców odpornościowych
Komórki pomocnicze typu 17, czyli Th17, to szczególny rodzaj białych krwinek patrolujących bariery organizmu, takie jak jelita i skóra, by odpierać bakterie i grzyby. Uczestniczą jednak także w chorobach autoimmunologicznych, gdy ich reakcje wymykają się spod kontroli. W tym badaniu zadano pozornie proste pytanie: jak te wysoce aktywne komórki chronią własne DNA przed chemicznym stresem, który same wytwarzają podczas zwalczania infekcji? Odpowiedź skupia się na sensorze uszkodzeń DNA zwanym XPC, znanym przede wszystkim z ochrony komórek skóry przed światłem słonecznym. Naukowcy wykazują tutaj, że XPC jest również kluczowy dla utrzymania Th17 w zdrowiu, z energią i zdolnych do działania.
Jak Th17 zwykle zachowują równowagę
Życie komórek Th17 jest niebezpieczne. By działać, zwiększają metabolizm i produkują reaktywne formy tlenu — cząsteczki chemicznie reaktywne, które mogą uszkadzać DNA. Zespół porównał komórki Th17 z innymi typami limfocytów T u myszy i stwierdził, że mimo intensywnej aktywności Th17 gromadzą mniej uszkodzeń DNA niż wiele ich krewnych. Kluczową wskazówką było silniejsze włączenie genów związanych z naprawą DNA, zwłaszcza z drogi zwykle naprawiającej uszkodzenia wywołane przez słońce. Wśród nich znalazł się XPC, białko skanujące DNA w poszukiwaniu uszkodzeń strukturalnych. W miarę dojrzewania Th17 poziomy XPC rosły i lokalizowały się w miejscach uszkodzeń w jądrze, co sugeruje, że jest ono w ciągłej pogotowiu, by utrzymać integralność genetyczną tych komórek.
Co się dzieje, gdy brakuje sensora DNA
Aby ocenić znaczenie XPC, badacze użyli myszy pozbawionych tego białka. Na pierwszy rzut oka ich układy odpornościowe wyglądały w dużej mierze normalnie: ogólne liczby limfocytów T i wiele podtypów pozostawały niezmienione. Gdy jednak zespół skupił się na komórkach Th17, ujawniła się uderzająca wada. Bez XPC znacznie mniej komórek produkowało charakterystyczną dla Th17 cząsteczkę IL-17, a kluczowe markery tożsamości i przełączniki sygnałowe napędzające program Th17 były przytłumione. W hodowlach komórkowych naiwne limfocyty z tych myszy miały trudności z pełnym przekształceniem się w dojrzałe Th17. W standardowym modelu, w którym przeniesione limfocyty T wywołują zapalenie jelit, komórki T pozbawione XPC nie wywołały zapalenia jelita grubego, co odzwierciedla obniżoną zdolność zapalną. Jednocześnie komórki regulatorowe T, które łagodzą odpowiedzi odpornościowe, stały się bardziej liczne, sugerując przesunięcie równowagi między agresją a hamowaniem.
Uszkodzenia DNA, fabryki energii i stres chemiczny
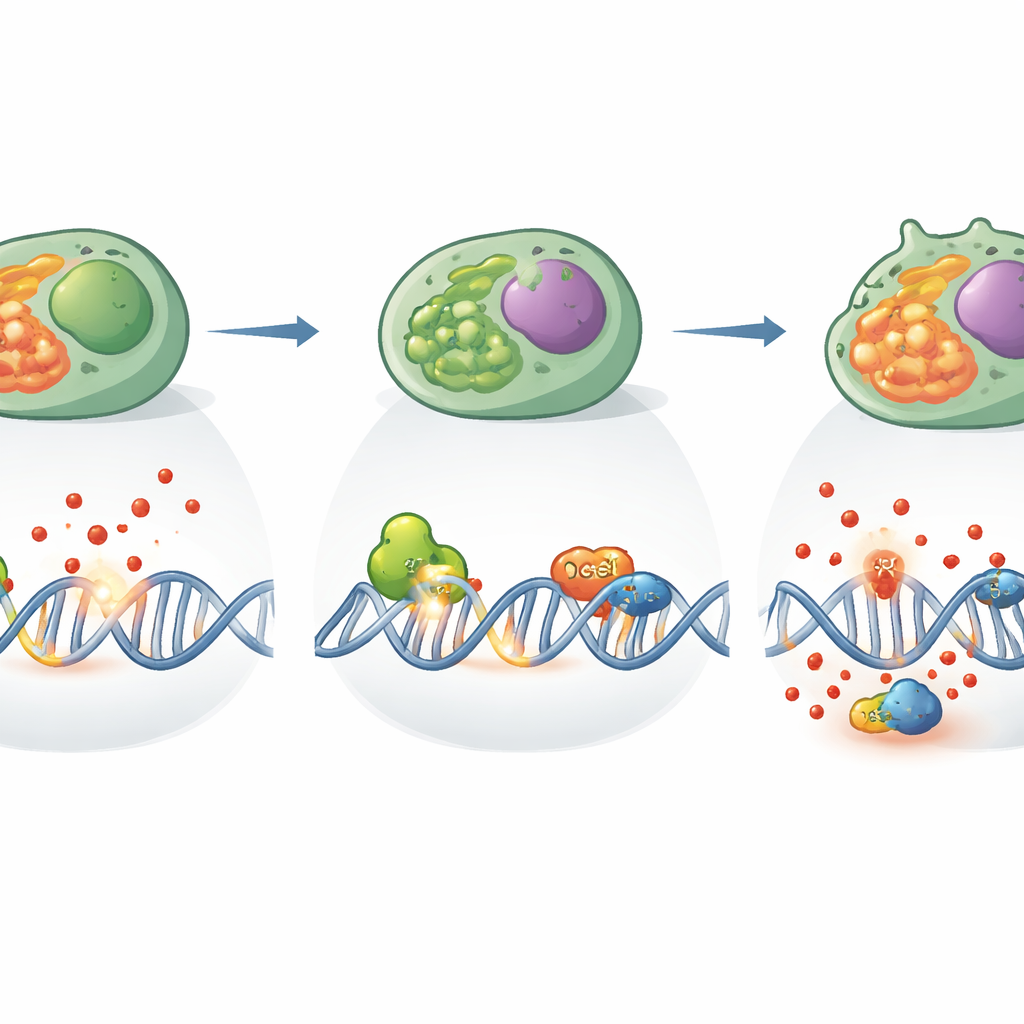
Dekonstrując dalej, zespół odkrył, że Th17 bez XPC miały więcej przerwanych nici DNA i więcej zoksydowanych zasad DNA — sygnaturę ataku przez reaktywne formy tlenu. Geny zazwyczaj wykrywające uszkodzenia DNA i zatrzymujące cykl komórkowy również były zredukowane, co sugeruje osłabiony system alarmowy. Metabolizm energetyczny komórek został przekształcony: straciły część zdolności do korzystania z szybkich szlaków spalania cukrów i stały się bardziej zależne od mitochondriów, małych elektrowni wewnątrz komórek. Jednak te mitochondria wydzielały więcej reaktywnych form tlenu i wykazywały oznaki przeciążenia, tworząc błędne koło narastającego stresu chemicznego i rosnących uszkodzeń DNA. Co znamienne, leczenie komórek przeciwutleniaczem przywróciło produkcję IL-17 i zmniejszyło uszkodzenia DNA, łącząc wprost stres oksydacyjny z obserwowaną dysfunkcją.
Współpraca w naprawie uszkodzonego DNA
Ponad swoją klasyczną rolą XPC współdziałał też z innym białkiem naprawczym, OGG1, które rozpoznaje powszechną zoksydowaną zasadę DNA. Naukowcy wykazali, że oba białka fizycznie się łączą w komórkach Th17, pomagając koordynować usuwanie uszkodzonych zasad. Gdy brakowało XPC, aktywność tnąca OGG1 faktycznie wzrosła, jakby próbowała zrekompensować nadmiar uszkodzeń. Jednak ta nadaktywność następowała w kontekście wysokiego stresu oksydacyjnego i zaburzonych sieci naprawczych i nie była wystarczająca, by przywrócić normalną funkcję Th17. Analizy genetyczne i strukturalne sugerowały, że XPC działa jako węzeł łączący różne ścieżki naprawcze i kontrolę redoks, zapewniając, że uszkodzenia są nie tylko wykrywane, lecz także przetwarzane w sposób pozwalający komórce kontynuować podziały i produkcję ochronnych cząsteczek.
Dlaczego to ma znaczenie dla chorób i terapii
Dla czytelnika popularnonaukowego kluczowy komunikat jest taki: komórki odpornościowe potrzebują swoich wewnętrznych ochroniarzy, by zachować formę, chroniąc nas. Badanie to ujawnia, że XPC, dotąd znane z ochrony komórek skóry przed UV, jest także istotnym strażnikiem komórek Th17, utrzymującym ich DNA w nienaruszonym stanie i stabilizującym systemy energetyczne pod stresem oksydacyjnym. Gdy XPC brakuje, Th17 stają się genetycznie i metabolicznie kruche, produkują mniej czynników zapalnych i mogą przesunąć równowagę immunologiczną w stronę regulacji zamiast ataku. Ponieważ Th17 odgrywają kluczową rolę w schorzeniach takich jak choroba zapalna jelit, łuszczyca czy stwardnienie rozsiane, szlaki kontrolowane przez XPC mogą stać się nowymi celami do modulowania odpowiedzi immunologicznych — zarówno w celu stłumienia szkodliwego zapalenia, jak i wzmocnienia obrony tam, gdzie jest ona zbyt słaba — poprzez wpływ na to, jak te komórki naprawiają DNA i radzą sobie ze stresem oksydacyjnym.
Cytowanie: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
Słowa kluczowe: Komórki Th17, naprawa DNA, stres oksydacyjny, białko XPC, choroba autoimmunologiczna