Clear Sky Science · pl
Wydzielanie białek z ER i mitochondriów zależne od VAMP7 wpływa na mikrośrodowisko guza i zaangażowanie makrofagów
Jak zestresowane komórki dają sygnał o pomoc
Komórki nowotworowe mają trudne życie. Pozbawione tlenu i składników odżywczych gromadzą uszkodzenia w swoich „elektrowniach” (mitochondriach) i w fabrykach białek (retikulum endoplazmatycznym, ER). W tym badaniu odkryto nieoczekiwany sposób, w jaki komórki pod presją wyrzucają na zewnątrz uszkodzone części tych wewnętrznych struktur. W guzach mózgu zwanych glejakami system „wywozu śmieci” sterowany przez białko VAMP7 okazuje się wpływać na to, jak komórki odpornościowe rozpoznają i wnikają do guza.
Ukryte trasy transportu wewnątrz komórek
Większość białek opuszczających komórkę korzysta z klasycznej drogi: wchodzą do ER, przechodzą przez centralną sortownię — aparat Golgiego — i są pakowane do pęcherzyków, które łączą się z błoną komórkową. Komórki korzystają jednak również z niekonwencjonalnych szlaków omijających Golgiego. Jednym z nich są późne endosomy — wewnętrzne pęcherze, które mogą łączyć się z powierzchnią i uwalniać zawartość na zewnątrz. Autorzy skupiają się na molekularnym „zamek” białku VAMP7, już znanym z tego, że pomaga późnym endosomom łączyć się z błoną zewnętrzną i uwalniać małe pęcherzyki zewnątrzkomórkowe, drobne paczki przenoszące ładunek między komórkami.
Przenoszenie zużytych części na wyjście
Wykorzystując zmodyfikowane komórki nerkowe szczura i komórki glejaka pozbawione VAMP7, badacze śledzili los białek zwykle obecnych w ER i mitochondriach. Pokażali, że bez VAMP7 komórki wydzielały znacznie mniej krótkiej formy białka kształtującego ER o nazwie RTN3 oraz mniej VDAC, kanału na powierzchni mitochondriów. Jednocześnie późne endosomy były nieprawidłowo rozmieszczone, a małe pęcherzyki bogate w marker CD63 były słabo wydzielane. Obrazowanie o wysokiej rozdzielczości i testy bliskości wykazały, że RTN3 i materiał mitochondrialny fizycznie kojarzą się z endosomami pozytywnymi dla CD63 przed uwolnieniem, a to przekazanie zależy od VAMP7 i jego partnerów fuzyjnych. Wyniki te wspierają model, w którym zestresowane ER i mitochondria odrywają małe pęcherzyki, które następnie łączą się z późnymi endosomami, a te eksportują ładunek na zewnątrz komórki. 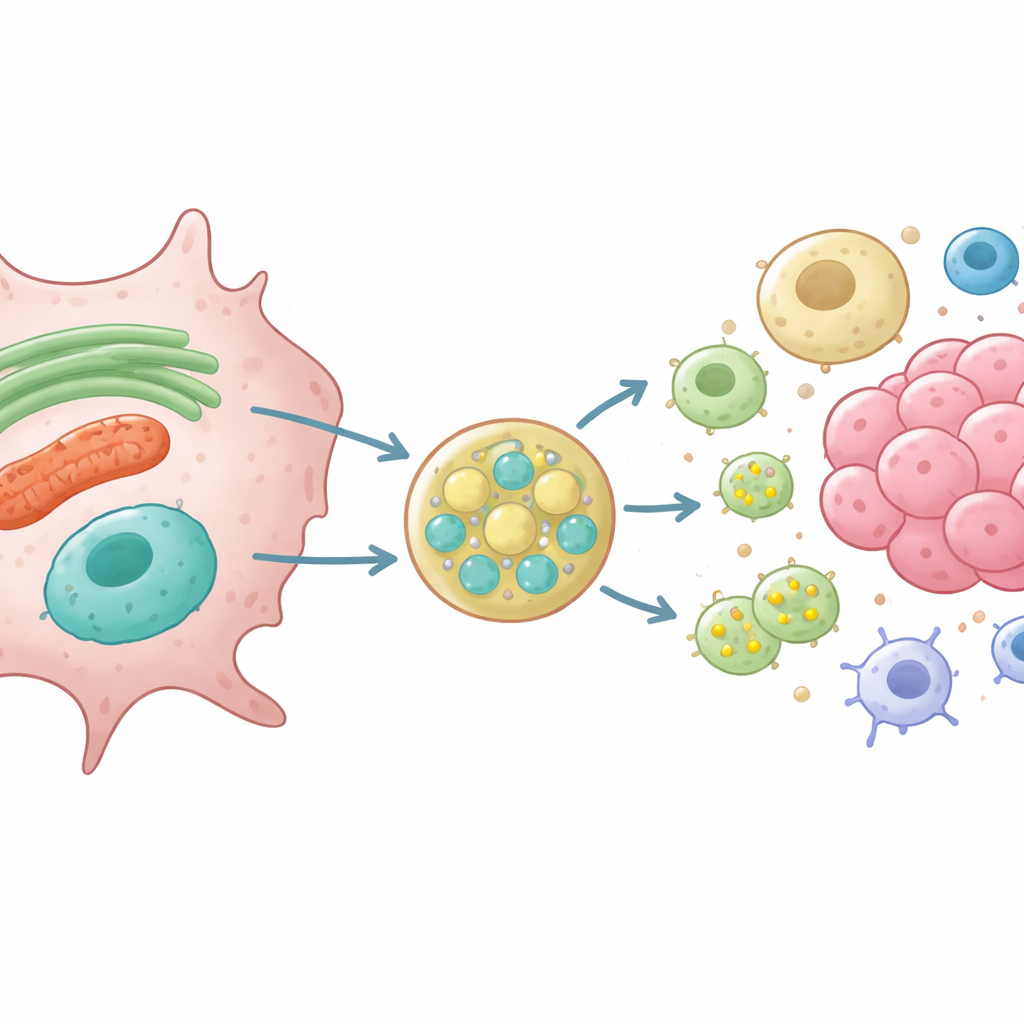
Ulga w stresie i kontrola jakości
Komórki pozbawione VAMP7 nie utraciły ogólnej ścieżki recyklingu znanej jako autofagia, ale wykazywały wyraźne oznaki przeciążenia. Wzorce aktywności genów wskazywały na aktywację odpowiedzi na stres w ER i zmiany w genach związanych z mitochondriami. Mikroskopia ujawniła nieprawidłowe „wirówki” błony ER oraz nadmiernie zespolone, wydłużone mitochondria — obie cechy organelli mających trudności z utrzymaniem równowagi. Pomiary zużycia tlenu wykazały, że pomimo większej masy mitochondrialnej, komórki pozbawione VAMP7 lub kluczowego białka autofagii (ATG5) miały słabszą produkcję energii. Gdy naukowcy celowo wywołali stres ER lub mitochondrialny za pomocą leków, komórki z nienaruszonym VAMP7 zwiększały wydzielanie RTN3 lub VDAC, odpowiednio. Ten wzrost znikał po usunięciu VAMP7, co sugeruje, że wydzielanie przez późne endosomy działa jak zawór bezpieczeństwa pomagający pozbyć się uszkodzonych elementów i przekazywać informację o stanie wewnętrznym komórki.
Kształtowanie sąsiedztwa guza
Aby przetestować znaczenie tego szlaku w chorobie, zespół zwrócił się do modelu szczura glejaka, wysoce agresywnego guza mózgu. Przeszczepili do mózgów szczurów komórki glejaka normalne, pozbawione VAMP7 lub pozbawione ATG5. Guzy rozwijające się z komórek bez VAMP7 były duże i zawierały znacznie więcej martwej tkanki, a jednocześnie były mniej nacieczone przez makrofagi — komórki odpornościowe pochłaniające szczątki i wpływające na to, czy guz rośnie, czy się zatrzymuje. Dla odmiany guzy pozbawione ATG5 były ogólnie mniejsze, ale nie wykazywały tak wyraźnego spadku napływu makrofagów do rdzenia guza. Analizy danych dotyczących ludzkich guzów mózgu dodatkowo ujawniły, że niższe poziomy VAMP7 (i RTN3) wiążą się z gorszym przeżyciem pacjentów, co sugeruje, że ten powiązany ze stresem szlak sekrecyjny może naturalnie działać hamująco na postęp guza przez kształtowanie krajobrazu odpornościowego. 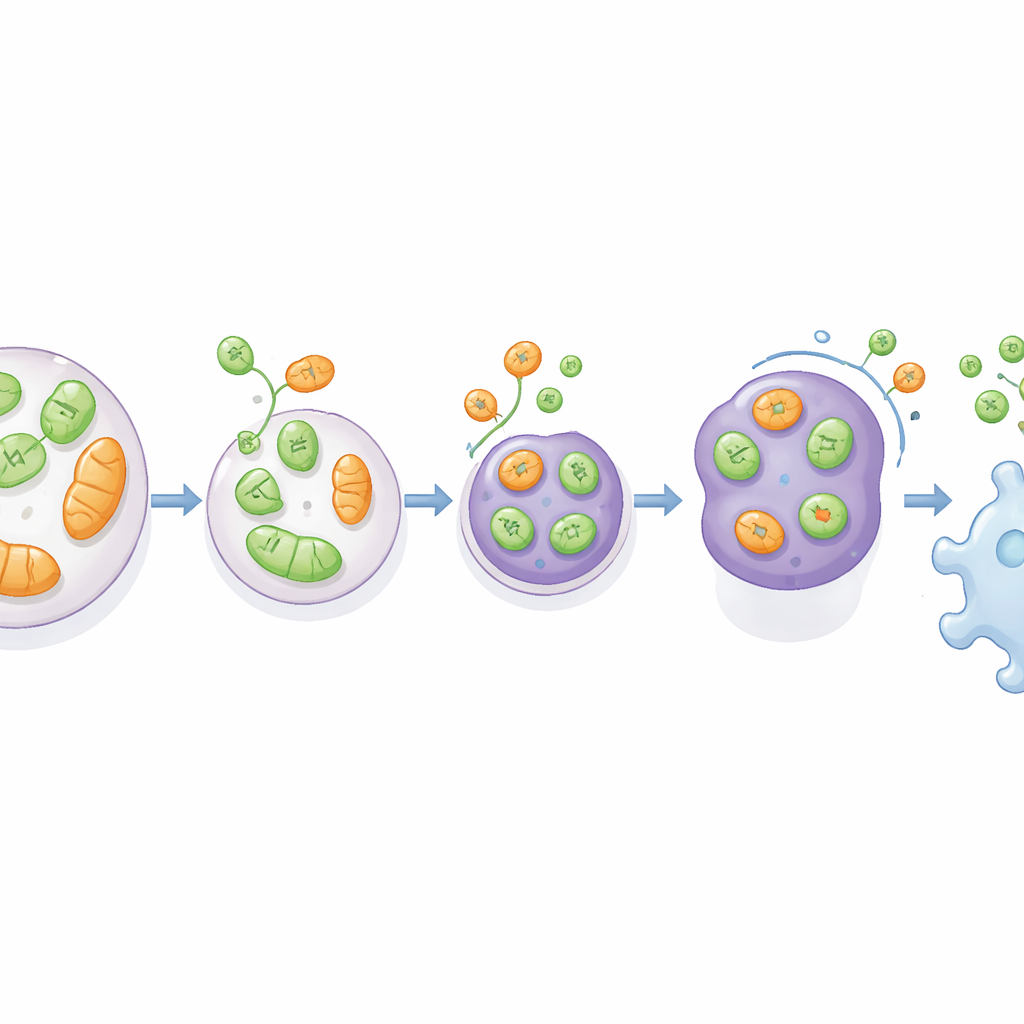
Dlaczego to ma znaczenie dla raka i odporności
Mówiąc krótko, badanie proponuje, że VAMP7 pomaga komórkom pakować i eksportować uszkodzone fragmenty wewnętrznej aparatury poprzez późne endosomy, zwłaszcza pod wpływem stresu. W glejakach ten wypływ materiału pochodzącego z ER i mitochondriów wydaje się działać jako sygnał alarmowy, który zachęca makrofagi do wnikania do guza i usuwania szczątków, przyczyniając się do bardziej hamującego wzrost guza środowiska. Gdy VAMP7 jest nieobecny, sygnał słabnie, uszkodzenia organelli się kumulują, guzy stają się bardziej martwicze, a zaangażowanie makrofagów maleje. Zrozumienie i potencjalne modulowanie tego systemu kontroli jakości w sekrecji mogłoby otworzyć nowe sposoby uczynienia opornych guzów bardziej widocznymi i podatnymi na reakcję układu odpornościowego.
Cytowanie: Vats, S., Dionisio, P., Lemercier, Q. et al. VAMP7-dependent late endosomal secretion of ER and mitochondrial proteins impacts the tumor microenvironment and macrophage engagement. Nat Commun 17, 3012 (2026). https://doi.org/10.1038/s41467-026-69900-4
Słowa kluczowe: niekonwencjonalna sekrecja białek, VAMP7, glejak, mikrośrodowisko guza, pęcherzyki zewnątrzkomórkowe