Clear Sky Science · pl
Czynnik inicjacji eukariotycznej 6 modyfikuje plastyczność drobnokomórkowego raka płuca poprzez oś sygnalizacyjną integryna–FAK
Dlaczego te badania nad rakiem płuca są ważne
Drobnokomórkowy rak płuca (SCLC) jest jedną z najbardziej śmiertelnych postaci raka płuca. Zazwyczaj na początku dobrze odpowiada na chemioterapię, ale niemal zawsze nawraca — i to szybko oraz agresywnie. W tym badaniu zadano kluczowe pytanie: co umożliwia komórkom SCLC „zmianę osobowości” i nabycie oporności na leki, i czy da się tę przemianę spowolnić lub zablokować?
Nowotworowe komórki zmieniające kształt
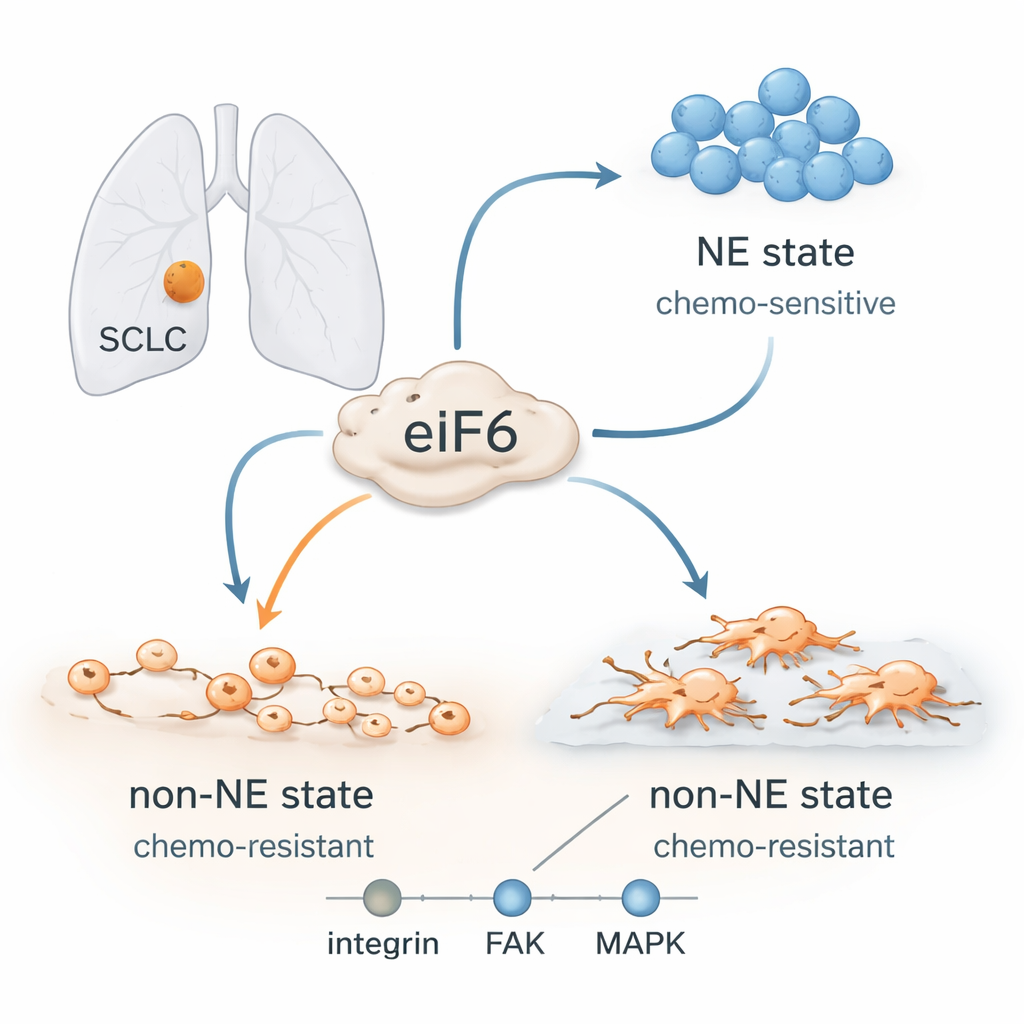
Wcześniej sądzono, że SCLC to choroba jednorodna, jednak dziś wiadomo, że guzy te zawierają różne typy komórek. Niektóre mają silną tożsamość „neuroendokrynną”: rosną w zwartym, pływającym skupisku, dobrze reagują na chemioterapię na bazie platyny i są bogate w określone białka przypominające białka nerwowe. Inne tracą tę tożsamość i przyjmują stan „nieneuroendokrynny”: rozprzestrzeniają się, przyczepiają do otaczającej tkanki, wykazują cechy bardziej ruchliwych, inwazyjnych komórek i są znacznie trudniejsze do zabicia lekami. Guzy pacjentów często ewoluują ze stanu wrażliwego do odpornego podczas lub po leczeniu, mimo że ich DNA nie ulega znacznym zmianom. Wskazuje to na elastyczne programy komórkowe, a nie nowe mutacje, jako motor nawrotu choroby.
Czynnik translacji z podwójnym życiem
Autorzy skoncentrowali się na białku zwanym eIF6, najlepiej znanym z udziału w składaniu rybosomów — fabryk białek komórki. Analizując próbki od pacjentów, modele mysi oraz kilka ludzkich linii komórkowych SCLC, odkryli, że poziom eIF6 konsekwentnie rośnie, gdy komórki przechodzą w oporny, nieneuroendokrynny stan. Co zaskakujące, wzrost ten występował równocześnie z ogólnym spadkiem produkcji białek w masie, co sugeruje, że eIF6 może pełnić role wykraczające poza podręcznikową funkcję. Szczegółowe analizy przyczepiania mRNA do rybosomów wykazały, że podstawowe elementy rybosomów niewiele się zmieniały. Zamiast tego przeorganizowano wybór i przetwarzanie komunikatów do translacji w miarę przełączania się tożsamości komórek.
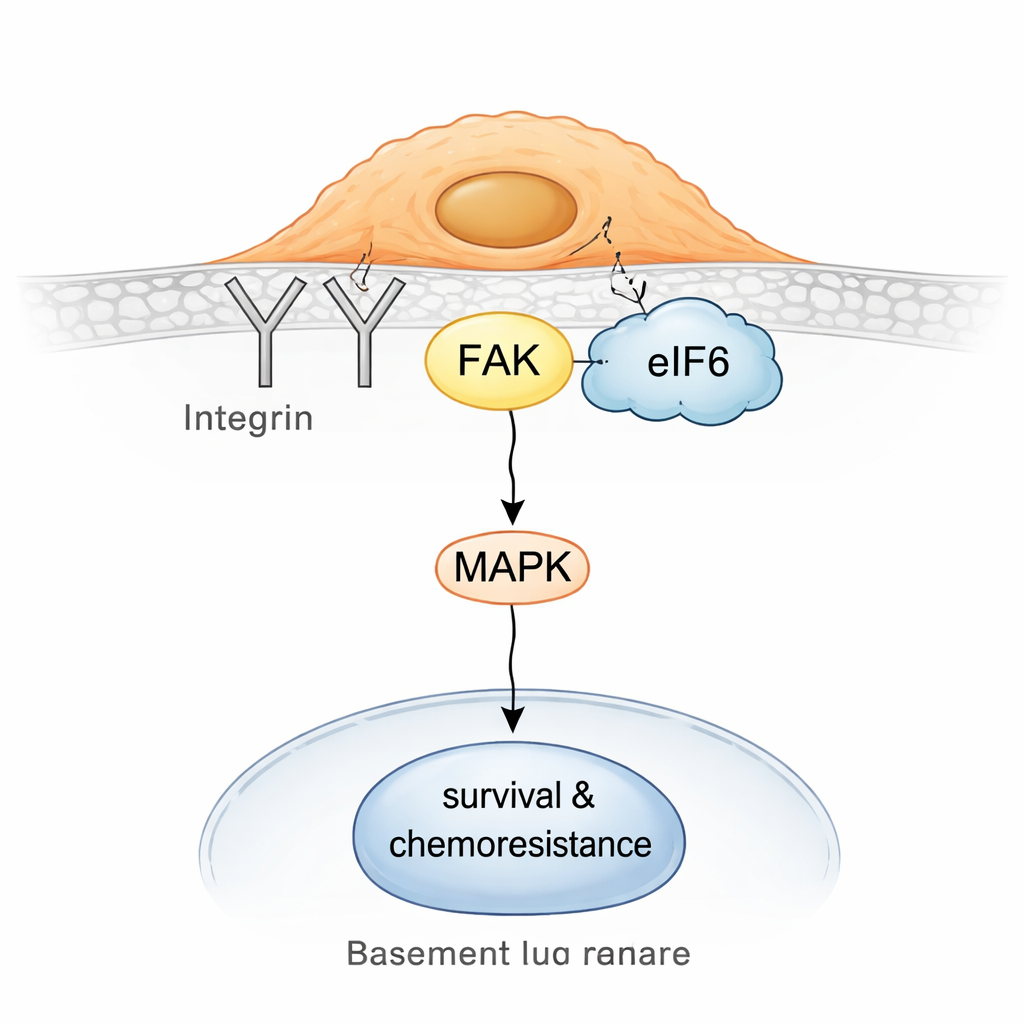
Oddzielenie się i wpięcie w sygnały przetrwania
Badając to głębiej, zespół odkrył, że w komórkach opornych eIF6 częściowo odłącza się od rybosomów i łączy z powierzchniowym centrum sygnalizacyjnym zbudowanym wokół integryn i białka zwanego kinazą ognisk adhezji (FAK). Integryny pomagają komórkom wyczuwać i przylegać do otoczenia; FAK przekazuje te sygnały do wnętrza komórki, często uruchamiając szlaki sprzyjające ruchowi, przeżyciu i tolerancji na leki. Biochemiczne wyłapywanie kompleksów oraz testy bliskości w komórkach pokazały, że eIF6 fizycznie wchodzi w interakcję z partnerem integryny CD104 i z FAK, a te kompleksy są bardziej liczne w komórkach nieneuroendokrynnych. To z kolei wzmacnia aktywność szlaku sygnałowego MAPK, znanego regulatora wzrostu i odporności na stres.
Uczynienie opornych guzów znów wrażliwymi
Naukowcy zapytali następnie, czy manipulacja eIF6 zmienia zachowanie SCLC. Gdy obniżono poziom eIF6 w komórkach opornych, geny związane z programem mobilnym i tworzeniem blizn (epitelialno–mezenchymalnym) zostały stłumione, podczas gdy klasyczne geny neuroendokrynne częściowo się przywróciły. Zmiany te nie cofnęły w pełni zegara, ale spowolniły przejście ku stanowi opornemu. Co istotne, komórki z mniejszą ilością eIF6 stały się bardziej wrażliwe na standardową chemioterapię karboplatyna–etopozyd w hodowli komórkowej i w guzach mysich, dając mniej przetrwałych kolonii i dłużej utrzymującą się redukcję guza. Ponieważ eIF6 nie ma obecnie specyficznych leków, zespół przetestował inhibitory FAK będące już w rozwoju klinicznym. Blokada sygnalizacji FAK ponownie uczuliła komórki oporne na chemioterapię, a w badaniach na myszach leczenie skojarzone dało najsilniejszą kontrolę guza.
Od laboratoryjnego odkrycia do przyszłych narzędzi dla pacjentów
Na koniec autorzy przeanalizowali próbki guzów od pacjentów z ograniczonym zaawansowaniem SCLC, którzy przeszli zabieg chirurgiczny. Przy użyciu czułej metody barwienia, która uwidacznia białka tylko wtedy, gdy znajdują się blisko siebie, zmierzyli, jak często eIF6 tworzy kompleksy z CD104 lub FAK w komórkach nowotworowych. Wysokie poziomy tych kompleksów — silniej niż sam eIF6 — wiązały się z wcześniejszym nawrotem i krótszym przeżyciem, co wskazuje na ich wartość jako obiecujących markerów prognostycznych. Podsumowując, praca ta ujawnia, że eIF6 może „pracować na boku” poza rybosomami, pomagając wpiąć komórki nowotworowe w silne obwody przetrwania. Mapując oś eIF6–integryna–FAK, badanie sugeruje sposoby identyfikacji pacjentów o wyższym ryzyku nawrotu oraz wspiera łączenie inhibitorów FAK z chemioterapią, aby przeciwdziałać niebezpiecznej plastyczności SCLC.
Cytowanie: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Słowa kluczowe: drobnokomórkowy rak płuca, oporność na leki, plastyczność komórek, eIF6, sygnalizacja integryny FAK