Clear Sky Science · pl
Hamowanie translacji zależne od kontekstu jako terapia przeciwnowotworowa
Obrócenie fabryk białek przeciwko rakowi
Komórki nowotworowe przetrwają dzięki ciągłemu wytwarzaniu dużych ilości krótkotrwałych „białek kierujących”, które utrzymują ich wzrost i podziały. W pracy tej analizuje się nową strategię walki z rakiem polegającą na subtelnym zablokowaniu maszyn wytwarzających białka — rybosomów — tylko wtedy, gdy próbują zbudować określone sekwencje białkowe, zwłaszcza te występujące w trudnoleczalnych onkogenach, takich jak MYC. Taka selektywna ingerencja mogłaby zabijać komórki nowotworowe, jednocześnie oszczędzając większość normalnej produkcji białek.
Jak komórki budują białka — i gdzie może dojść do błędów
Każda komórka polega na rybosomach, małych molekularnych fabrykach, które odczytują komunikaty genetyczne (mRNA) i łączą aminokwasy w białka. Większość istniejących leków celujących w rybosomy, takich jak antybiotyki lub starsze leki przeciwnowotworowe, działa jak tępe narzędzia: szeroko blokuje syntezę białek, co może uszkadzać zdrowe komórki i powodować poważne skutki uboczne. Autorzy wyszli z założenia, że ponieważ każdy nowo powstający łańcuch białkowy ma unikalną sekwencję i charakter chemiczny, możliwe może być zaprojektowanie małych cząsteczek, które blokują rybosom tylko wtedy, gdy w maszynie znajduje się konkretna sekwencja, pozostawiając resztę produkcji białek w komórce w dużej mierze nienaruszoną.
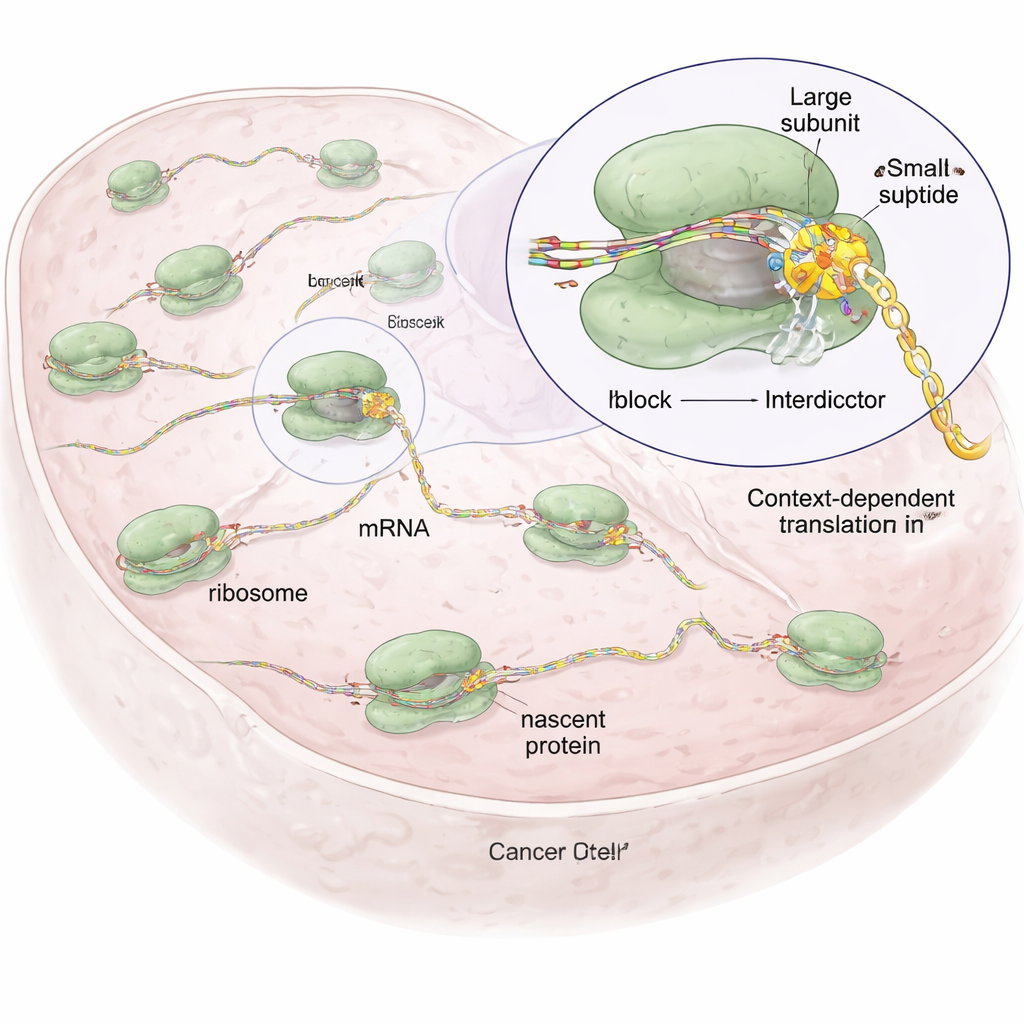
Zaprojektowane cząsteczki, które zatrzymują tylko wybrane sekwencje białek
W oparciu o naturalny związek o nazwie anizomycyna, który wiąże się z katalitycznym centrum rybosomu, gdzie powstają wiązania peptydowe, badacze stworzyli rodzinę syntetycznych molekuł, które nazywają „interdyktorami”. Wszystkie mają rdzeń kotwiczący je wewnątrz rybosomu, ale różnią się grupami bocznymi skierowanymi ku rosnącemu łańcuchowi peptydowemu. Grupy boczne są dostrojone do faworyzowania określonych typów aminokwasów — na przykład jeden interdyktor (IDB‑001) przyciąga reszty o ładunku ujemnym, podczas gdy inny (IDB‑002) preferuje małe, oleiste (hydrofobowe) reszty. Przy użyciu techniki zwanej profilowaniem rybosomów, która globalnie mapuje miejsca, w których rybosomy zatrzymują się na mRNA w komórkach, zespół wykazał, że każda z tych cząsteczek powoduje zatrzymania przy odrębnych krótkich motywach w nowo powstającym łańcuchu, często przy przedostatnim (−1) aminokwasie, co dowodzi działania zależnego od sekwencji, a nie bezwzględnego wyłączenia.
Obserwowanie spotkania leku z rybosomem atom po atomie
Aby zobaczyć, jak ta selektywność działa w szczegółach fizycznych, autorzy zamrożili ludzkie rybosomy w trakcie translacji zaprojektowanych sekwencji peptydowych i obrazowali je za pomocą krioelektronowej mikroskopii przy niemal atomowej rozdzielczości. Zaobserwowali interdyktor osadzony w miejscu aktywnym rybosomu, tworzący precyzyjne kontakty z kilkoma ostatnimi aminokwasami nowo powstającego łańcucha. W jednej strukturze hydrofobowa grupa boczna IDB‑002 jest otoczona przez małe, nieprzesadnie steryczne reszty w peptydzie, co wyjaśnia, dlaczego większe łańcuchy boczne są tam niekorzystne. W innej strukturze kwaśna grupa boczna reszty pochodzącej z MYC zwraca się, tworząc most solny z dodatnio naładowaną grupą na IDB‑001. Obecność leku powoduje również przesunięcie pobliskich zasad rRNA rybosomu w nowe pozycje, które zwężają miejsce aktywne i częściowo blokują wejście następnego tRNA, co pomaga zamrozić elongację przy wybranych sekwencjach.
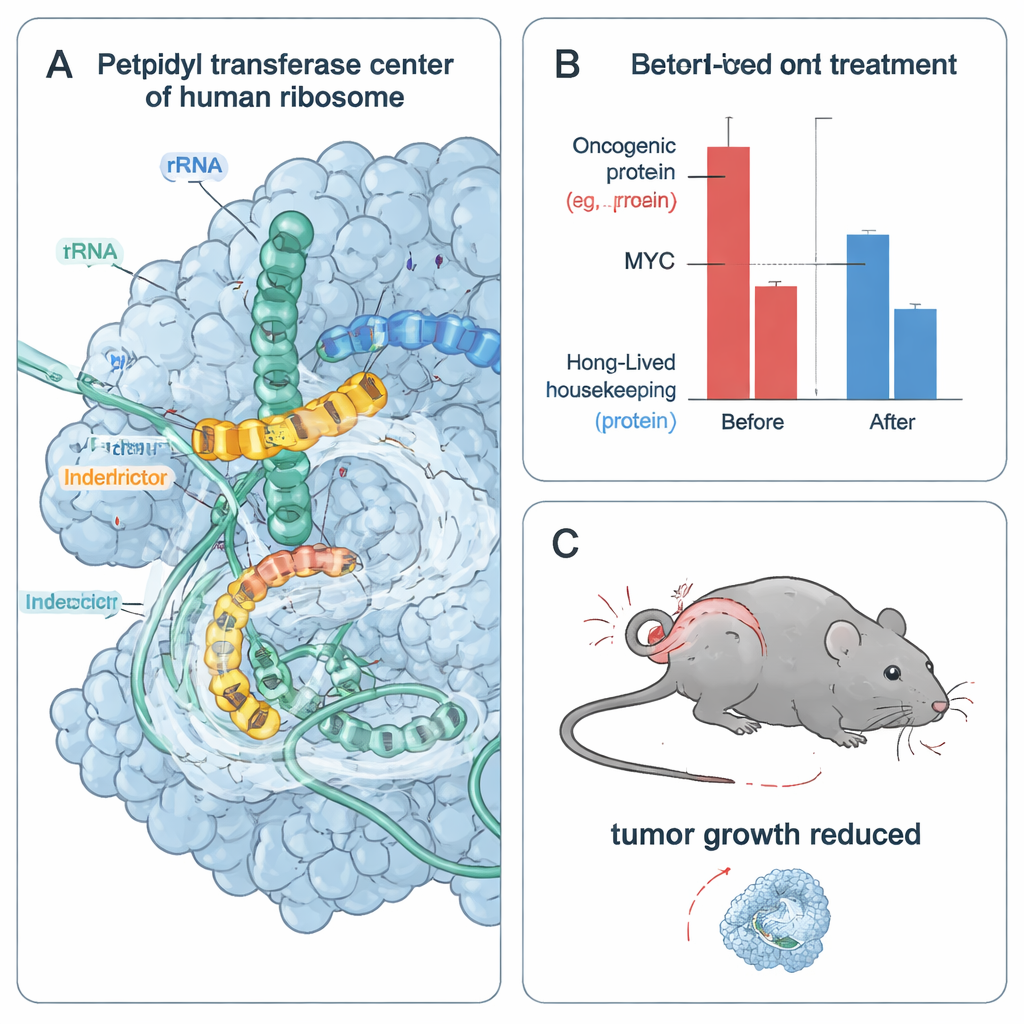
Od zatrzymanych rybosomów do zestresowanych i umierających komórek nowotworowych
Ponieważ szybko dzielące się komórki nowotworowe silnie polegają na krótkotrwałych onkoproteinach, takich jak MYC i CCND1, zespół przetestował wpływ interdyktorów na przeżywalność komórek nowotworowych. W wielu liniach komórkowych zależnych od MYC, IDB‑001 i IDB‑002 obniżały przeżywalność komórek przy stężeniach od nanomolowych do niskomikromolowych. Dalszy zoptymalizowany analog, IDB‑003, był jeszcze bardziej aktywny i nadający się do podawania doustnego. W komórkach te związki szybko wyczerpywały poziomy MYC i innych szybko obracających się onkoprotein, podczas gdy dłużej żyjące białka „porządkowe” pozostawały stosunkowo stabilne w tym samym przedziale czasowym. Leki te wywoływały również odpowiedzi stresowe komórki związane ze zderzającymi się rybosomami, ale blokada tych szlaków sygnałowych nie znosiła utraty przeżywalności, co sugeruje, że bezpośrednie pozbawienie istotnych onkogenicznych białek jest głównym czynnikiem prowadzącym do śmierci komórek nowotworowych.
Dowód koncepcji w trudnym modelu raka piersi
Aby sprawdzić, czy podejście działa u zwierząt, autorzy leczyli myszy z ludzkimi guzami raka piersi potrójnie ujemnego doustnie podawanym IDB‑003. Przez 28 dni guzy u leczonych zwierząt rosły znacznie wolniej niż u zwierząt kontrolnych, z zahamowaniem wzrostu guza do 80% przy wyższych dawkach i bez doniesień o ciężkiej toksyczności w tym badaniu. Analiza ekspresji genów guzów wykazała silne wyciszenie programów genów docelowych MYC, zgodne z obniżoną aktywnością MYC in vivo. Razem te wyniki wskazują, że selektywne zatrzymywanie rybosomów na określonych sekwencjach białek może osłabić guzy zależne od niestabilnych onkogenicznych czynników i jednocześnie potencjalnie unikać szerokiej toksyczności klasycznych blokerów translacji.
Dlaczego to ma znaczenie dla przyszłych terapii przeciwnowotworowych
Praca ta wprowadza nowy typ leku małocząsteczkowego: działający nie przez wiązanie gotowego białka, lecz przez przechwycenie go w trakcie powstawania i tylko wtedy, gdy obecny jest krótki „adresowy tag” sekwencyjny. Ponieważ wiele białek promujących nowotwór jest luźnych, krótkotrwałych lub pozbawionych oczywistych kieszeni dla konwencjonalnych leków, celowanie ich syntezy bezpośrednio przy rybosomie może otworzyć drogę do leczenia guzów napędzanych przez obecnie „nieleczalne” geny takie jak MYC. Badanie sugeruje także, że przez dostrojenie chemii interdyktorów, przyszłe leki mogłyby być zaprojektowane do celowania różnych motywów sekwencyjnych i wskazań chorobowych, rozszerzając tę strategię poza onkologię na inne stany, w których przycięcie specyficznych białek mogłoby przywrócić zdrowie.
Cytowanie: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Słowa kluczowe: terapia przeciwnowotworowa ukierunkowana na rybosomy, hamowanie translacji, guzy napędzane przez MYC, cząsteczki małocząsteczkowe zależne od kontekstu, rak piersi potrójnie ujemny