Clear Sky Science · pl
Identyfikacja sygnalizacji ephrin-A1–EphA2 jako potencjalnego celu zapobiegania złamaniom
Dlaczego warto chronić kruche kości
W miarę starzenia się organizmu kości mogą stawać się cienkie i łamliwe, przez co codzienne potknięcie o dywan może prowadzić do poważnego złamania. Złamania osteoporotyczne są nie tylko bolesne, ale też kosztowne dla systemów opieki zdrowotnej i mogą skracać lata zdrowego życia. Obecne leki pomagają, ale zwykle stosuje się je u osób z już rozpoznaną osteoporozą i mogą wiązać się z rzadkimi, lecz niepokojącymi działaniami niepożądanymi. W tym badaniu postawiono pytanie przyszłościowe: czy można wykorzystać genetykę i pomiary białek w dużych populacjach, aby odkryć zupełnie nowe sposoby wzmacniania kości i zapobiegania złamaniom, zanim one zajdą?
Polowanie na wskazówki o złamaniach we krwi
Badacze zaczęli od potraktowania krążących w organizmie białek jako wielkiej księgi wskazówek. Wiele leków działa poprzez celowanie w białka we krwi, więc znalezienie białek, które rzeczywiście wpływają na ryzyko złamań, mogłoby wskazać bezpośrednio nowe terapie. Korzystając z próbek z UK Biobank, przeanalizowali warianty genetyczne, które podwyższają lub obniżają poziomy 1 615 różnych białek krążących. Następnie powiązali te genetyczne „odciski białkowe” z danymi z ogromnego badania genetycznego obejmującego ponad 50 000 przypadków złamań przedramienia. Metoda statystyczna zwana Mendelowską randomizacją pomogła im zadać pytanie: gdy ludzie rodzą się z genami, które podnoszą lub obniżają poziom danego białka, czy ich całe życie ryzyko złamań zmienia się w sposób spójny?
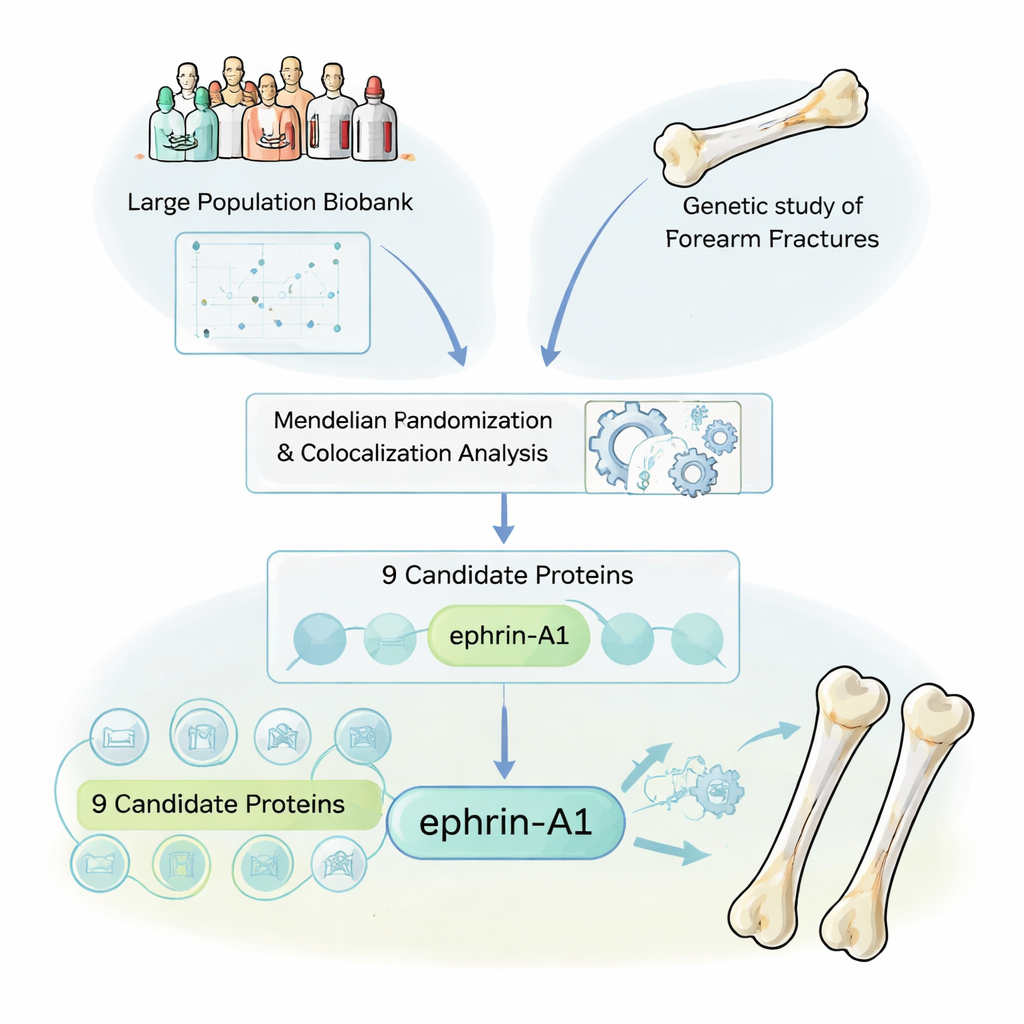
Oddzielanie prawdziwych sygnałów od genetycznego szumu
Ponieważ sąsiednie geny często występują razem, zespół zastosował drugi poziom analizy, zwany kolokalizacją, aby upewnić się, że obserwują prawdziwą przyczynowość, a nie mylące „sąsiedztwo” genetyczne. Spośród 1 615 białek dziewięć wyróżniło się jako przyczynowo związane ze złamaniami przedramienia. Co ważne, niektóre z nich były już znanymi aktorami w regulacji kości: sklerostyna i osteoprotegeryna, które są celem istniejących leków na osteoporozę, oraz inne białka długo powiązane z gęstością mineralną kości. Ich ponowne odkrycie stanowiło istotne potwierdzenie jakości, pokazując, że użyte podejście potrafi wiarygodnie odnajdywać sprawdzone cele lekowe, jednocześnie ujawniając nowe kandydatury.
Zaskakujący nowy ochroniarz: ephrin-A1
Wśród nowo wyróżnionych białek szczególną uwagę przyciągnęła ephrin‑A1. Osoby genetycznie predysponowane do wyższych poziomów ephrin‑A1 we krwi miały gęstsze kości i rzadsze złamania przedramienia. Ephrin‑A1 zwykle jest związana z powierzchnią komórek i może być odcinana do krążenia. Wiąże się z receptorem o nazwie EphA2, który zespół stwierdził, że jest silnie eksprymowany na komórkach tworzących kość, zwanych osteoblastami. Badając tkanki ludzkie i mysie za pomocą sekwencjonowania pojedynczych komórek, obrazowania RNA in situ i zaawansowanej trójwymiarowej techniki „DeepBone” clearing, zaobserwowali spójny wzorzec: ephrin‑A1 znajduje się na komórkach wyściełających naczynia krwionośne w obrębie kości, podczas gdy EphA2 leży na osteoblastach wzdłuż powierzchni kości, często zaledwie kilka średnic komórkowych dalej. Takie rozmieszczenie sprawia, że bezpośrednia komunikacja komórka‑do‑komórki między komórkami naczyniowymi a komórkami tworzącymi kość jest nie tylko możliwa, lecz i prawdopodobna.
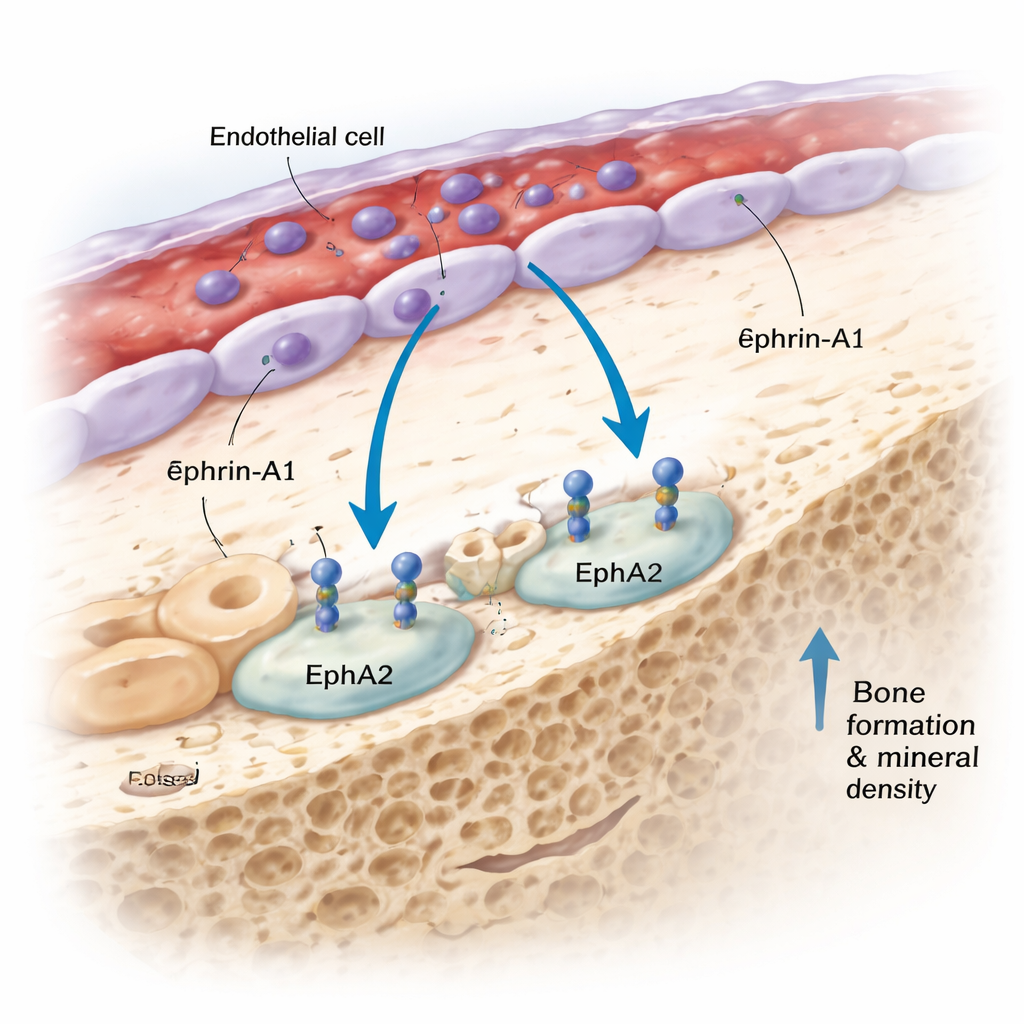
Testowanie sygnału w żywych kościach
Aby sprawdzić, czy rozmowa ephrin‑A1–EphA2 rzeczywiście ma znaczenie dla wytrzymałości kości, badacze sięgnęli po genetykę myszy. Myszy zmodyfikowane tak, by brakowało im albo ephrin‑A1, albo jej receptora EphA2, miały istotnie niższą całkowitą gęstość mineralną kości ciała w porównaniu do normalnych rodzeństwa, i to w obu płciach. Zespół zbadał następnie, jak ta para sygnalizacyjna zachowuje się w różnych modelach mysich, które naśladują ludzką utratę i przyrost tkanki kostnej. Zapalenie, starzenie i wysokie dawki witaminy A — każde z nich znane ze swego działania osłabiającego kość — wiązały się ze zmniejszoną ekspresją ephrin‑A1 i/lub EphA2 w tkance kostnej. Dla porównania, obciążenie mechaniczne, które naśladuje korzystny efekt ćwiczeń obciążających, zwiększało ekspresję ephrin‑A1. Co warte podkreślenia, te zmiany nie pokrywały się z tymi obserwowanymi przy obecnych lekach na osteoporozę, co sugeruje, że ephrin‑A1–EphA2 może działać inną drogą, która mogłaby uzupełniać istniejące terapie.
Co to oznacza dla przyszłego zapobiegania złamaniom
Podsumowując, badanie pokazuje, że wyrafinowane podejście łączące genetykę i pomiary białek potrafi ponownie odkryć znane cele lekowe w kontekście kości oraz ujawnić nowe. Wskazuje na interakcję ephrin‑A1 z EphA2 na osteoblastach jako kluczowy sygnał pomagający utrzymać kości gęste i odporne. Dla czytelnika nieznającego szczegółów najważniejszy wniosek jest taki: nasza krew i geny zawierają szczegółowe plany dotyczące utrzymania siły kości — a ephrin‑A1 jest teraz obiecującym nowym przełącznikiem w tym planie. Jeśli przyszłe badania pokażą, że można bezpiecznie wzmocnić ten sygnał, na przykład za pomocą leków wzmacniających sygnalizację ephrin‑A1–EphA2, może to dać nową, potencjalnie bezpieczniejszą metodę zapobiegania złamaniom, szczególnie u wielu osób, które dziś pozostają bez leczenia.
Cytowanie: Movérare-Skrtic, S., Nethander, M., Li, L. et al. Identification of ephrin-A1–EphA2 signalling as a potential target for fracture prevention. Nat Commun 17, 1988 (2026). https://doi.org/10.1038/s41467-026-69863-6
Słowa kluczowe: osteoporoza, gęstość mineralna kości, zapobieganie złamaniom, ephrin-A1 EphA2, Mendelowska randomizacja