Clear Sky Science · pl
In situ inżynieria TRIM13 zwiększa przeciwzapalne właściwości CAR‑makrofagów w terapii zwłóknienia wątroby
Przeprogramowanie wątrobowego zespołu sprzątającego
Zwłóknienie wątroby, proces bliznowacenia prowadzący do marskości i niewydolności wątroby, dotyka miliony osób i obecnie ma niewiele skutecznych terapii. W tym badaniu zbadano sposób wykorzystania i przeprogramowania własnych komórek odpornościowych wątroby, by nie tylko usuwały komórki tworzące blizny, lecz także tłumiły szkodliwe zapalenie — co może dać bezpieczniejszą i skuteczniejszą terapię chorób przewlekłych wątroby.
Dlaczego bliznowacenie jest tak trudne do zatrzymania
Kiedy wątroba jest wielokrotnie uszkadzana — przez wirusy, alkohol lub choroby metaboliczne — próbuje się zregenerować, odkładając tkankę bliznowatą. Specjalne komórki zwane komórkami gwiaździstymi wątroby przechodzą w stan „aktywowany” i wydzielają wytrzymałe włókna, niczym budowlańcy wylewający beton. Z czasem to bliznowacenie, zwane włóknieniem, deformuje narząd i upośledza jego funkcję. W centrum tego procesu znajdują się komórki odpornościowe — makrofagi. W uszkodzonej wątrobie mogą one działać jak miecz obosieczny: w jednym trybie napędzają zapalenie i aktywują komórki gwiaździste, a w innym — sprzyjającym naprawie — pomagają rozkładać tkankę bliznowatą i przywracać równowagę.
Przekształcanie szkodliwych sygnałów w pomocne
Naukowcy skupili się na kluczowym sygnale zagrożenia w uszkodzonej wątrobie: mitochondrialnym DNA wyciekającym z uszkodzonych komórek. Makrofagi wykrywają to DNA przez ścieżkę zwaną cGAS‑STING, która popycha je w kierunku stanu prozapalnego i sprzyjającego bliznowaceniu. Białko o nazwie TRIM13 zwykle pomaga tłumić STING, oznaczając je do zniszczenia. Zespół założył, że zwiększenie poziomu TRIM13 w makrofagach wątroby mogłoby przywrócić je do stanu łagodzącego i naprawczego. Równocześnie chcieli, aby te komórki bezpośrednio polowały na i usuwały aktywowane komórki gwiaździste. W tym celu wykorzystali koncepcję chimerowego receptora antygenowego (CAR) zapożyczoną z immunoterapii nowotworów: syntetyczny receptor pozwalający komórkom odpornościowym rozpoznawać wybrany cel — w tym przypadku białko FAP, obficie obecne na aktywowanych komórkach gwiaździstych.
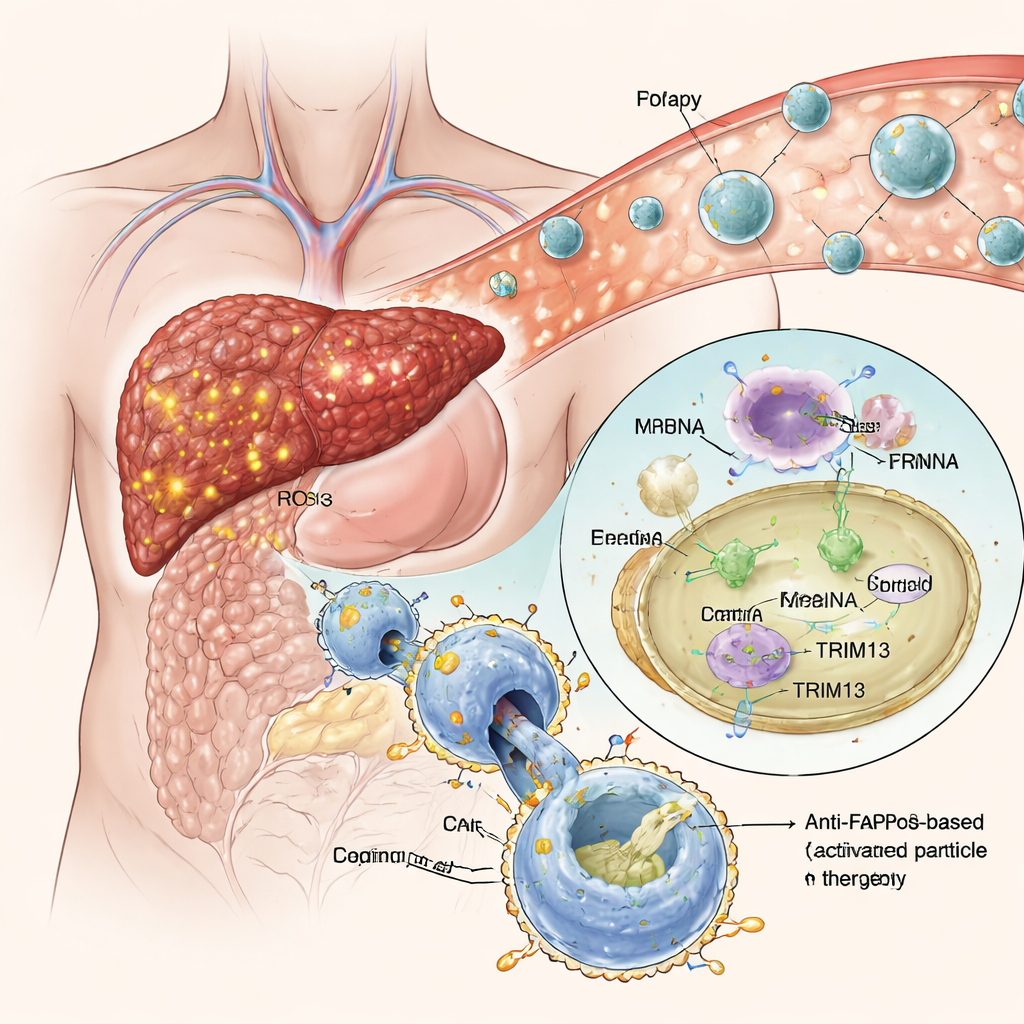
Inteligentne nanocząstki kierujące się do chorej tkanki
Zamiast modyfikować makrofagi poza organizmem, zespół zbudował „iskrzące eferocytozę” lipidowe nanocząstki — maleńkie kuleczki lipidowe niosące instrukcje genetyczne w postaci mRNA. Cząstki te są pokryte zamaskowaną formą fosfatydyloseryny, naturalnego sygnału „zjedz mnie”, który wykazują umierające komórki, aby przyciągnąć makrofagi. W środowisku o wysokim utlenieniu, charakterystycznym dla zwłókniałej wątroby, maskowanie jest usuwane i sygnał zostaje ujawniony, skłaniając pobliskie makrofagi do pochłonięcia nanocząstek. Po wnętrzu komórki mRNA jest uwalniane i odczytywane, co prowadzi do produkcji zarówno TRIM13, jak i przeciw‑FAP CAR. W hodowlach komórkowych podejście to skutecznie skierowało makrofagi w stronę stanu przeciwzapalnego, jednocześnie nadając im silne i selektywne upodobanie do komórek bliznowatych pozytywnych dla FAP, bez zaburzania ich normalnej zdolności do usuwania innego materiału.
Z chorych do regenerujących się wątrób u myszy
Zespół przetestował następnie strategię w modelach mysich zwłóknienia wątroby wywołanego toksycznym związkiem lub dietą ubogą w składniki odżywcze i sprzyjającą stłuszczeniu. Systemowo wstrzyknięte nanocząstki efektywnie docierały do wątroby i, szczególnie u zwierząt z włóknieniem, były głównie pochłaniane przez makrofagi. Tam zmodyfikowane komórki wykazywały obniżoną aktywność ścieżki STING i niższą produkcję mediatorów zapalnych, wraz ze zwiększoną zdolnością do zabijania aktywowanych komórek gwiaździstych. Analizy tkankowe wykazały wyraźne spadki kolagenu i innych markerów blizny, drobniejszą i bardziej normalną strukturę macierzy zewnątrzkomórkowej oraz poprawę badań krwi obrazujących funkcję wątroby. Wątroby leczonych myszy miały więcej proliferujących komórek i odzyskały zdrowszą architekturę, co sugeruje prawdziwą naprawę narządu, a nie tylko chwilowe stłumienie zapalenia.
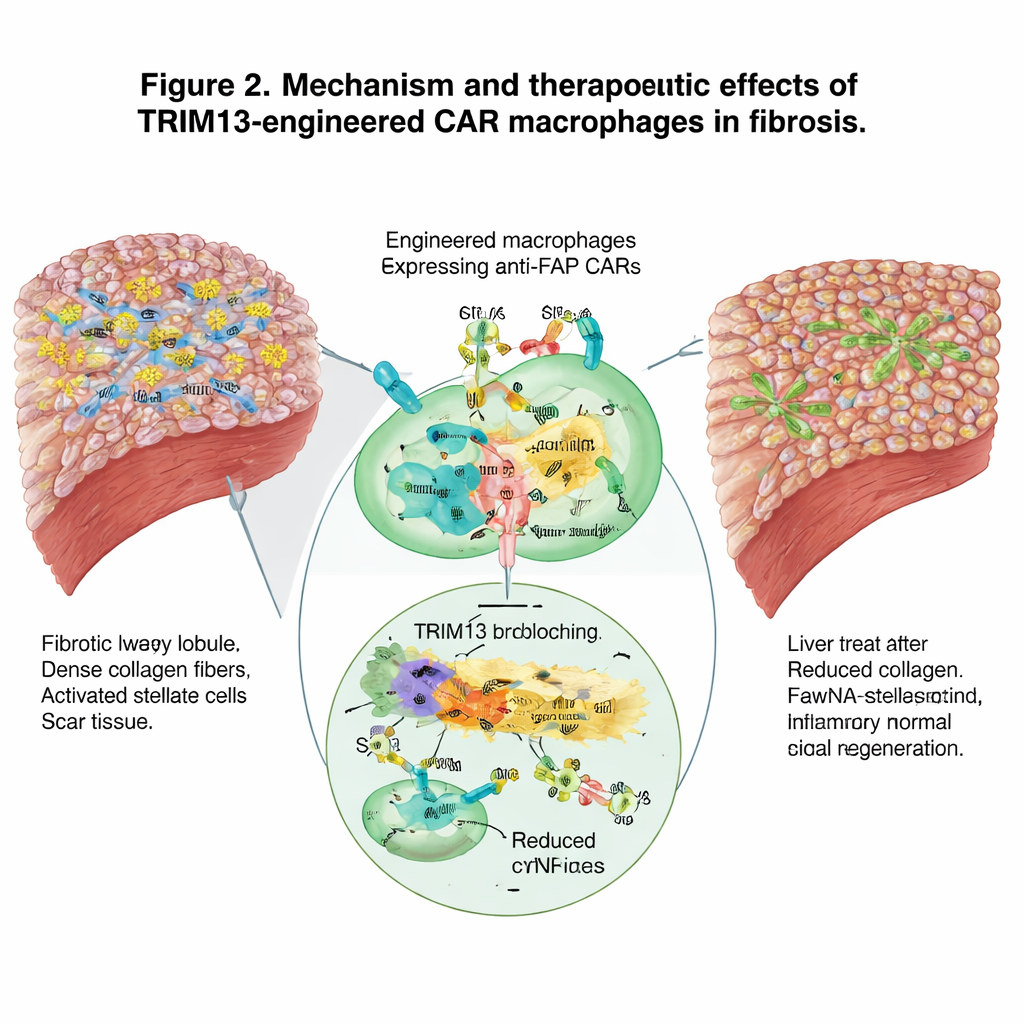
Włączenie szerszego układu odpornościowego
Poza bezpośrednim usuwaniem blizn, zmodyfikowane makrofagi przekształciły szerszy pejzaż immunologiczny. Przesunęły się z agresywnego, promującego uszkodzenie profilu w stronę bardziej rozstrzygającego i naprawczego, zmniejszając sygnały zapalne we krwi. Jednocześnie, poprzez pożeranie komórek tworzących blizny, zdawały się pełnić rolę nauczycieli dla układu odpornościowego adaptacyjnego, przyciągając neutrofile, komórki dendrytyczne i limfocyty T oraz zachęcając do skoordynowanej odpowiedzi przeciw tkance włóknistej. Sekwencjonowanie RNA pojedynczych komórek populacji immunologicznych wątroby potwierdziło odejście od programów genów prozapalnych i przesunięcie w stronę zwiększonej zdolności pochłaniania i usuwania szkodliwych komórek oraz szczątków.
Co to może znaczyć dla pacjentów
Dla czytelnika niebędącego specjalistą wniosek jest taki, że praca ta wskazuje sposób „przeedukowania” wątrobowych komórek sprzątających, aby jednocześnie rozmontowywały tkankę bliznowatą i wyłączały przewlekłe sygnały alarmowe podtrzymujące uszkodzenie. Dzięki wykorzystaniu krótkotrwałych instrukcji mRNA zapakowanych w inteligentne nanocząstki terapia unika trwałej modyfikacji komórek i ogranicza aktywność do chorych obszarów, co może zmniejszyć działania niepożądane. Choć potrzebne są dalsze badania zanim metoda trafi do zastosowań u ludzi, strategia ta stanowi obiecujący plan leczenia zwłóknienia wątroby — i potencjalnie innych chorób włóknieniowych — przez przekształcenie własnego układu odpornościowego organizmu z czynnika napędzającego bliznowacenie w aktywnego partnera naprawy.
Cytowanie: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
Słowa kluczowe: zwłóknienie wątroby, terapia makrofagowa, dostawa mRNA za pomocą nanocząstek, chimerowy receptor antygenowy, ścieżka TRIM13 STING