Clear Sky Science · pl
Radiomarkowanie oligopeptydów przez selektywną wymianę izotopów wodoru na deuter i tryt w buforach wodnych
Śledzenie leków na poziomie atomowym
Współczesne leki coraz częściej obejmują złożone cząsteczki biologiczne, takie jak peptydy i małe białka. Aby zrozumieć, gdzie te leki trafiają w organizmie i jak długo tam pozostają, naukowcy często zastępują kilka zwykłych atomów rzadkimi lub promieniotwórczymi izotopami, które można wykrywać. Artykuł przedstawia sposób „oznaczania” leków peptydowych takimi śledzącymi atomami bezpośrednio w roztworach wodnych, bliżej rzeczywistych warunków biologicznych niż większość wcześniejszych metod.
Dlaczego drobne atomowe zamiany mają znaczenie
Podmiana zwykłego wodoru na cięższe izotopy, takie jak deuter czy tryt, przekształca codzienne cząsteczki w potężne narzędzia badawcze. Znakowane wersje zachowują się niemal identycznie jak oryginalny lek, ale można je śledzić za pomocą czułych przyrządów wykrywających masę lub promieniowanie. Dla małych cząsteczek leczniczych chemicy dysponują dużym zestawem metod do wytwarzania takich znakowanych związków. Natomiast metody oznaczania większych, delikatnych biologików — jak peptydy i białka — są rzadkie, często skomplikowane i słabo przystosowane do środowisk wodnych przypominających krew czy płyny komórkowe. Autorzy postawili sobie za cel wypełnić tę lukę: prosty, selektywny sposób wprowadzenia deuteru lub trytu do elementów budulcowych peptydów bezpośrednio w buforach wodnych.
Strategia jednego naczynia w wodzie
Zespół skupił się na reakcji zwanej wymianą izotopów wodoru, w której atom wodoru na cząsteczce zostaje zamieniony na jego cięższego kuzyna z gazu, takiego jak deuter (D2) czy tryt (T2). Opracowali katalizator tworzony in situ, oparty na metalicznym irydzie i specjalnie dobranym pomocniczym fosfinowym ligandzie. Po zmieszaniu w łagodnie zasadowym buforze i podgrzaniu system aktywuje specyficzne wiązania węgiel–wodór w aminokwasach i krótkich peptydach i zastępuje te wodory deuterem lub trytem pochodzącym z gazu. Co kluczowe, odbywa się to w jednym etapie, w środowisku bogatym w wodę i przy bardzo niskich ilościach metalu — warunki przyjaźniejsze dla delikatnych leków peptydowych i praktycznych procedur laboratoryjnych. 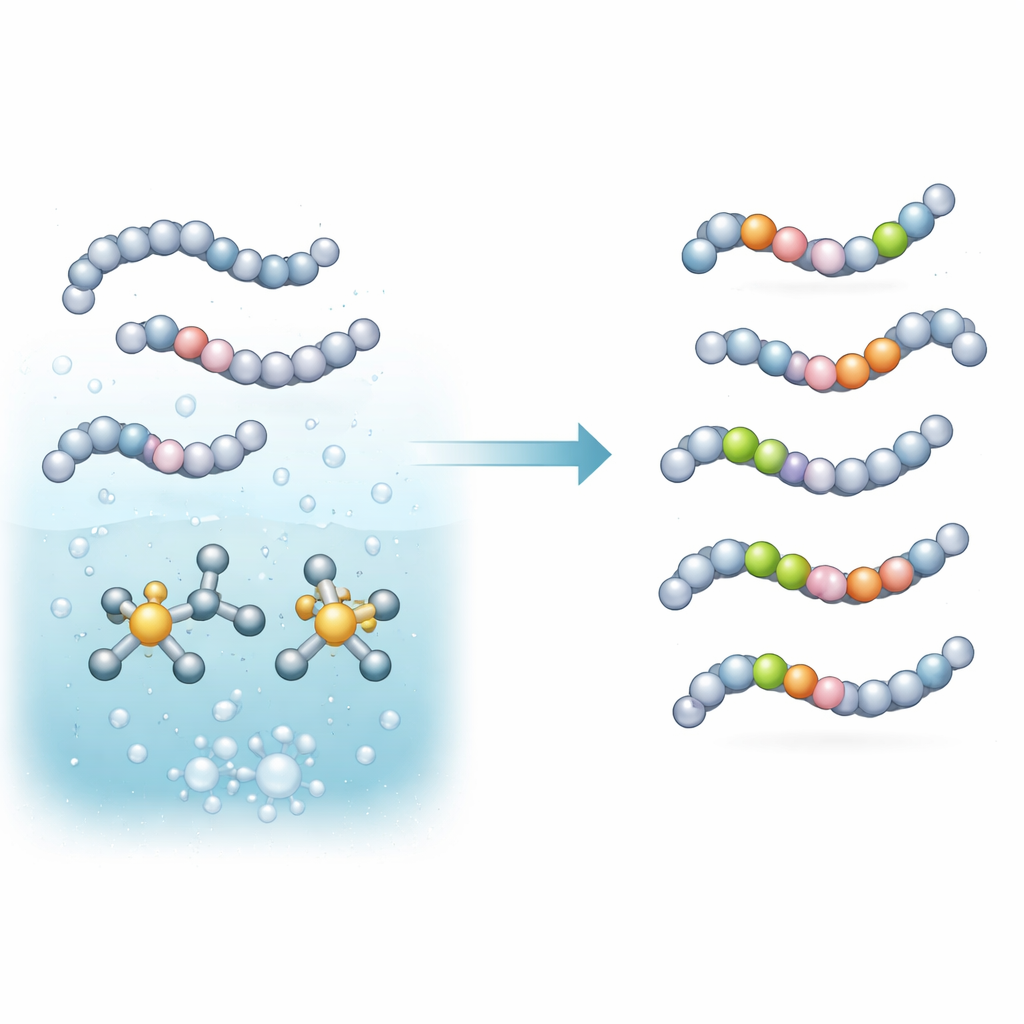
Wybór odpowiednich miejsc na peptydach
Nie każdy atom wodoru w peptydzie jest równie użyteczny jako znacznik. Niektóre łatwo ulegają utracie podczas metabolizmu, co spowodowałoby zanik radioaktywnego znacznika. Autorzy dokładnie zbadali, gdzie ich katalizator ma preferencję działania. Odkryli, że szczególnie dobrze nadają się niechronione aminokwasy, takie jak lizyna i arginina. W przypadku lizyny metoda selektywnie oznacza atom węgla w łańcuchu bocznym (tzw. pozycja gamma), miejsce uznawane za „nieaktywowane” i bardziej stabilne w organizmie. Arginina wykazuje podobne zachowanie w pobliskich pozycjach łańcucha bocznego. Testując serię pokrewnych cząsteczek, w tym krótkich łańcuchów z dwoma grupami aminowymi, zespół ustalił, że obecność dwóch atomów azotu ustawionych we właściwy sposób pomaga katalizatorowi metalicznemu zacisnąć się na cząsteczce i dotrzeć do docelowego wiązania węgiel–wodór.
Zajrzeć pod maskę katalizatora
Aby zrozumieć, skąd bierze się ta selektywność, badacze połączyli eksperymenty z szczegółowymi symulacjami komputerowymi opartymi na teorii funkcjonału gęstości. Obliczenia mapują krajobraz energetyczny podczas tworzenia kompleksu irydowego z dimerowego prekursora, wiązania z wodą, następnie z aminokwasem, aż po insertację w konkretne wiązanie węgiel–wodór. Modele pokazują, że rozbicie pierwotnego dimeru irydu jest energetycznie wykonalne w wodzie dla jednego typu prekursora, ale nie dla blisko spokrewnionego — co wyjaśnia, dlaczego tylko niektóre kompleksy wyjściowe są skuteczne. Wykazują również, że sam substrat stabilizuje aktywne centrum metalu i zapobiega jego aglomeracji w nieaktywne cząstki. Najbardziej korzystna ścieżka obejmuje wiązanie aminokwasu przez dwa atomy azotu, tworząc „szczypcowy” chwyt, który ustawia pojedyncze wiązanie węgiel–wodór do wymiany z deuterem lub trytem.
Od prostych cegiełek do prawdziwych leków peptydowych
Z mechanizmem wyjaśnionym, zespół rozszerzył metodę z pojedynczych aminokwasów na krótkie peptydy zawierające do siedmiu reszt, a następnie na bardziej złożone sekwencje przypominające terapie, sięgające nawet 13 aminokwasów. We wszystkich przypadkach znakowanie następowało na łańcuchach bocznych lizyny lub argininy znajdujących się na końcu peptydu, a peptydy pozostawały w dużej mierze nietknięte pod warunkami reakcji. Dla trytu zoptymalizowano reakcję przy niskich ciśnieniach gazu, aby bezpiecznie osiągnąć wysokie aktywności właściwe — czyli duży odsetek cząsteczek nosił co najmniej jeden atom trytu. Te trytowane peptydy uzyskano w jednym naczyniu i są gotowe do użycia jako znaczniki w badaniach in vitro, a potencjalnie także in vivo. 
Co to oznacza dla przyszłych leków
Praca pokazuje, że możliwe jest selektywne dołączenie deuteru lub trytu do realistycznych leków peptydowych w prostym, wodnym etapie, jednocześnie celując w pozycje na kluczowych aminokwasach odporne na metabolizm. Dla deweloperów leków oznacza to łatwiejszy dostęp do precyzyjnie znakowanych wersji śledzących terapii peptydowych, niezbędnych do pomiaru wchłaniania, dystrybucji i metabolizmu. Poza produkcją znaczników, wgląd w mechanikę oddziaływań katalizatora irydowego z aminokwasami może zainspirować nowe sposoby dostrajania miejsc i sposobu modyfikacji złożonych biomolekuł, otwierając drogę do większej kontroli chemicznej nad przyszłymi lekami biologicznymi.
Cytowanie: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
Słowa kluczowe: peptydy znakowane radioaktywnie, wymiana izotopów wodoru, znakowanie deuterem i trytem, leki peptydowe, kataliza irydowa