Clear Sky Science · pl
Cholecystokinina pochodząca z komórek beta napędza rozwój raka trzustki związanego z otyłością
Kiedy nadmiar wagi rozmawia z trzustką
Otyłość jest znana z podnoszenia ryzyka raka trzustki, jednego z najgroźniejszych nowotworów, ale biologiczna „rozmowa”, która łączy nadmiar tkanki tłuszczowej z powstawaniem guzów, pozostawała niejasna. To badanie odkrywa nieoczekiwanego posłańca: hormon trawienny zwany cholecystokininą (CCK), produkowany wewnątrz komórek wytwarzających insulinę w trzustce. Śledząc, jak te komórki zmieniają się pod wpływem stresu metabolicznego, autorzy pokazują, w jaki sposób hormon mający pomagać organizmowi może zamiast tego napędzać rozwój nowotworu i sugerują nowe sposoby przechwycenia choroby, zanim się zadomowi.
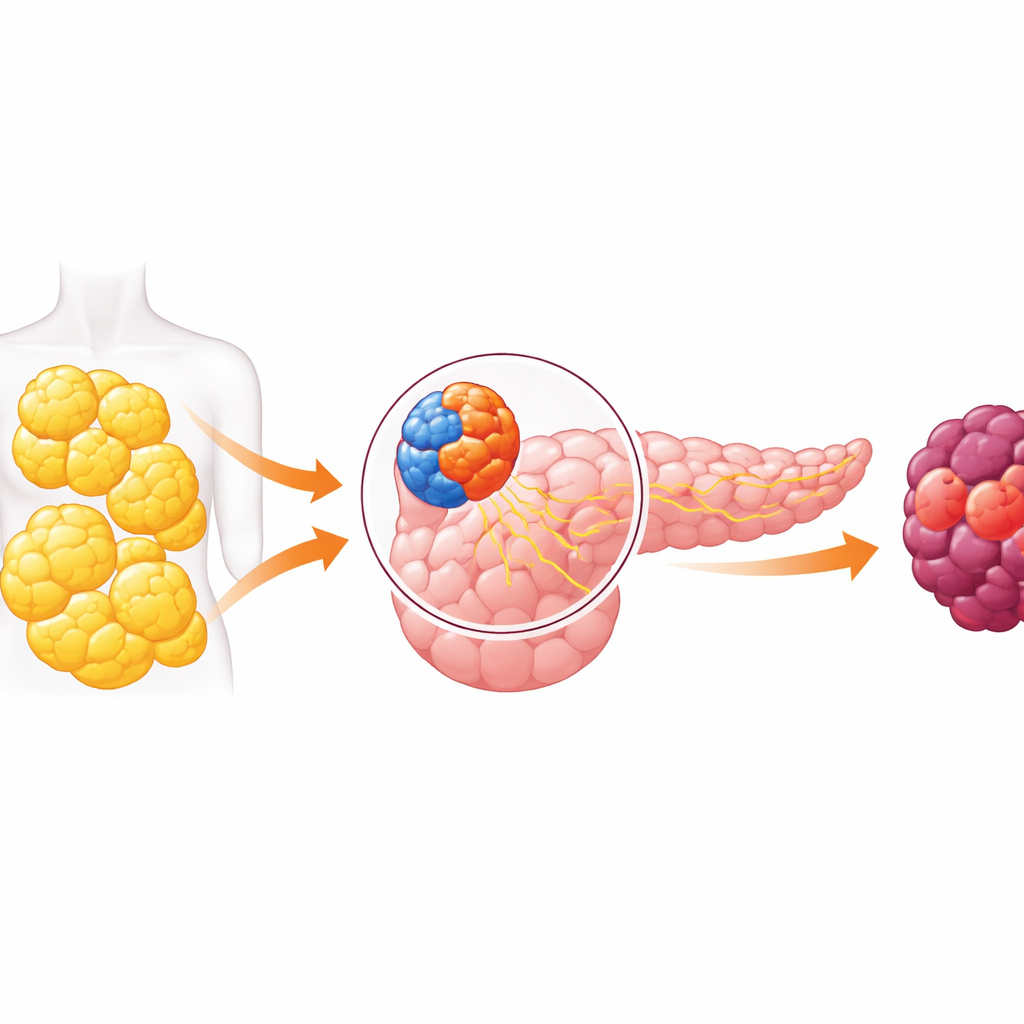
Organ o dwóch twarzach i niebezpieczny dialog
Trzustka pełni dwie główne funkcje. Jedna część, endokrynna, zawiera małe wysepki komórek wydzielających hormony, jak insulina, kontrolujące poziom cukru we krwi. Druga, egzokrynna, produkuje soki trawienne i obejmuje komórki, które najczęściej dają początek rakowi trzustki. Przez lata badacze zakładali, że te dwie komory działają w dużej mierze niezależnie. Nowsze prace obaliły ten pogląd, pokazując, że sygnały z komórek produkujących hormony mogą wpływać na pobliskie komórki trawienne. Artykuł zgłębia tę komunikację i wykazuje, że w otyłości może ona popychać część egzokrynną trzustki w kierunku raka.
Stres w komórkach hormonalnych wywołuje nowy sygnał
W otyłości komórki beta produkujące insulinę są pod stałą presją, by sprostać rosnącemu zapotrzebowaniu na insulinę. Wykorzystując sekwencjonowanie RNA pojedynczych komórek i zaawansowane narzędzia obliczeniowe, badacze śledzili pojedyncze komórki beta, gdy myszy przechodziły od szczupłości przez nadwagę do ciężkiej otyłości. Odkryli, że podzbiór niedojrzałych komórek beta się powiększył i stopniowo utracił swoją wyspecjalizowaną tożsamość insulinową. W miarę jak te komórki ulegały stresowi, wzrosły markery obciążenia związane ze składaniem białek i uszkodzeniem komórkowym, a produkcja insuliny spadła. Jednocześnie komórki te zaczęły wytwarzać wysoki poziom CCK, hormonu zwykle kojarzonego z jelitami, który może pobudzać komórki trawienne do wzrostu i przemian.
Z użytecznego hormonu w paliwo dla raka
Aby sprawdzić, czy nowo produkowana CCK jest tylko produktem ubocznym stresu, czy aktywnym czynnikiem choroby, zespół wygenerował myszy, których komórki beta produkowały dodatkową CCK, nawet bez otyłości. Zwierzęta te rozwinęły zmiany przednowotworowe trzustki i inwazyjne guzy w stopniu podobnym do myszy otyłych, mimo normalnej masy ciała i poziomu cukru we krwi. Przeciwnie, gdy CCK została usunięta specyficznie z trzustki myszy otyłych, obciążenie nowotworowe spadło wyraźnie, mimo że zwierzęta pozostały ciężkie i miały wysokie poziomy insuliny. W wielu modelach mysich poziomy CCK w trzustce ściśle korelowały z ilością guza, podczas gdy poziomy insuliny miały tendencję do przesuwania się w przeciwnym kierunku. To wskazywało, że w tych systemach to CCK — a nie insulina — jest dominującym hormonem łączącym otyłość z rakiem trzustki.
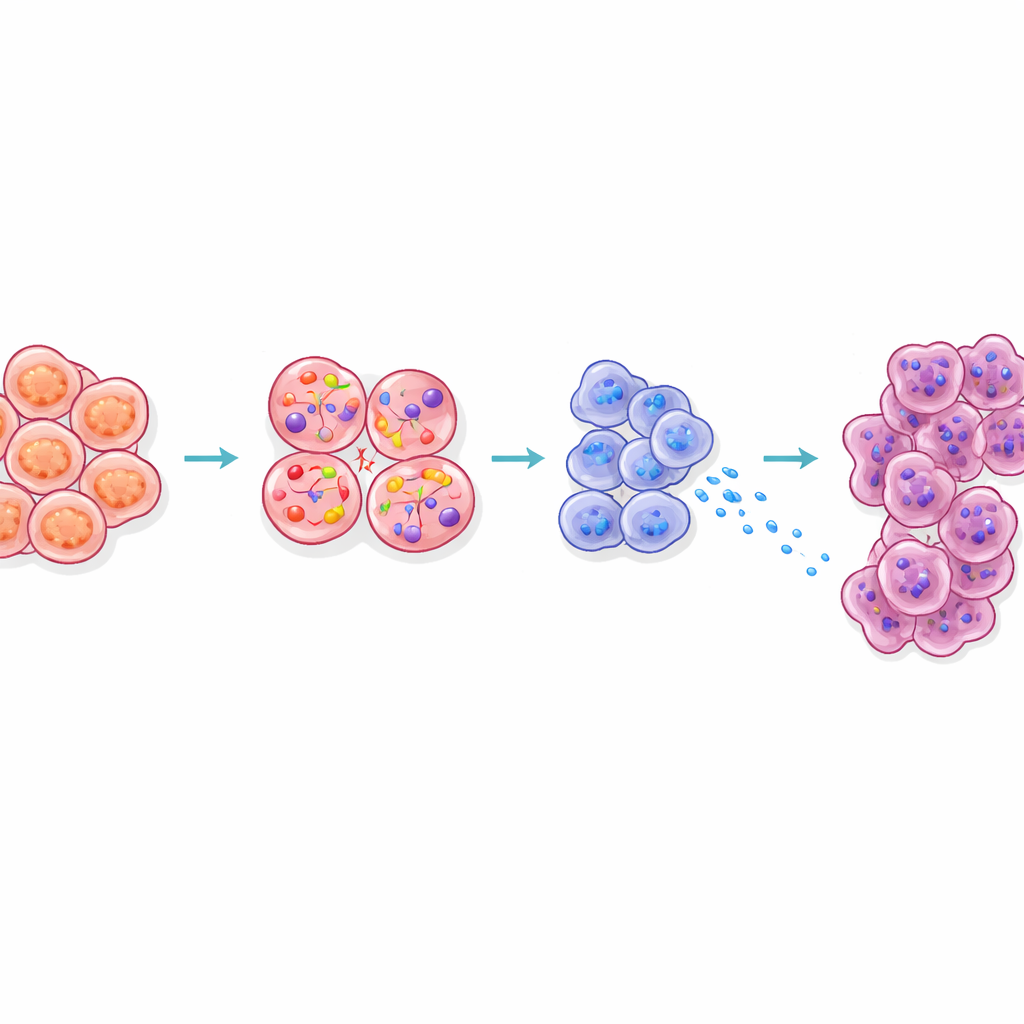
Jak sygnał dociera i przygotowuje sąsiednie komórki
Badanie przeanalizowało też, jak CCK z komórek beta przekształca otaczającą tkankę. Komórki acinarne, które normalnie wydzielają enzymy trawienne, leżą tuż obok wysepek w trzustce. U myszy otyłych komórki acinarne znajdujące się w pobliżu wysepek wykazywały sygnaturę stresu, produkowały więcej enzymów trawiennych i białek zwanych Reg oraz przechodziły w stany znane z większej podatności na przemianę nowotworową. Zablokowanie sygnalizacji CCK u myszy otyłych zmniejszyło te sygnały Reg. Obrazowanie trójwymiarowe ujawniło ponadto, że wczesne zmiany przednowotworowe miały tendencję do powstawania nietypowo blisko wysepek u zwierząt otyłych. Razem wyniki te sugerują, że dyfuzja CCK z zestresowanych komórek beta tworzy „gorącą strefę” wokół wysepek, gdzie komórki trawienne są przygotowane do przekształcenia się w guzy.
Wspólne wzorce z ludzką cukrzycą i kluczowy przełącznik
Porównując dane mysie z ludzką tkanką trzustki od osób z cukrzycą typu 2 i bez niej, autorzy odnaleźli uderzające paralelizmy: komórki beta od dawców z cukrzycą odwzorowywały te same zestresowane, mniej dojrzałe stany widziane u otyłych myszy. Następnie przeprowadzili analizę regulatorową, by ustalić, co uruchamia CCK w komórkach beta, i zidentyfikowali odpowiedź na stres skupioną wokół białka cJun. Gdy zablokowali szlak JNK–cJun u myszy otyłych lub w komórkopodobnych beta hodowanych na szalce, poziomy CCK spadły, a cJun zaobserwowano wiążącego się w pobliżu regionu regulatorowego genu CCK. Sugeruje to, że przewlekły stres aktywuje JNK–cJun, co z kolei przełącza komórki beta w tryb produkcji CCK.
Co to oznacza dla osób zagrożonych chorobą
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie: pod obciążeniem otyłości i cukrzycy komórki produkujące insulinę w trzustce nie tylko zawodzą — dostosowują się w sposób, który niezamierzenie sprzyja pobliskim komórkom w tworzeniu raka. Robią to, włączając CCK, hormon działający jak sygnał wzrostu i stresu dla sąsiednich komórek trawiennych, co pomaga stworzyć żyzną pożywkę dla guzów. Ponieważ CCK pochodząca z trzustki nie jest niezbędna do utrzymania kontroli glikemii, ukierunkowanie tego źródła hormonu lub jego stresowo aktywowanego przełącznika mogłoby w praktyce zmniejszyć ryzyko raka trzustki u osób z otyłością lub cukrzycą typu 2, nie naruszając równowagi hormonalnej. Praca ta przedefiniowuje raka trzustki jako chorobę wynikającą z błędnej komunikacji między dwiema stronami narządu i wskazuje nowe drogi wczesnej prewencji.
Cytowanie: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Słowa kluczowe: rak trzustki, otyłość, komórki beta, cholecystokinina, cukrzyca typu 2