Clear Sky Science · pl
Tworzenie złożonej domeny PIN przez SMG5–SMG6 jest niezbędne dla NMD
Jak komórki chronią się przed wadliwymi komunikatami
Komórki nieustannie odczytują genetyczne komunikaty (mRNA), aby wytwarzać białka. Czasem jednak te komunikaty zawierają wczesne sygnały stop, które doprowadziłyby do powstania skróconych, potencjalnie szkodliwych białek. Proces usuwający takie wadliwe komunikaty nazywa się degradacją mRNA zależną od nonsensu (NMD). Artykuł ten wyjaśnia, jak dwa kluczowe białka, SMG5 i SMG6, fizycznie współpracują przy przecinaniu uszkodzonych komunikatów, rozwiewając długo trwającą zagadkę dotyczącą mechanizmów kontroli jakości w komórce.
Odkrycie ukrytego partnerstwa
Przez lata naukowcy wiedzieli, że SMG6 potrafi bezpośrednio przecinać RNA, podczas gdy SMG5 uważano za „katalitycznie nieaktywne”, pełniące głównie rolę pomocnika lub rusztowania. Jednak eksperymenty komórkowe przynosiły zagadkowy wynik: SMG6 nie działał poprawnie bez SMG5, a NMD zawodziło, jeśli brakowało któregokolwiek z nich. Autorzy użyli najnowszych narzędzi do przewidywania struktur (AlphaFold), testów biochemicznych z oczyszczonymi białkami oraz badań genetycznych w liniach komórek ludzkich, aby rozwiązać tę sprzeczność. Ich modele przewidziały, że ogonowe regiony SMG5 i SMG6, zwane domenami PIN, łączą się ze sobą, tworząc wspólną strukturę. Jednostka ta — nazwana „cPIN” — została zaproponowana jako prawdziwa maszyna tnąca w NMD. 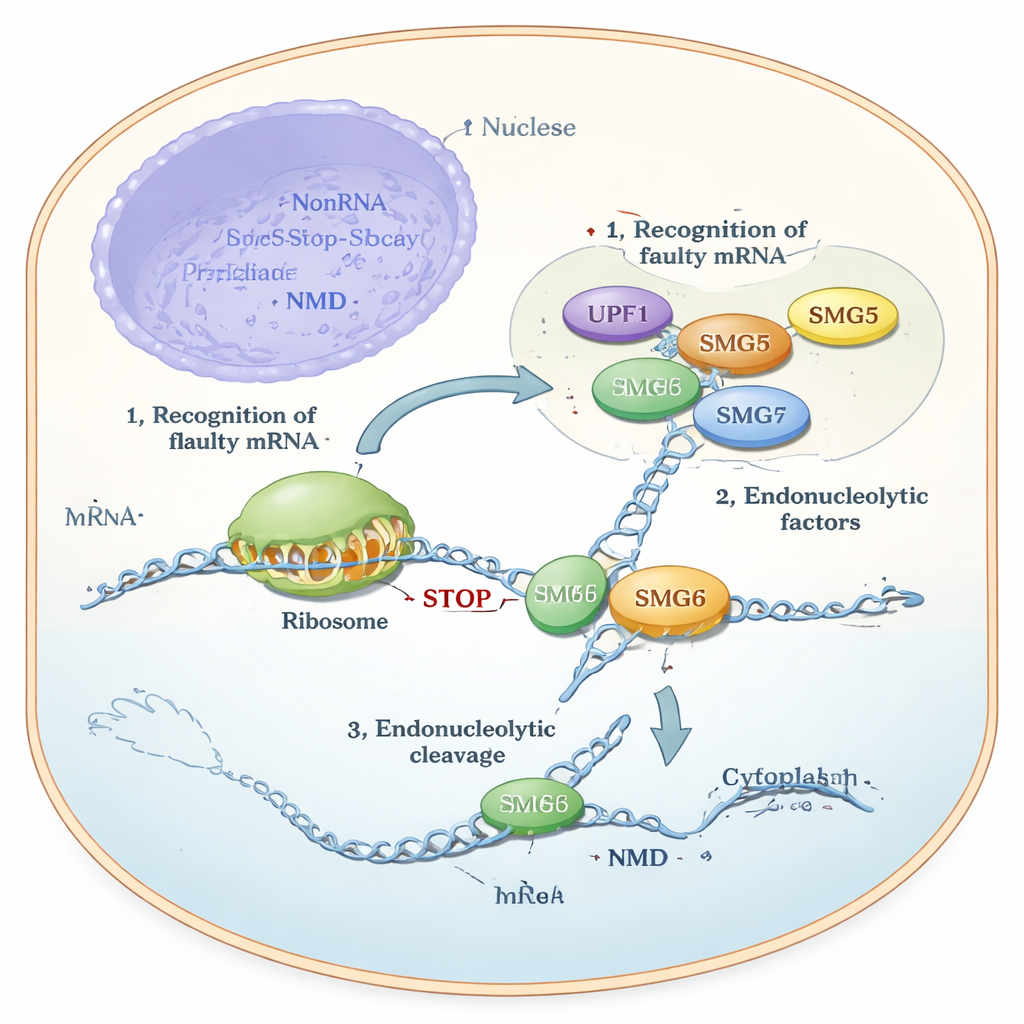
Odbudowa molekularnych nożyc w probówce
Aby przetestować przewidywanie, zespół wyprodukował fragmenty ludzkiego SMG5 i SMG6 w bakteriach i oczyścił je. Samodzielnie SMG6 wykazywał tylko słabą zdolność do przecinania zaprojektowanego substratu RNA, a SMG5 praktycznie żadnej. Jednak po zmieszaniu obu fragmentów aktywność tnąca gwałtownie wzrosła, nawet w warunkach, w których udział zanieczyszczających enzymów był mało prawdopodobny. Ten sam efekt zaobserwowano zarówno na liniowych, jak i kolistych cząsteczkach testowych opartych na RNA, co sugeruje, że zwiększone cięcie rzeczywiście pochodziło od pary SMG5–SMG6. Krzyżowanie chemiczne i spektrometria mas potwierdziły dodatkowo, że dwa białka wchodzą w bliski kontakt, wspierając koncepcję bezpośredniego, choć przejściowego, partnerstwa.
Uzupełnienie krawędzi tnącej
Modele strukturalne sugerowały dokładnie, w jaki sposób SMG5 wzmacnia SMG6. SMG6 dostarcza cztery kwaśne reszty aminokwasowe, które wiążą jony metali w centrum miejsca tnącego, co jest typowe dla tej rodziny enzymów. Ku zaskoczeniu, modele umieściły dodatkową kwaśną resztę z SMG5 tuż obok nich, efektywnie rozszerzając kieszeń katalityczną. Inne dodatnio naładowane reszty w SMG5 przewidywano jako chwytające szkielet RNA i pomagające ustawić go do przecięcia. Gdy badacze zmienili te krytyczne reszty w SMG5 lub SMG6, złożony kompleks stracił dużą część swojej mocy tnącej in vitro. Te same mutacje nie przywróciły też NMD w zmodyfikowanych komórkach ludzkich, w których normalne białko zostało wyczerpane, co ściśle łączy model strukturalny z funkcją komórkową.
Udowodnienie, że obaj partnerzy są niezbędni w komórkach
Ponieważ całkowite usunięcie SMG5 lub SMG6 zabija komórki, zespół zastosował system „degronowy”, który umożliwia znakowanie każdego białka tak, by można je było szybko zniszczyć za pomocą małej cząsteczki. Połączenie tego szybkiego rozkładu z interferencją RNA pozwoliło na niemal całkowite usunięcie SMG5, SMG6 lub centralnego regulatora nazwanego UPF1. Następnie sekwencjonowanie RNA na poziomie genomowym ujawniło, co się dzieje z NMD po utracie każdego czynnika. Odpływ SMG5 lub UPF1 wywołał niemal identyczne zmiany w RNA komórek, z silnym nagromadzeniem wadliwych, wrażliwych na NMD transkryptów. Usunięcie SMG6 dało bardzo podobny, choć nieco łagodniejszy efekt. Dane te pokazują, że SMG5 i SMG6 nie są opcjonalnymi, równoległymi gałęziami ścieżki; przeciwnie, działają razem z UPF1 jako rdzenne składniki jednej głównej drogi degradacji.
Dlaczego to ma znaczenie dla zdrowia komórek
Mówiąc prosto, badanie pokazuje, że SMG5 i SMG6 łączą się, tworząc jedną, wydajną molekularną parę nożyc, która przecina wadliwe komunikaty genetyczne. SMG6 dostarcza większość ostrza, ale SMG5 uzupełnia brakującą krawędź i pomaga utrzymać RNA na miejscu, przekształcając słaby przecinak w efektywne ostrze. Ta złożona „cPIN” wyjaśnia, dlaczego komórki absolutnie potrzebują obu białek, aby utrzymać czystość swoich komunikatów RNA. Poprzez wyjaśnienie, jak kluczowy etap cięcia w NMD jest włączany dopiero wtedy, gdy rozpoznane zostają wadliwe komunikaty, praca ta daje jaśniejszy obraz tego, jak komórki zapobiegają nagromadzeniu toksycznych, skróconych białek i precyzyjnie regulują ekspresję genów.
Cytowanie: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
Słowa kluczowe: degradacja mRNA zależna od nonsensu, kontrola jakości RNA, SMG5 SMG6, nadzór mRNA, regulacja ekspresji genów