Clear Sky Science · pl
Reduktaza S-nitrozoglutathionu GSNOR napędza otyłość związaną z wiekiem, promując „bielenie” tkanki tłuszczowej poprzez de-nitrozację Beclin-1
Dlaczego przyrost masy w połowie życia ma znaczenie
Wiele osób zauważa, że utrzymanie szczupłej sylwetki staje się trudniejsze w czterdziestce i pięćdziesiątce, nawet bez zwiększonego jedzenia czy mniejszej aktywności. Ten przyrost masy w połowie życia podnosi ryzyko cukrzycy, chorób serca i innych schorzeń, a jego biologiczne przyczyny wciąż są odkrywane. Badanie ujawnia wcześniej nieznanego winowajcę w samej tkance tłuszczowej: enzym o nazwie GSNOR, który zmienia sposób, w jaki komórki tłuszczowe zarządzają energią wraz z wiekiem, skłaniając je do większego magazynowania i mniejszego spalania.
Tłuszcz produkujący ciepło kontra tłuszcz zapasowy
Nasz organizm zawiera więcej niż jeden rodzaj tłuszczu. Klasyczna biała tkanka tłuszczowa to dobrze znane magazyn energii, złożony z dużych, jasnych komórek wypełnionych jedną dużą kroplą. W przeciwieństwie do niej, tkanka beżowa i brunatna mają wiele drobnych kropli i dużo mitochondriów — „pieców” komórkowych spalających paliwo dla produkcji ciepła. W młodości większa ilość tłuszczu beżowego pomaga utrzymać masę ciała i poziom glukozy pod kontrolą. Wraz z wiekiem jednak ten tłuszcz ma tendencję do „bielenia”: mitochondria są usuwane, komórki pęcznieją od zmagazynowanego tłuszczu, a ogólny metabolizm zwalnia.
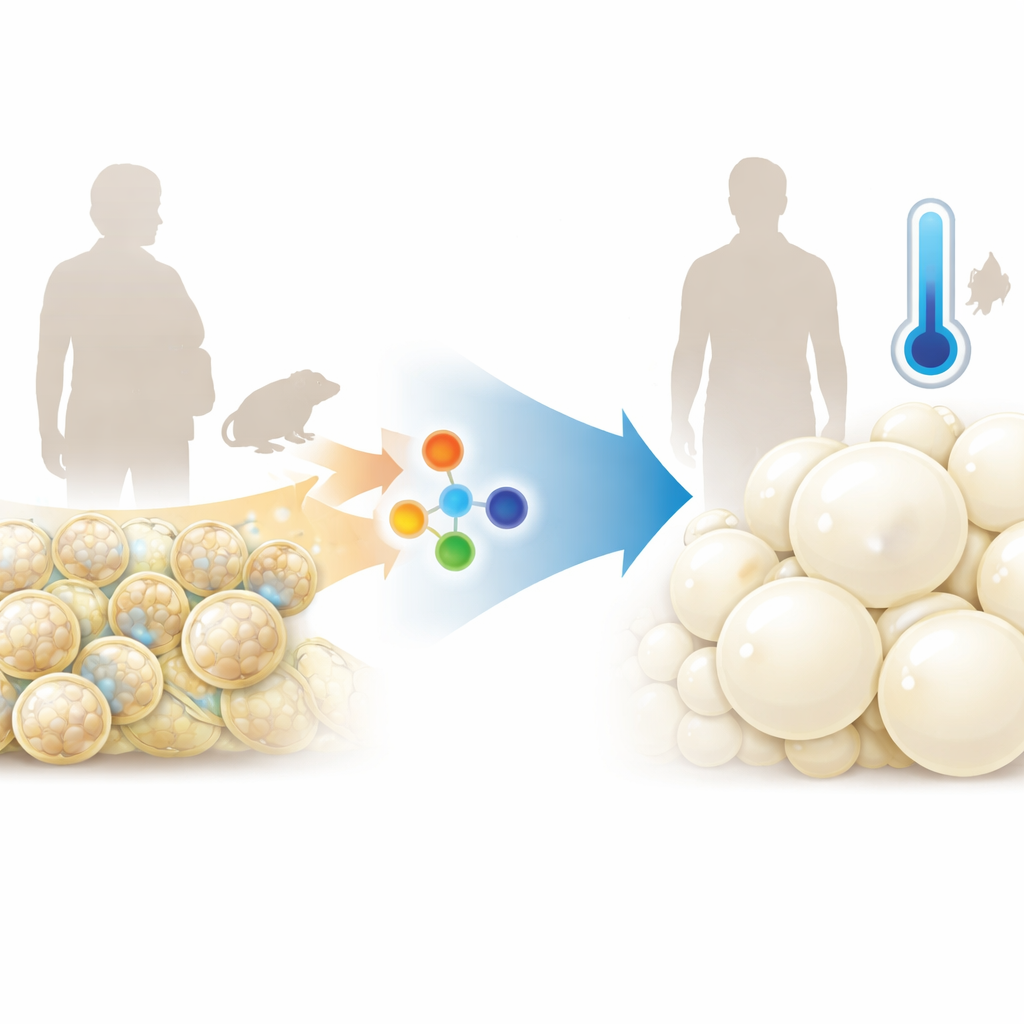
Przełącznik starzenia w tkance tłuszczowej
Naukowcy odkryli, że poziomy GSNOR rosną specyficznie w podskórnej tkance białej u myszy i ludzi w średnim wieku, lecz nie we wszystkich depozytach tłuszczu. GSNOR kontroluje sygnał oparty na tlenku azotu, który modyfikuje wiele białek. Gdy zespół usunął gen GSNOR u myszy, zwierzęta te w dużej mierze opierały się przyrostowi masy związanej z wiekiem. Miały mniej tłuszczu, więcej masy beztłuszczowej, lepszą kontrolę glikemii i wyższe zużycie energii, choć nie jadły mniej ani nie poruszały się więcej niż myszy kontrolne. Ich podskórne poduszki tłuszczowe miały mniejsze komórki i cechy bardziej przypominające beżowe tłuszczaki, z wyższymi markerami mitochondrialnymi i silniejszą aktywnością produkującą ciepło.
Wzrost GSNOR powoduje „bielenie” i otyłość
Aby sprawdzić kierunek odwrotny, naukowcy zwiększyli ekspresję GSNOR tylko w komórkach tłuszczowych, albo przez dostarczenie wirusowe do jednego depozytu tłuszczu, albo poprzez stworzenie myszy z insercją nadekspresji enzymu w tkance tłuszczowej. W obu przypadkach komórki tłuszczowe stały się większe i bledsze, markery mitochondrialne spadły, a geny związane z tłuszczem beżowym i produkcją ciepła zostały stłumione. Myszy z nadekspresją były widocznie otyłe, gorzej utrzymywały temperaturę ciała w zimnie i miały niższe zużycie tlenu oraz wydatkowanie energii. Ważne było to, że zmiana nie wynikała z większego spożycia pokarmu ani z zahamowania rozkładu tłuszczu, lecz z przeprogramowania tożsamości komórek tłuszczowych w kierunku magazynowania energii.
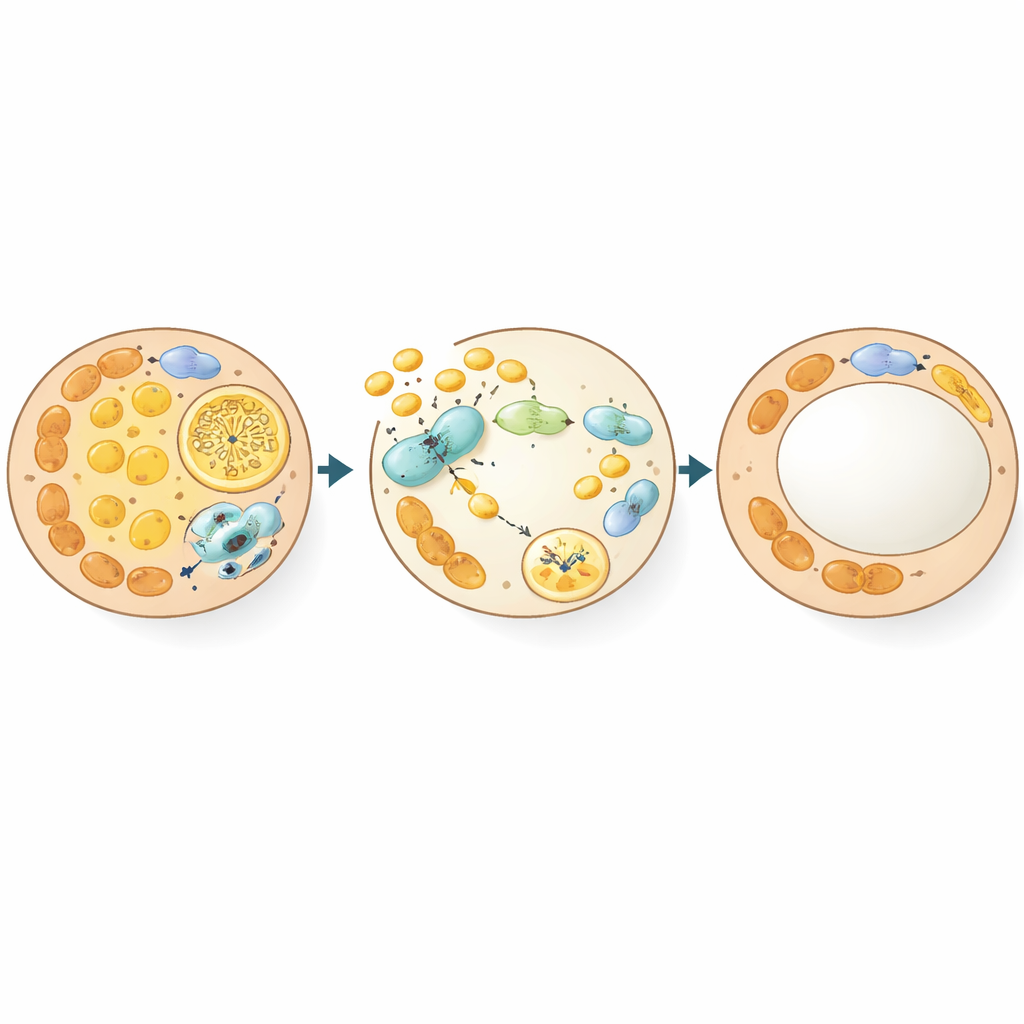
Ukryty hamulec recyklingu komórkowego
Zagłębiając się dalej, zespół zapytał, jak GSNOR przekształca komórki tłuszczowe na poziomie molekularnym. Korzystając z czułych metod proteomicznych, zmapowali białka, których modyfikacja zależna od tlenku azotu zmieniała się przy wysokim GSNOR. Wyłonił się centralny cel: Beclin-1, kluczowy organizator autofagii — procesu, w którym komórki recyklingują komponenty, w tym mitochondria. Zwykle tlenek azotu może przyłączać się do Beclin-1 na specyficznym reszcie cysteiny, działając jak hamulec autofagii. Gdy poziomy GSNOR rosną, ta modyfikacja zostaje usunięta, Beclin-1 silniej wiąże się ze swoim partnerem ATG14, a autofagia przyspiesza. W komórkach tłuszczowych zwiększony recykling preferencyjnie usuwa mitochondria, przesuwając beżowe komórki z powrotem w stronę bielszej, zapasowej postaci. Mikroskopia elektronowa i markery molekularne potwierdziły, że tkanka tłuszczowa bogata w GSNOR lub o mutantowym Beclin-1 miała więcej autofagosomów i mniej mitochondriów podczas przejścia z beżowego na biały fenotyp.
Przebudowa Beclin-1 potwierdza mechanizm
Aby dowieść, że to konkretne miejsce na Beclin-1 ma znaczenie, autorzy zaprojektowali myszy, w których ta cysteina została zastąpiona tak, by nie mogła już nosić modyfikacji zależnej od tlenku azotu. Zwierzęta Beclin-1C351A wykazywały więcej autofagii w tkance tłuszczowej, szybszą utratę cech beżowych i silniejsze bielenie po zaprzestaniu ekspozycji na zimno lub leki pobudzające brązowienie, chociaż ich całkowita masa ciała nie zmieniła się natychmiast. W hodowlach komórkowych blokowanie GSNOR utrzymywało cechy beżowe tylko wtedy, gdy Beclin-1 miało nadal modyfikowalne miejsce; po mutacji utrata GSNOR przestała pomagać. Wreszcie, u myszy w średnim wieku, miejscowe wyciszenie GSNOR w jednym depozycie tłuszczu przywróciło markery beżowe, zmniejszyło rozmiar komórek tłuszczowych i lokalną masę tłuszczu, podkreślając, że tę ścieżkę da się modulować u dorosłych zwierząt.
Co to oznacza dla przyrostu masy w połowie życia
Mówiąc wprost, praca ta identyfikuje GSNOR jako aktywowany z wiekiem przełącznik w tkance tłuszczowej, który przyspiesza utratę „dobrego”, produkującego ciepło tłuszczu beżowego poprzez nadaktywację mechanizmu recyklingu komórkowego za pośrednictwem Beclin-1. Wraz ze wzrostem GSNOR w połowie życia enzym ten usuwa ochronny znacznik tlenku azotu z Beclin-1, umożliwiając nadmierne usuwanie mitochondriów, bielenie tłuszczu, spowolnienie metabolizmu i większą podatność na otyłość. Wyniki sugerują, że leki łagodnie hamujące GSNOR w podskórnym tłuszczu — lub w inny sposób przywracające znak tlenku azotu na Beclin-1 — mogłyby pomóc zachować funkcję tłuszczu beżowego i przeciwdziałać przyrostowi masy i pogorszeniu metabolizmu związanym z wiekiem.
Cytowanie: Qiao, X., Xie, T., Zhang, Y. et al. S-nitrosoglutathione reductase GSNOR drives age-related obesity by promoting adipose tissue whitening through de-nitrosation of Beclin-1. Nat Commun 17, 3059 (2026). https://doi.org/10.1038/s41467-026-69793-3
Słowa kluczowe: otyłość związana z wiekiem, beżowa tkanka tłuszczowa, GSNOR, autofagia, sygnalizacja tlenku azotu