Clear Sky Science · pl
Nierozkładalne analogi acetylolizyny do badania acetylacji białek in vitro i w komórkach
Dlaczego małe chemiczne znaczniki na białkach mają znaczenie
W każdej komórce białka są nieustannie modyfikowane małymi chemicznymi znacznikami, które działają jak przełączniki włącz/wyłącz lub regulatory natężenia ich aktywności. Jednym z najważniejszych takich znaczników jest acetylacja, która może zmieniać zachowanie białka bez modyfikacji jego kodu genetycznego. Dokładne zrozumienie, co robi acetylacja w konkretnym miejscu konkretnego białka, okazało się zaskakująco trudne, ponieważ komórki potrafią usuwać te znaczniki równie szybko, jak je dodają. W tym badaniu przedstawiono pomysłowy chemiczny „zamiennik” acetylacji, którego nie da się usunąć, dając naukowcom sposób na „zamrożenie” tych przełączników i obserwację skutków.
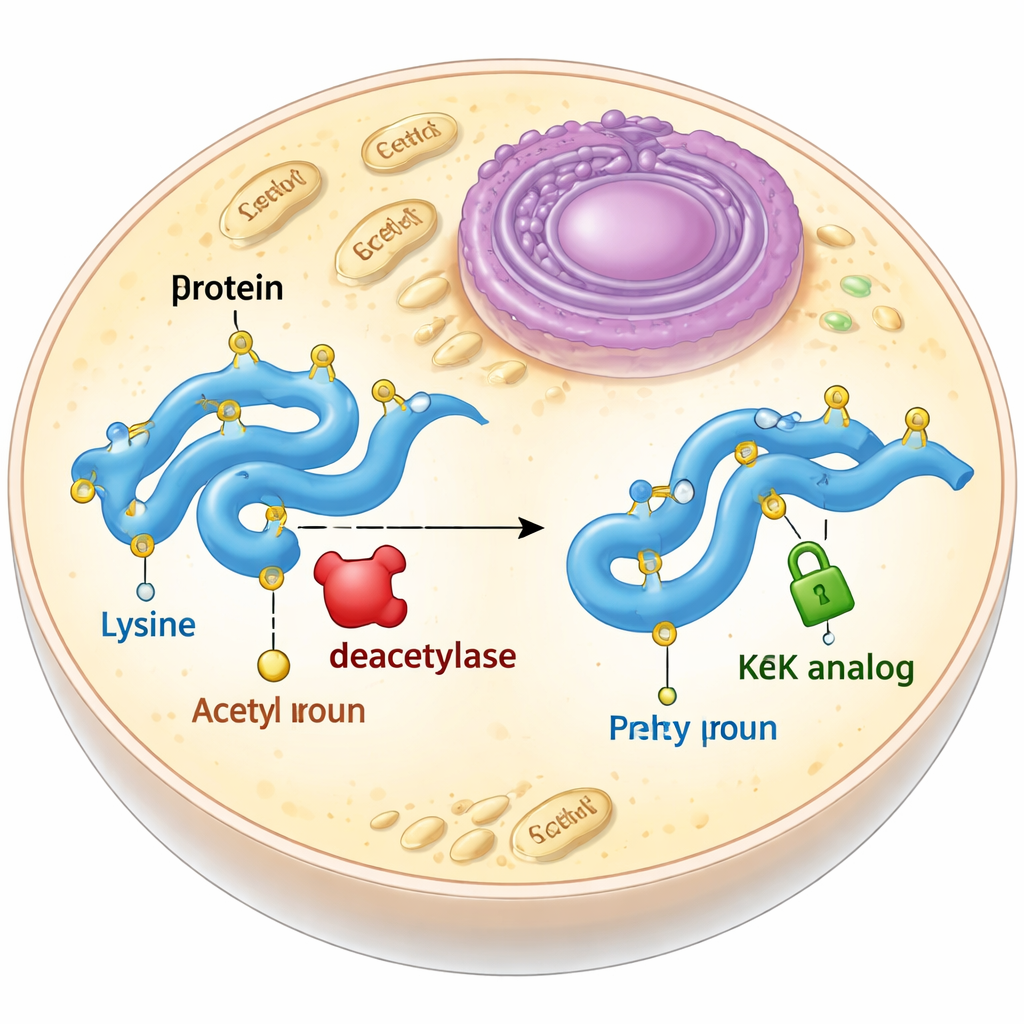
Trwały zastępca ulotnego znacznika
Acetylacja zwykle zachodzi na reszcie aminokwasu nazywanej lizyną. Gdy lizyna jest acetylowana, traci swój ładunek dodatni, a jej łańcuch boczny staje się nieco dłuższy. Biolodzy często próbują to naśladować, mutując lizynę na inny aminokwas, glutaminę, która jest obojętna, ale krótsza, albo wprowadzając prawdziwą acetylolizynę za pomocą rozszerzonego kodu genetycznego. Oba podejścia mają wady: glutamina nie odtwarza w pełni zmian kształtu spowodowanych acetylacją, a prawdziwa acetylolizyna jest szybko usuwana przez enzymy zwane deacetylazami w komórkach. Autorzy postanowili zaprojektować i przetestować analogi acetylolizyny, które zachowują odpowiedni rozmiar i kształt, ale nie dają się usunąć.
Testowanie nowych chemicznych imitacji na białku modelowym
Zespół skupił się najpierw na ubikwitynie, małym, dobrze zbadanym białku, które samo jest ozdabiane wieloma różnymi znacznikami. Wykorzystując zaawansowane inżynierstwo genetyczne, umieścili w jednej pozycji ubikwityny różne warianty lizyny: naturalną acetylolizynę, dwa nierozkładalne analogi o nazwach TFAcK i ketolizyna (KeK) oraz powszechnie stosowane substytuty, takie jak glutamina, alanina i arginina. Następnie badali, jak te zmiany wpływają na kształt i funkcję ubikwityny. Pomiary wysokorozdzielcze metodą NMR wykazały, że acetylolizyna, TFAcK i KeK wywołują niemal identyczne zmiany strukturalne, szczególnie wokół centralnej helisy, podczas gdy glutamina i inne proste mutacje tego nie robiły. Testy funkcjonalne z użyciem enzymu HDM2 ujawniły, że ubikwityna zawierająca acetylolizynę, TFAcK lub KeK zachowywała się podobnie między sobą i odmiennie od wersji z glutaminą, co podkreśla, że długość i objętość łańcucha bocznego — nie tylko jego ładunek — są kluczowe.
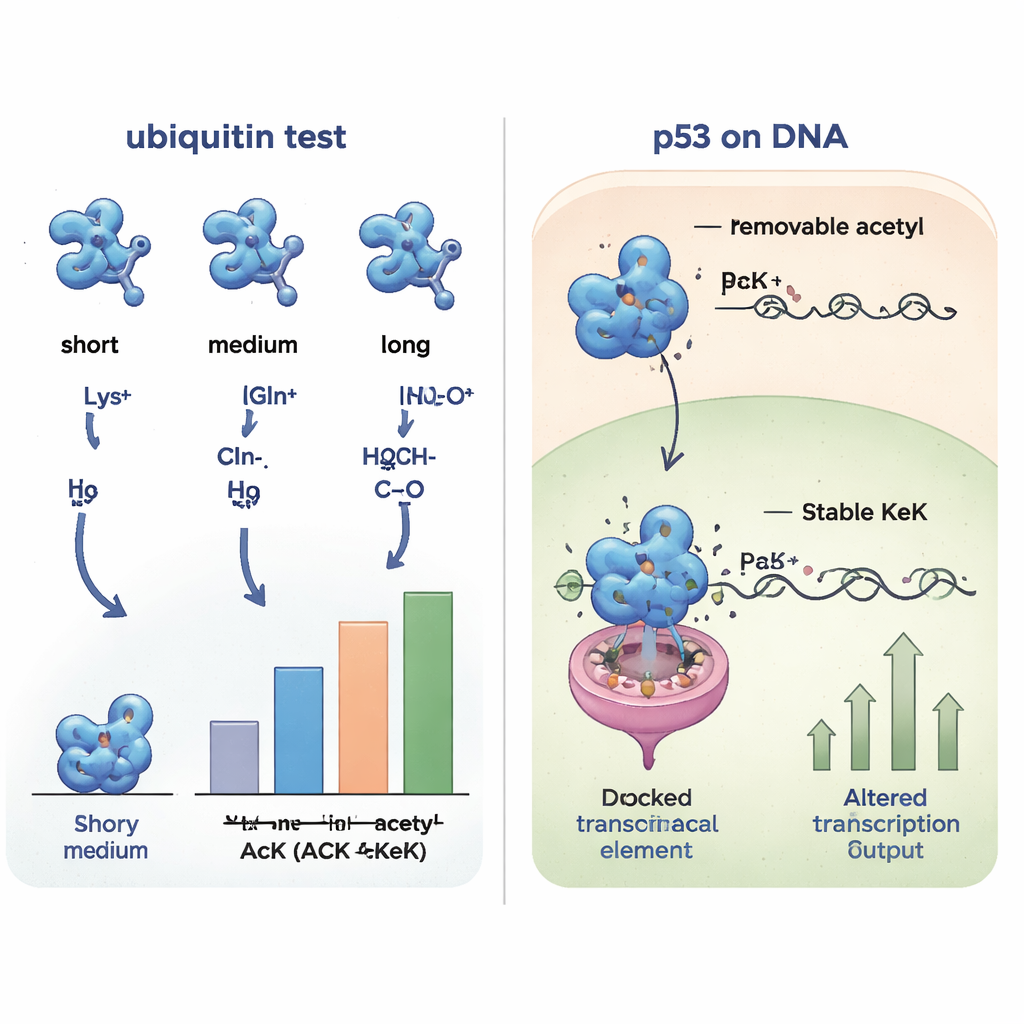
Badanie partnerskich interakcji białek w całej komórce
Ponieważ niewielkie zmiany strukturalne mogą zmieniać, z którymi partnerami białko wchodzi w interakcje, badacze porównali następnie, jak różne wersje ubikwityny wiązały się z innymi białkami pochodzącymi z ekstraktów ludzkich komórek. Wyławiając partnerów wiążących i identyfikując je metodą spektrometrii mas, stwierdzili, że ubikwityna zawierająca acetylolizynę, TFAcK lub KeK wykazywała bardzo podobne wzorce interakcji, podczas gdy formy z glutaminą lub alaniną tworzyły odrębną grupę i wyglądały inaczej. Warianty dodatnio naładowane (lizyna lub arginina) utworzyły jeszcze inną grupę. To systematyczne porównanie pokazało, że nierozkładalne analogi TFAcK, a szczególnie KeK, lepiej naśladują zarówno strukturę, jak i zachowanie wiążące prawdziwej acetylacji niż tradycyjna substytucja glutaminą.
Zablokowanie acetylacji białka supresorowego p53
Aby sprawdzić, czy te narzędzia działają w żywych komórkach, autorzy zwrócili się do p53, kluczowego białka supresorowego guza nazywanego często „strażnikiem genomu”. Specyficzne lizyny w regionie wiążącym DNA p53 mogą być acetylowane, co zmienia, które geny są przez niego włączane, na przykład te zatrzymujące cykl komórkowy lub wywołujące apoptozę. Zespół zaprojektował komórki ludzkie tak, aby p53 włączało acetylolizynę, TFAcK lub KeK w dwóch istotnych pozycjach lizyny (120 i 164) tylko wtedy, gdy dostarczono odpowiadający niestandardowy aminokwas. Wszystkie trzy mogły zostać wbudowane w p53, ale szczegółowe pomiary wykazały, że w komórkach grupy acetylowe i TFAcK były w dużej mierze usuwane przez deacetylazy, podczas gdy KeK pozostawał nietknięty. Gdy testowano zdolność p53 do aktywacji raportera genowego i naturalnego genu p21, warianty z KeK w tych miejscach były znacznie mniej aktywne, co odpowiada oczekiwanemu rezultatowi przy zablokowanej acetylacji w tych pozycjach, natomiast acetylolizyna i TFAcK zachowywały się bardziej jak normalne p53, ponieważ zostały zdeacetylowane.
Co to oznacza dla badania decyzji komórkowych
Podsumowując, badanie pokazuje, że KeK jest wiernym i nierozkładalnym zamiennikiem acetylolizyny: bardzo dobrze odwzorowuje zmiany strukturalne, preferencje wiążące i funkcjonalne konsekwencje acetylacji, a jednocześnie nie może być usunięty przez enzymy komórkowe. Dla osób niebędących specjalistami oznacza to, że naukowcy mają teraz sposób, by „zamrozić” normalnie odwracalny chemiczny przełącznik w pojedynczym miejscu na białku i obserwować, jak to wpływa na procesy takie jak regulacja genów i decyzje o losie komórki. Powinno to ułatwić oddzielenie specyficznych ról acetylacji od innych nakładających się modyfikacji i w końcu wyjaśnić, jak nieprawidłowo regulowana acetylacja białek przyczynia się do chorób, takich jak nowotwory.
Cytowanie: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Słowa kluczowe: acetylacja białek, modyfikacja potranslacyjna, ubikwityna, p53, ekspansja kodu genetycznego