Clear Sky Science · pl
Dynamiczne przebudowywanie transkryptomu w przeszczepionych ludzkich komórkach progenitorowych układu nerwowego ujawnia mechanizmy zachowania widzenia w modelu szczura z retiną barwnikową
Dlaczego ochrona utraconego wzroku ma znaczenie
Retinitis pigmentosa to grupa chorób dziedzicznych, które stopniowo pozbawiają ludzi wzroku, często zaczynając od nocnej ślepoty i postępując aż do prawnej ślepoty. Ponieważ setki różnych mutacji genowych mogą wywołać to schorzenie, leczenie każdej z nich za pomocą terapii genowej jest trudne. W tym badaniu zbadano bardziej uniwersalne podejście: przeszczepienie ludzkich komórek progenitorowych układu nerwowego — niedojrzałych komórek nerwowych hodowanych w laboratorium — do oka, aby chronić pozostające komórki światłoczułe. Zrozumienie, jak dokładnie te przeszczepione komórki zachowują się i pomagają zachować wzrok, może kształtować przyszłe terapie nie tylko dla retinitis pigmentosa, lecz także dla innych schorzeń prowadzących do utraty wzroku.
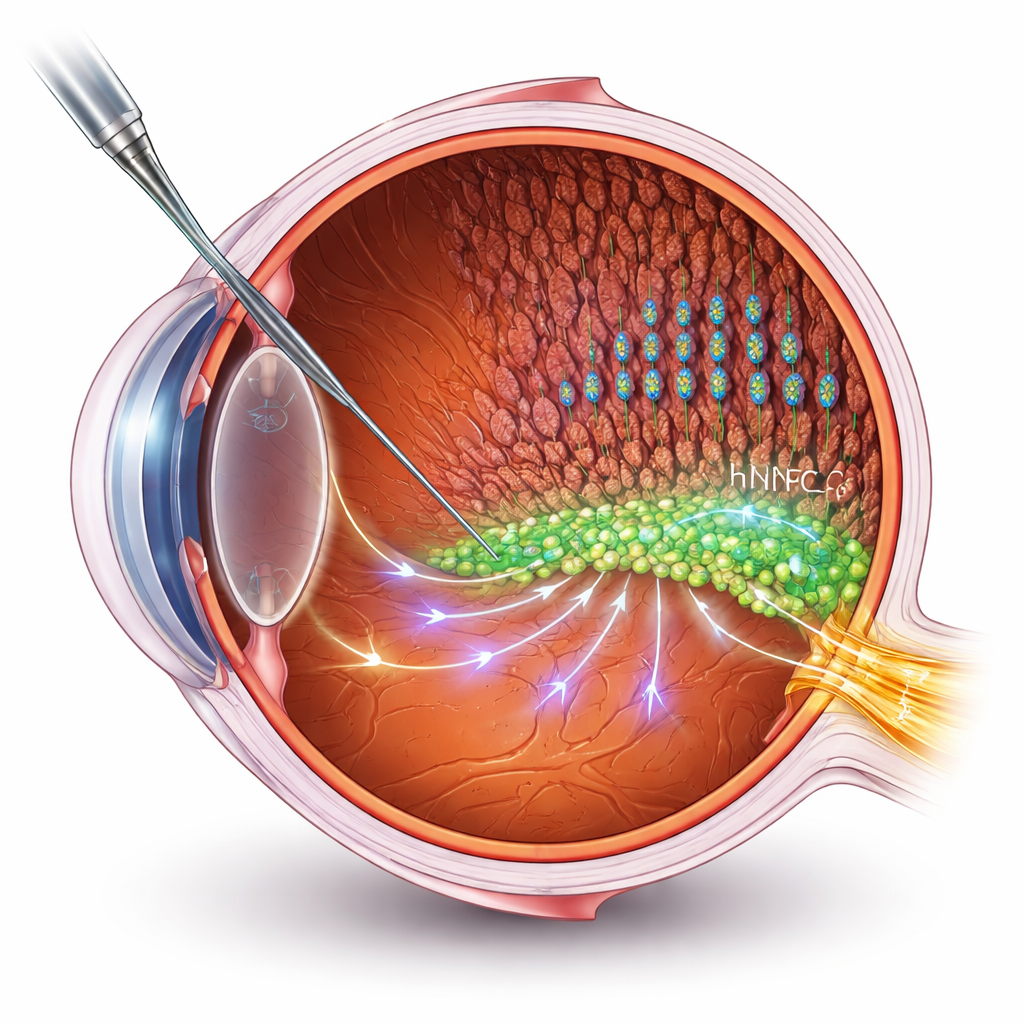
Wspieranie komórek zamiast ich zastępowania
Wiele terapii komórkowych ma na celu zastąpienie martwych lub uszkodzonych komórek. Jednak w zaawansowanych chorobach siatkówki odbudowa połączeń z mózgiem stanowi duże wyzwanie techniczne. Autorzy badania wybrali inną drogę: wykorzystanie ludzkich komórek progenitorowych układu nerwowego (hNPC) jako „pomocników”, którzy wspierają własne komórki siatkówki pacjenta. Przeszczepili hNPC do przestrzeni podsiatkówkowej dobrze znanego modelu szczura z retinitis pigmentosa, a następnie oceniali wzrok za pomocą zapisów elektrycznych i testów behawioralnych. Leczone szczury zachowały lepszą funkcję wzrokową i bardziej nienaruszone warstwy fotoreceptorów — pręcików i czopków przechwytujących światło — niż zwierzęta nieleczone, choć degeneracja wciąż postępowała powoli.
Jak przeszczepione komórki zmieniają się w chorym oku
Aby zobaczyć, co dzieje się na poziomie molekularnym, zespół użył sekwencjonowania RNA pojedynczych komórek, techniki profilującej, które geny są aktywne w tysiącach pojedynczych komórek. Śledzili przeszczepione hNPC w dwóch punktach czasowych, odpowiadających w przybliżeniu wczesnym i późniejszym etapom po transplantacji. Zamiast przekształcać się w nowe fotoreceptory, większość przeszczepionych komórek dojrzała do postaci przypominającej astrocyty, a mniejsza część wykazywała markery oligodendrocytów lub niedojrzałych neuronów. Z upływem czasu komórki te się stabilizowały, nabierając cech sugerujących, że są przystosowane do przetrwania w stresującym, degenerującym środowisku i do bliskiej interakcji z sąsiednimi komórkami siatkówki.
Sygnały ochronne, metabolizm i sprzątanie
hNPC wytwarzały bogatą mieszaninę białek ochronnych znanych jako czynniki troficzne. Wśród nich znajdowały się MANF i MYDGF, powiązane z przeżyciem komórek, zmniejszeniem stresu oksydacyjnego i tłumieniem stanu zapalnego, a także inne czynniki, takie jak midkine i pleiotrofin, które wspierają wzrost i migrację komórek nerwowych. Molekuły te wydawały się działać zarówno na sam przeszczep, jak i na otaczającą siatkówkę. U leczonych szczurów pręciki i czopki wykazywały wzorce aktywności genów bliższe zdrowym kontrolom, z poprawionym wsparciem dla sygnalizacji wzrokowej i utrzymania komórek. Przeszczepione komórki też wzmocniły szlaki zaangażowane w usuwanie szczątków komórkowych i dostosowywanie metabolizmu, co sugeruje, że pomagają fotoreceptorom radzić sobie z zapotrzebowaniem energetycznym i toksycznymi produktami ubocznymi gromadzącymi się w chorobie.
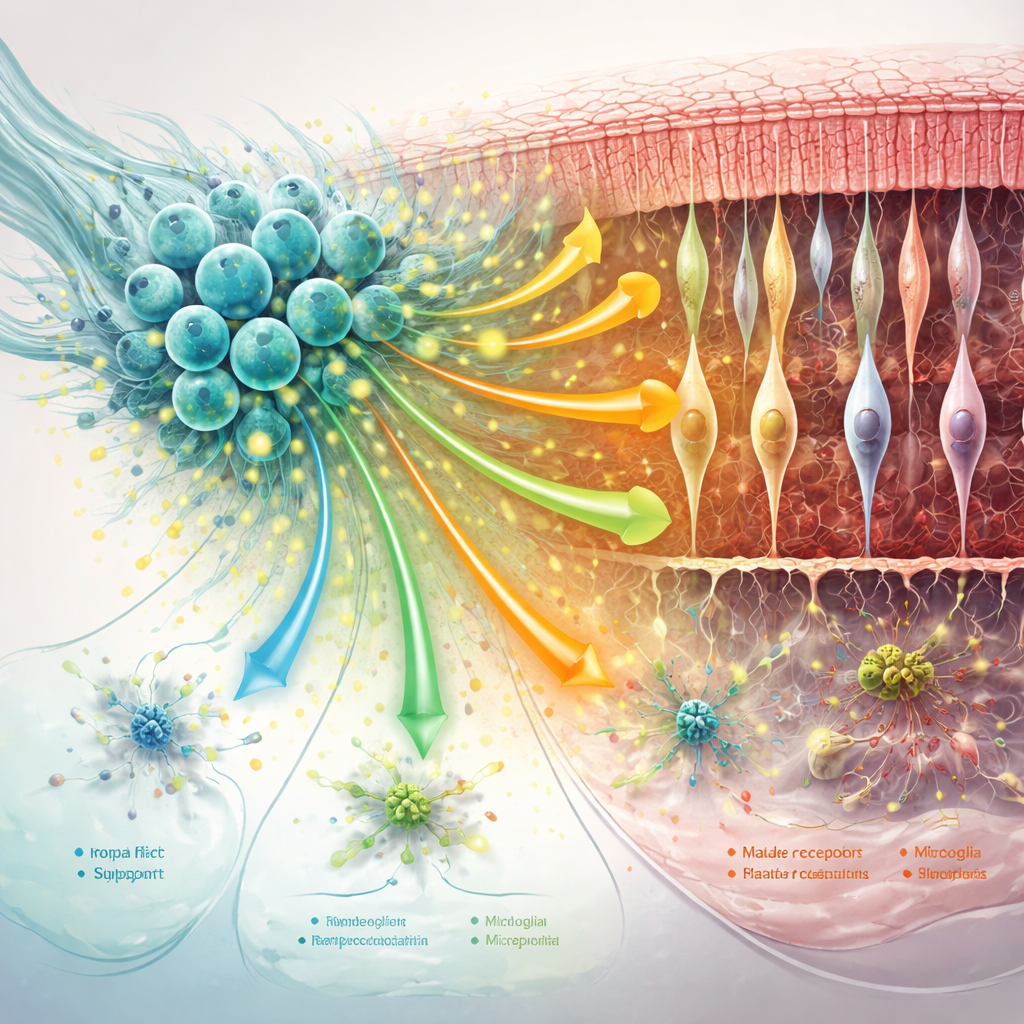
Uspokojenie komórek wspierających i przekształcanie sąsiedztwa siatkówki
Sieć wspierająca siatkówki — komórki Müller, mikroglej i otaczająca macierz białkowa — odgrywa dużą rolę w pogarszaniu lub spowalnianiu degeneracji. Badanie wykazało, że leczenie hNPC zmniejszyło kluczowe markery szkodliwych „reaktywnych” zmian w komórkach Müllera i przesunęło mikroglej z nadmiernie zapalnych stanów, zwłaszcza we wcześniejszych punktach czasowych. Jednocześnie wzmocniono sygnały komunikacyjne, które pomagają stabilizować synapsy, zespalać komórki i utrzymywać rusztowanie wokół fotoreceptorów. W miarę postępu choroby część tych korzyści zanikała: ogólna komunikacja międzykomórkowa osłabła, pewne ścieżki ochronne — w tym sygnalizacja związana z MANF — zmniejszyły się, a komórki wspierające przyjęły bardziej stresowo- i immunologicznie ukierunkowane profile.
Co to oznacza dla przyszłych terapii oczu
Dla osoby niebędącej specjalistą najważniejsze jest to, że przeszczepione ludzkie komórki progenitorowe układu nerwowego mogą działać jak miejscowi „ratownicy pierwszej potrzeby” w degenerującej siatkówce. Nie odbudowują siatkówki od podstaw, ale uwalniają molekuły ochronne, dostosowują metabolizm, łagodzą szkodliwe zapalenie i pomagają utrzymać lokalną strukturę, co razem spowalnia utratę wzroku. Jednak ten efekt ochronny słabnie z czasem, gdy środowisko staje się bardziej wrogie, a dialog między przeszczepem a komórkami gospodarza osłabia się. Autorzy sugerują, że wzmocnienie kluczowych czynników, takich jak MANF, oraz poprawa stanu zdrowia siatkówki gospodarza — na przykład poprzez inżynierię genetyczną przeszczepu lub terapie skojarzone — mogą być niezbędne, by przemienić chwilową ulgę w trwale długotrwałą ochronę wzroku.
Cytowanie: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Słowa kluczowe: retinitis pigmentosa, terapia komórkami macierzystymi, degeneracja siatkówki, neuroprotekcja, sekwencjonowanie RNA pojedynczych komórek