Clear Sky Science · pl
TCL1A pośredniczy w defektach metylacji DNA w nawrotowych pęcherzykowatych zaśniadach u pacjentek z patogennymi wariantami NLRP7
Dlaczego to ma znaczenie dla zdrowia kobiet
Niektóre ciąże kończą się bardzo wcześnie, przekształcając się w skupisko nieprawidłowej tkanki łożyskowej zamiast w rozwijające się dziecko. Ten stan, zwany pęcherzykowatym zaśniadem, może się powtarzać u niektórych kobiet i czasem przechodzić w nowotwór. Badanie to zgłębia jeden z głównych genetycznych powodów tych rzadkich, lecz poważnych ciąż i ujawnia, jak pojedynczy wadliwy mechanizm ochronny w komórce jajowej może zaburzyć chemiczne „etykietki”, które kierują prawidłowym rozwojem.
Problem ciąży zakorzeniony w komórce jajowej
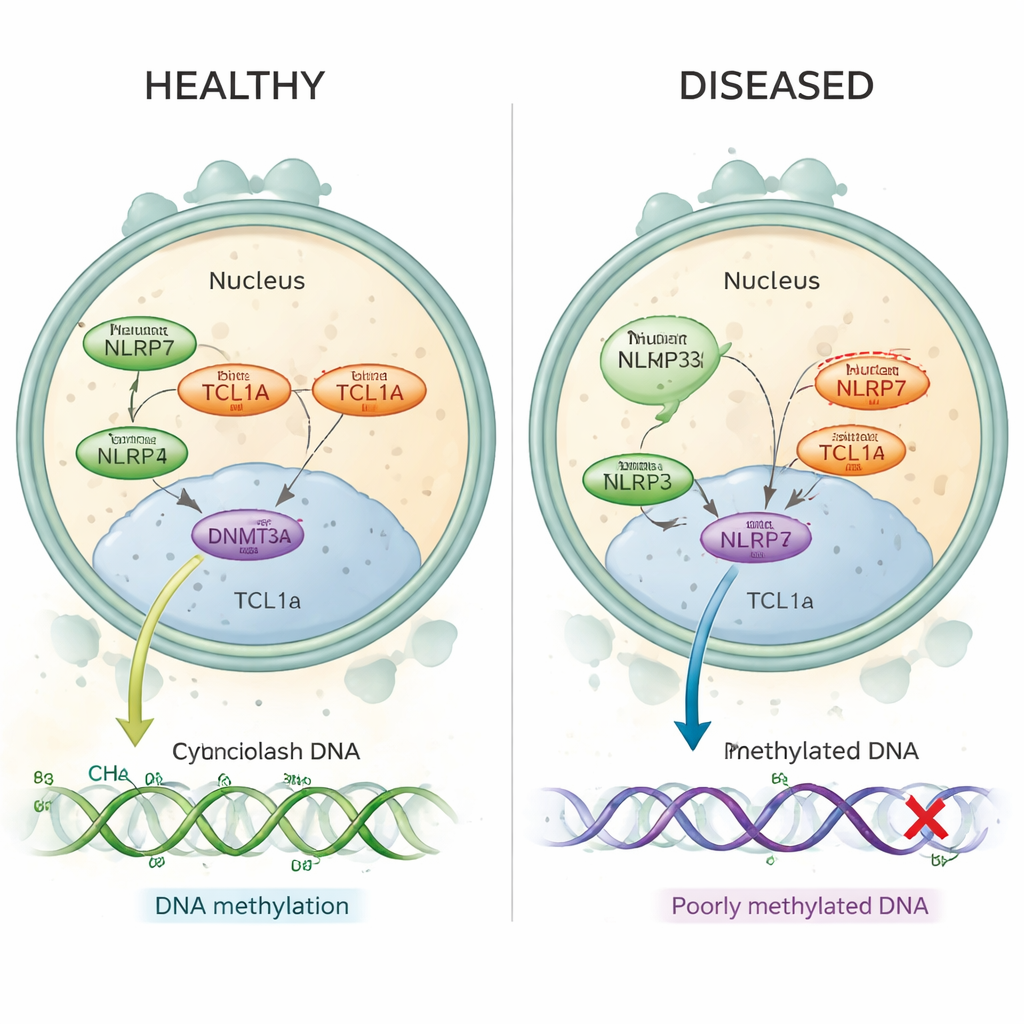
Nawrotowy pęcherzykowaty zaśniad to zaburzenie, w którym kobiety doświadczają powtarzających się ciąż zaśniadowych, często bez normalnych ciąż pomiędzy nimi. Wiele takich przypadków jest obecnie znanych jako spowodowane szkodliwymi zmianami w genie NLRP7, który jest aktywny w komórce jajowej przed i tuż po zapłodnieniu. U tych kobiet kluczowe fragmenty DNA, które powinny nosić „piętno” od matki, pozbawione są normalnych znaków metylacji — małych chemicznych znaczników pomagających w włączaniu lub wyłączaniu genów w odpowiednim czasie. Dotychczas naukowcom nie było jasne, jak białko znajdujące się w cytoplazmie komórki jajowej, takie jak NLRP7, mogłoby kontrolować metylację zachodzącą na DNA upakowanym w jądrze.
Odnalezienie brakującego partnera
Aby rozwiązać tę zagadkę, badacze przeanalizowali odrzucone ludzkie komórki jajowe i bardzo wczesne zarodki z klinik leczenia niepłodności. Wyizolowali NLRP7 i jego znane partnerki z tych komórek i zidentyfikowali inne białka, które towarzyszą kompleksowi. Jeden z nich wyróżniał się: TCL1A, już znane w nowotworach krwi jako białko mogące wnikać do jądra i zakłócać działanie enzymów metylujących DNA, DNMT3A i DNMT3B. TCL1A występuje w komórkach jajowych człowieka w nietypowo dużych ilościach, co sugeruje jego istotną rolę. Szczegółowe testy interakcji wykazały, że TCL1A wiąże się mocno i specyficznie z NLRP7, ale nie z blisko spokrewnionymi białkami, oraz że ten kompleks jest włączony w większą, specyficzną dla komórki jajowej strukturę zwaną podkorowym kompleksem macierzystym.
Widok molekularnego uścisku
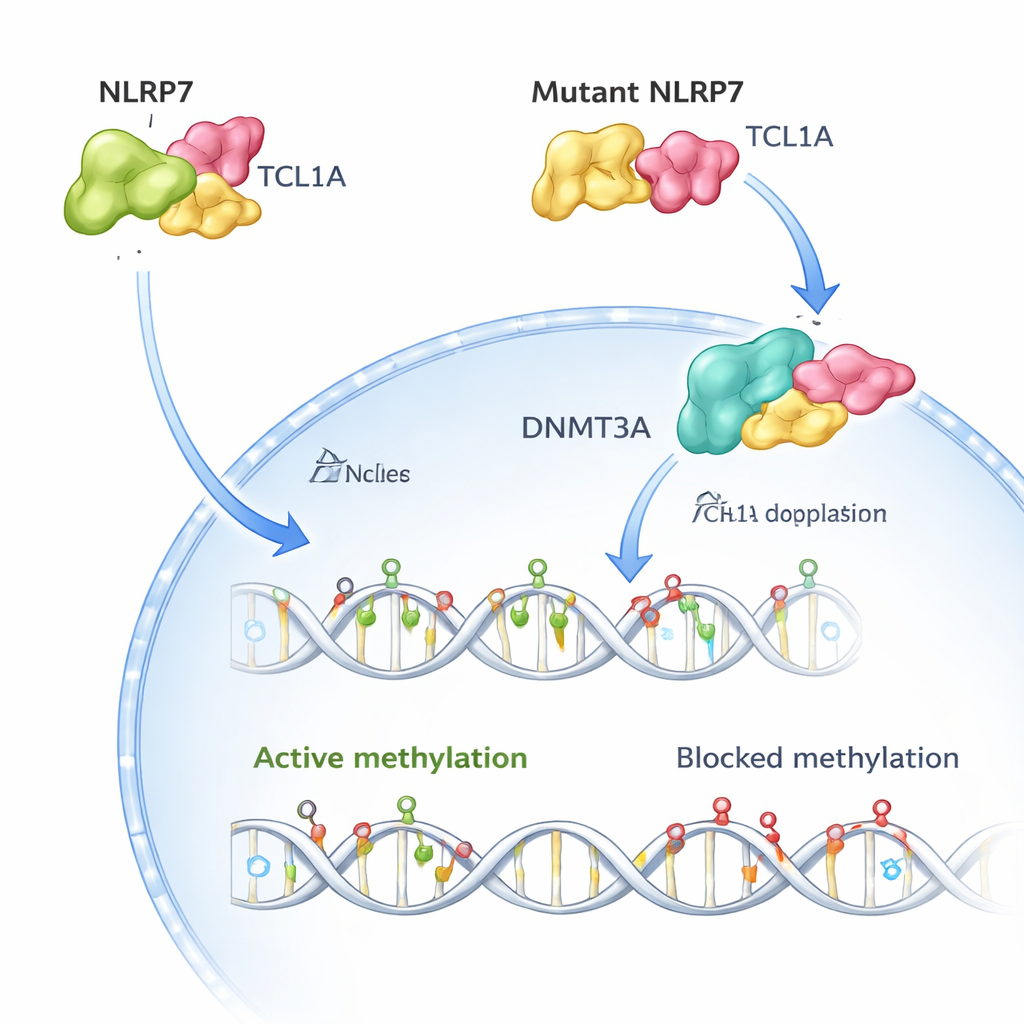
Zespół następnie zastosował krioelektronową mikroskopię, aby zobrazować trójwymiarową strukturę kompleksu NLRP7–TCL1A. Stwierdzili, że dwie cząsteczki NLRP7 łączą się parami, a każda z nich obejmuje dimer TCL1A wzdłuż zakrzywionej powierzchni z powtarzających się motywów. To ułożenie wyjaśnia, dlaczego wiele zmian powodujących chorobę w NLRP7 skupia się wzdłuż tej powierzchni: modyfikacja kluczowych punktów kontaktu osłabia lub niszczy połączenie z TCL1A. Gdy badacze odtworzyli w komórkach ponad 50 znanych wariantów z pacjentów, większość wersji powiązanych z nawrotowymi ciążami zaśniadowymi albo destabilizowała NLRP7, albo wyraźnie zmniejszała jego zdolność do wiązania TCL1A.
Jak błędne rozmieszczenie białek zaburza znaki DNA
W zdrowych ludzkich komórkach jajowych zarówno NLRP7, jak i TCL1A znajdują się głównie w cytoplazmie, przy czym tylko niewielka ilość TCL1A trafia do jądra. Autorzy pokazują, że NLRP7 działa efektywnie jako strażnik: kiedy potrafi utrzymać TCL1A, TCL1A pozostaje poza jądrem. Gdy NLRP7 jest zmutowany i nie może dobrze wiązać, TCL1A przedostaje się do jądra. Tam przyłącza się do DNMT3A, głównego enzymu zakładającego nowe markery metylacji w komórkach jajowych, i tłumi jego aktywność. W modelach komórek macierzystych, które normalnie zyskują metylację w miarę dojrzewania, nadprodukcja TCL1A spowodowała dramatyczną utratę metylacji w całym genomie, podczas gdy współekspresja NLRP7 częściowo naprawiała ten defekt. Razem te ustalenia wspierają prosty obraz: normalne NLRP7 trzyma hamulec metylacyjny (TCL1A) zablokowany w cytoplazmie, dzięki czemu DNMT3A może prawidłowo oznaczać DNA; wadliwe NLRP7 pozwala temu hamulcowi przesunąć się do jądra i zablokować proces.
Od mechanizmu do diagnostyki
Poza wyjaśnieniem, jak powstają nawrotowe ciąż zaśniadowe, badanie sugeruje praktyczny sposób oceny, czy właśnie odkryta zmiana w NLRP7 u pacjentki jest naprawdę szkodliwa. Autorzy porównują trzy podejścia — testy laboratoryjne wiązania NLRP7–TCL1A, przewidywania komputerowe i standardowe narzędzia oceny genetycznej — i pokazują, że utrata wiązania z TCL1A silnie koreluje z wariantami powodującymi chorobę. Odkrywają też wcześniej nierozpoznany szkodliwy wariant, L766R, w rodzinach z nawrotami zaśniadów, potwierdzając, że zarówno osłabia on białko, jak i przekierowuje TCL1A do jądra.
Co to znaczy w prostych słowach
Ta praca ujawnia łańcuch molekularnych zdarzeń stojących za rzadkim, ale wyniszczającym zaburzeniem ciąży. W istocie, komórki jajowe pacjentek niosą uszkodzone „ciało‑straż” — białko NLRP7 — które nie utrzymuje partnera TCL1A poza jądrem. Gdy TCL1A znajdzie się w jądrze, zakłóca działanie enzymu zapisującego istotne chemiczne znaczniki na DNA. Bez tych znaczników wczesne łożysko rozwija się nieprawidłowo i nie powstaje płód. Śledząc tę ścieżkę krok po kroku, badanie wyjaśnia, dlaczego niektóre zmiany genetyczne u matek mogą wielokrotnie sabotować ciąże, oraz wskazuje drogę do bardziej precyzyjnego doradztwa genetycznego i diagnostyki dla kobiet z nawrotowymi pęcherzykowatymi zaśniadami.
Cytowanie: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
Słowa kluczowe: metylacja DNA, nawrotowy pęcherzykowaty zaśniad, NLRP7, TCL1A, genomiczne piętno