Clear Sky Science · pl
GCN5 napędza postęp MASLD poprzez szlak sygnalizacyjny LXRα/SREBP1c—zależną de novo lipogenezę
Dlaczego ta historia wątroby ma znaczenie
Metabolicznie związana ze stłuszczeniem wątroby choroba (MASLD), wcześniej nazywana niealkoholową stłuszczeniową chorobą wątroby, dotyka obecnie około jednej na cztery osoby na świecie. Często rozwija się bezobjawowo, ale może przechodzić w zwłóknienie, raka wątroby i poważne zaburzenia metaboliczne. To badanie odkrywa molekularny „pokrętło głośności”, który napędza szkodliwe gromadzenie tłuszczu w wątrobie, i pokazuje, że jego przykręcenie może chronić wątrobę i potencjalnie uczynić bezpieczniejszymi istniejące strategie lecznicze ukierunkowane na serce.
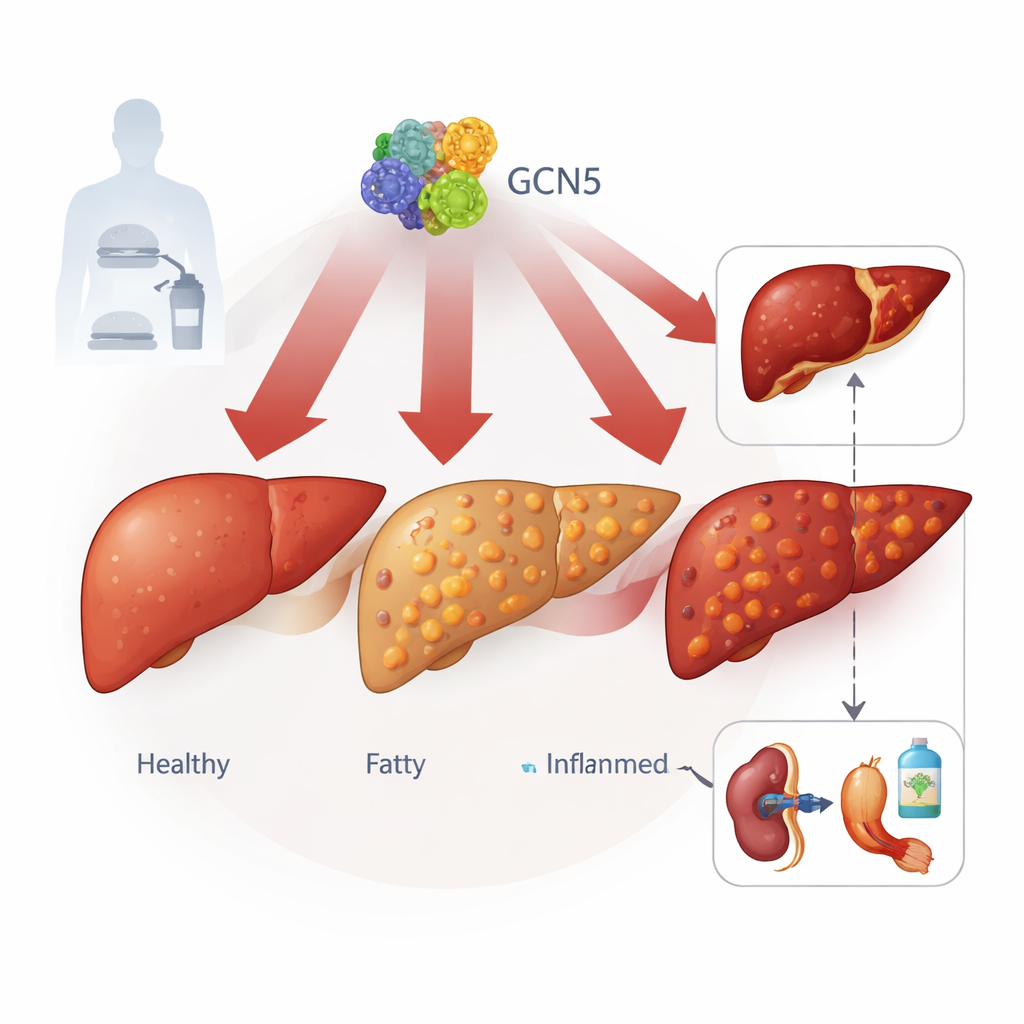
Ukryty przełącznik wewnątrz komórek wątroby
Autorzy koncentrują się na białku o nazwie GCN5, najlepiej znanym jako regulator stopnia upakowania DNA. Analizując tkankę wątrobową od ponad 100 osób — od zdrowych po ciężkie MASLD — oraz z kilku modeli mysich z dietą wywołującą stłuszczenie wątroby, stwierdzili, że poziomy GCN5 w komórkach wątroby rosną stopniowo wraz z pogorszeniem choroby. Białko blisko spokrewnione, PCAF, nie wykazywało tego wzorca, co sugeruje szczególną rolę GCN5. Wysoki poziom GCN5 korelował z większą zawartością tłuszczu w wątrobie, wyższymi lipidami we krwi i silniejszymi oznakami uszkodzenia wątroby, łącząc ten molekularny przełącznik z rzeczywistą ciężkością choroby.
Podkręcanie i wyłączanie GCN5 u zwierząt
Aby przetestować zależność przyczyna–skutek, zespół genetycznie zwiększył lub usunął GCN5 specyficznie w komórkach wątroby myszy. Gdy GCN5 był podniesiony, myszy na diecie wysokotłuszczowej rozwijały cięższe, bardziej stłuszczone wątroby, wyższe stężenia lipidów we krwi i więcej uszkodzeń komórek wątroby, mimo że nie jadły więcej ani nie przybierały na masie ciała. Hodowane in vitro komórki wątrobowe zachowywały się podobnie: dodatkowy GCN5 prowadził do większych i liczniejszych kropli tłuszczu. Natomiast myszy zaprojektowane tak, żeby brakowało im GCN5 wyłącznie w komórkach wątroby, były silnie chronione. W kilku modelach dietetycznych odzwierciedlających ludzkie MASLD i jego cięższą zapalną postać, te zwierzęta gromadziły mniej tłuszczu w wątrobie, miały niższe stężenia lipidów i enzymów wątrobowych we krwi oraz wykazywały mniej zapalenia i zwłóknienia.
Jak GCN5 popycha wątrobę do produkcji tłuszczu
Wnikając w metabolizm, badacze zmierzyli wiele kwasów tłuszczowych i ich prekursorów w wątrobie. Utrata GCN5 głównie zmniejszała ilość tłuszczów, które wątroba wytwarza od podstaw, procesu nazywanego de novo lipogenezą, przy jednoczesnym pozostawieniu tłuszczów wielonienasyconych pochodzenia dietetycznego w dużej mierze niezmienionych. Eksperymenty z ekspresją genów i śledzeniem izotopowym wykazały, że GCN5 działa powyżej głównego regulatora syntezy tłuszczów, SREBP1c. Gdy GCN5 był aktywny, geny budujące i modyfikujące kwasy tłuszczowe były włączone, a wewnętrzne tempo produkcji tłuszczu w wątrobie wzrosło. Usunięcie lub zablokowanie GCN5 wyciszało ten program, zmniejszając przepływ węgla z cukru do nowo wytwarzanego tłuszczu w wątrobie.
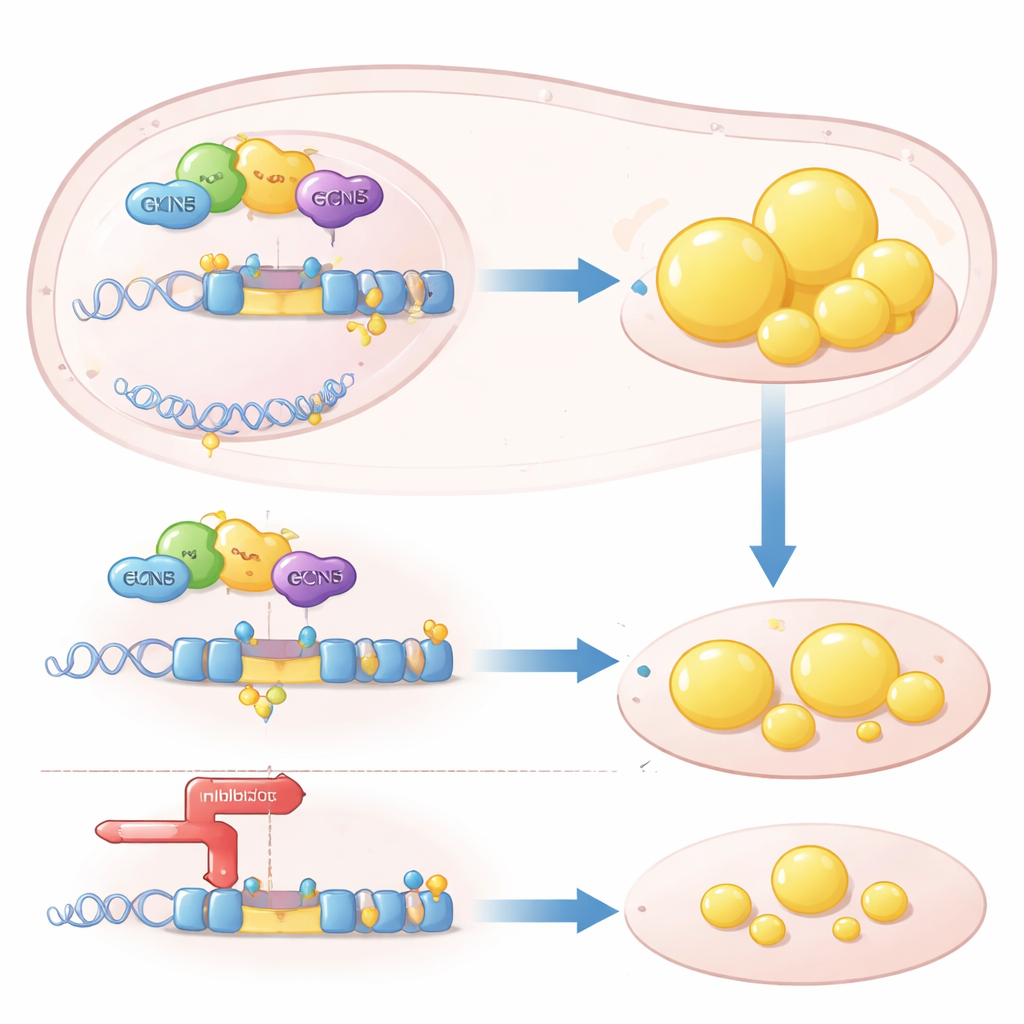
Epigenetyczna dźwignia na kluczowym genie tłuszczowym
Mechanicznie GCN5 działa jako „epigenetyczna” dźwignia: chemicznie modyfikuje białka histonowe na DNA, ułatwiając odczyt niektórych genów. Autorzy wykazali, że GCN5 jest rekrutowany do regionu kontrolnego genu SREBP1c razem z receptorem jądrowym LXRα, który wyczuwa związki powiązane z cholesterolem. Raz tam, GCN5 dodaje grupy acetylowe do histonu H3, rozluźniając lokalną chromatynę i zwiększając transkrypcję SREBP1c. Efekt ten był wysoce selektywny: GCN5 wzmacniał zdolność LXRα do włączania SREBP1c, ale nie innego celu LXR, ABCA1, który pomaga usuwać cholesterol z tkanek. Bez GCN5 LXRα nie był już w stanie efektywnie zaangażować promotora SREBP1c, a program syntezy tłuszczu ulegał zatrzymaniu.
Kandydat na lek i obiecujące połączenie
Zespół przetestował następnie CPTH2, inhibitor małocząsteczkowy GCN5, który gromadzi się w wątrobie. W modelach mysich już karmionych dietami wysokotłuszczowymi CPTH2 zmniejszał rozmiar wątroby, zawartość tłuszczu i markery uszkodzenia bez oczywistej toksyczności ani zmian w spożyciu pokarmu. W hodowlach ludzkich i mysich komórek wątrobowych CPTH2 obniżał liczbę kropli tłuszczu i trójglicerydów tylko wtedy, gdy obecny był GCN5, co potwierdza specyficzność jego działania. Co ważne, zarówno w komórkach, jak i u myszy leczonych związkami aktywującymi LXR (zaplanowanymi do poprawy usuwania cholesterolu i walki z miażdżycą), CPTH2 selektywnie blokował niepożądany wzrost produkcji tłuszczu napędzanej przez SREBP1c, jednocześnie zachowując geny wspierające transport zwrotny cholesterolu. W połączeniu z agonistą LXR u myszy na diecie wysokotłuszczowej CPTH2 dodatkowo obniżał szkodliwe lipidy krwi i cholesterol w wątrobie oraz zapobiegał nadmiernemu gromadzeniu tłuszczu w wątrobie.
Co to oznacza dla pacjentów
Badanie stawia GCN5 jako centralny czynnik napędzający gromadzenie tłuszczu w wątrobie w MASLD, łącząc sygnały dietetyczne i hormonalne ze włącznikiem produkcji tłuszczu SREBP1c. Ponieważ GCN5 wydaje się być zbędny dla korzystnego ramienia sygnalizacji LXR odpowiedzialnego za oczyszczanie cholesterolu, leki hamujące GCN5 — takie jak CPTH2 lub bardziej zaawansowane następne generacje — mogłyby osłabić stłuszczenie i zapalenie wątroby przy jednoczesnym zachowaniu działania ochronnego wobec serca. Dla osób zagrożonych zarówno chorobą stłuszczeniową wątroby, jak i chorobami sercowo-naczyniowymi, ukierunkowanie tej epigenetycznej dźwigni może kiedyś pozwolić chronić wątrobę bez rezygnacji z korzyści wynikających z poprawy gospodarowania cholesterolem.
Cytowanie: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
Słowa kluczowe: stłuszczeniowa choroba wątroby, epigenetyka, metabolizm lipidów, metabolizm wątroby, receptory jądrowe