Clear Sky Science · pl
Kontrola bez chelatacji w allylacjach ketonów α‑oksy przy użyciu allylatranów grupy 14
Precyzyjniejsze formowanie kształtów molekularnych
Wiele leków i produktów naturalnych działa tylko wtedy, gdy ich atomy są ułożone w odpowiedni, trójwymiarowy sposób. Chemicy w związku z tym wkładają ogromny wysiłek w naukę, jak „dokładać” nowe fragmenty do cząsteczki z jednej lub drugiej strony. Niniejszy tekst opisuje nowy sposób przyłączania grup allylowych — krótkich, trzywęglowych łańcuchów — do powszechnej klasy związków, umożliwiający dostęp do struktur lustrzanych, które do tej pory trudno było otrzymać.
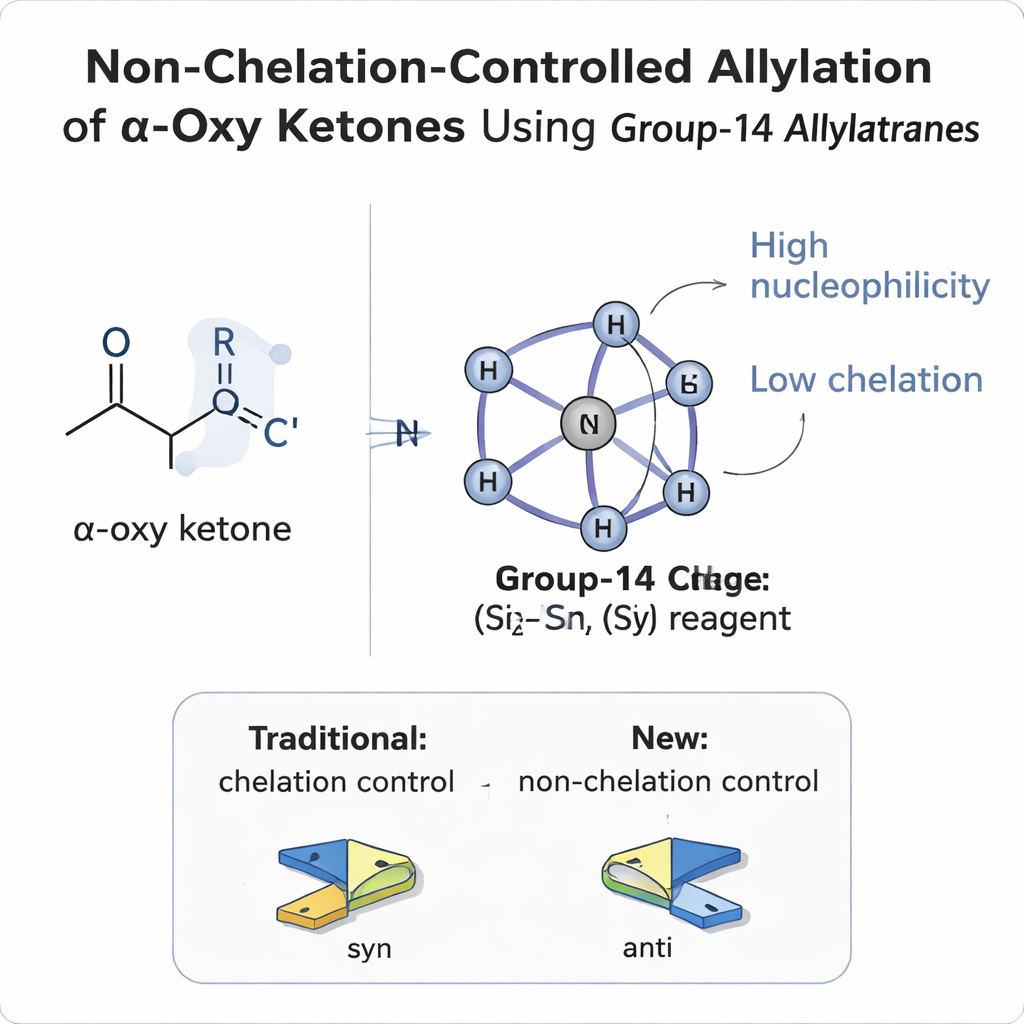
Dlaczego kontrola stron cząsteczki jest tak trudna
Gdy nowa grupa przyłącza się do płaskiego, planarnego wiązania węgiel–tlen (karbonylu), może atakować z dowolnej strony, jak piłka uderzająca monetę z góry lub z dołu. Jeśli przy sąsiadującym węglu (pozycji α) znajduje się już podstawnik, powstają dwie możliwe trójwymiarowe produkty, zwane diastereoizomerami. Przez dziesięciolecia chemicy polegali na prostych modelach — Felkin–Anh, polar Felkin–Anh, Cram i modelach chelatacyjnych — by przewidywać, którą stronę wybierze odczynnik. W związkach karbonylowych α‑oksy, gdzie sąsiadujący podstawnik zawiera tlen (np. eter lub ester), tlen zwykle zachowuje się jak szczypce chwytające odczynniki metaliczne. Ta „chelatacja” blokuje cząsteczkę w określonej konformacji i prawie zawsze prowadzi do tzw. produktów syn, gdzie nowo utworzone grupy alkoholowe znajdują się po tej samej stronie łańcucha węglowego.
Trudny, długoletni problem z sąsiadami tlenowymi
Choć droga przez chelatację jest użyteczna, narzuca ograniczenia: silnie skłania reakcje ku produktom syn i utrudnia otrzymanie przeciwnego ułożenia, anti, w którym dwie grupy hydroksylowe wskazują na przeciwne strony. Dla aldehydów α‑oksy — związków, w których węgiel karbonylowy ma co najmniej jeden atom wodoru — kilka sprytnych trików z użyciem specjalnych odczynników krzemowych i dobrze dobranych kwasów Lewisa pozwoliło uzyskać produkty anti. Jednak w przypadku ketonów α‑oksy, które są mniej reaktywne i powszechniejsze w złożonych celach syntetycznych, wyzwanie jest większe. Silniejsze nukleofile zazwyczaj są bardziej kwasowe Lewisa, co z kolei sprzyja dokładnie tej chelatacji, której chemicy chcą uniknąć. Zrównoważenie „wystarczająco reaktywny” z „niewykluczająco chwytliwy względem tlenu” było i pozostaje centralnym, nierozwiązanym problemem.
Reagent w formie klatki, który łamie regułę
Autorzy przedstawiają nową rodzinę odczynników nazwanych allylatranami, opartą na pierwiastkach grupy 14 — krzemie, germanie i cynie — utrzymanych w sztywnym, klatkowym szkielecie. W tych cząsteczkach wewnętrzny atom azotu sięga przez klatkę, wiążąc się z centralnym atomem, tworząc wysoko skoordynowane, niemal zapakowane centrum metalu. Projekt ten ma dwa kluczowe efekty. Po pierwsze, zwiększa nukleofilowość przyłączonego fragmentu allylowego, czyniąc go chętnym do tworzenia nowego wiązania węgiel–węgiel. Po drugie, łagodzi kwasowość Lewisa centralnego atomu, dzięki czemu mniej skłonny jest on do silnego wiązania z atomami tlenu substratu. Obliczenia kwantowo‑chemiczne i dane z rezonansu magnetycznego jądrowego (NMR) potwierdzają, że ładunek jest zlokalizowany na fragmencie allylowym, podczas gdy komunikacja elektronowa z centrum krzemowym jest ograniczona, co wyjaśnia, jak odczynnik może być jednocześnie silny i niechętny do chelatacji.
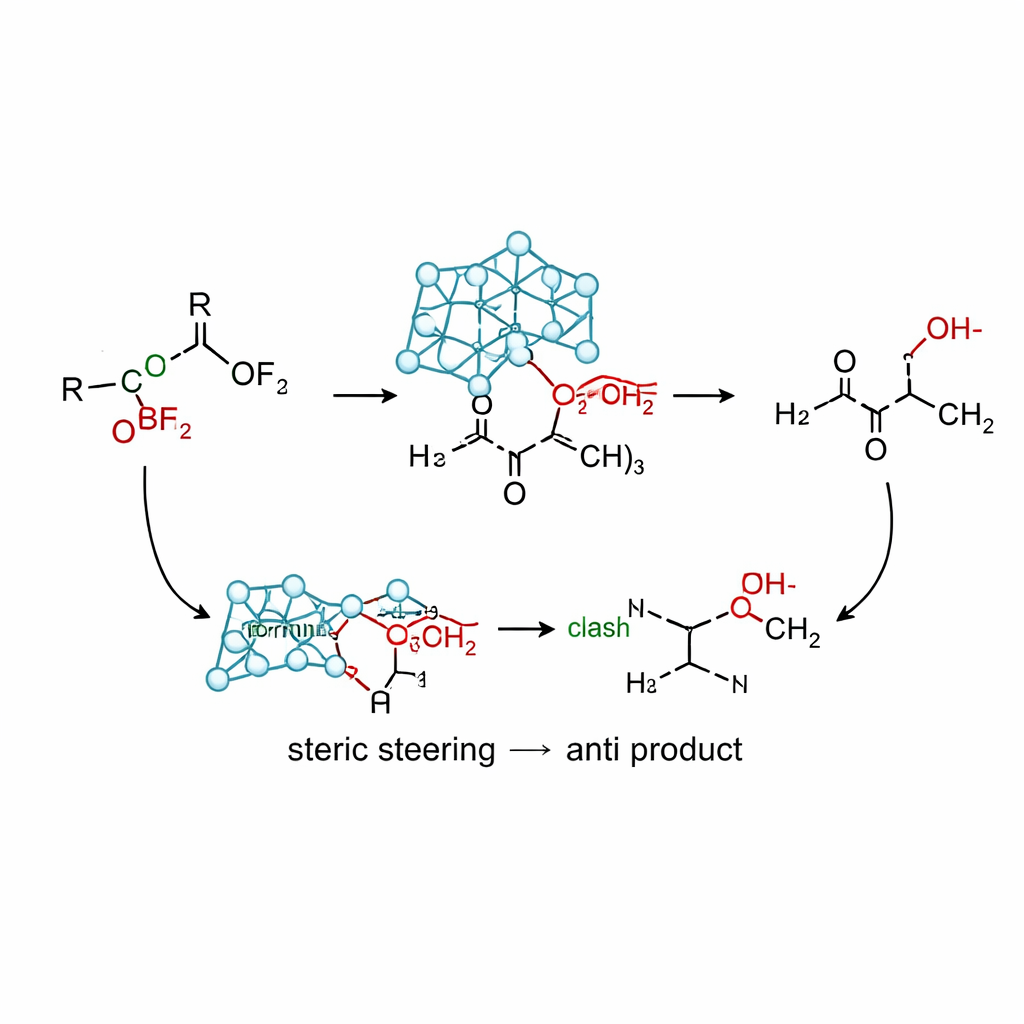
Jak nowa reakcja działa w praktyce
Używając krzemowej wersji tego odczynnika, allylsilatranu, wraz z łagodnym kwasem Lewisa (trifluorkiem boru), zespół opracował warunki dające wysokie wydajności anty‑homoallylicznych alkoholi z szerokiego zakresu ketonów α‑oksy. Eksperymenty porównawcze wykazują, że wiele tradycyjnych źródeł allylu — oparte na cynie, germanie, magnezie, litu i prostych silanach — albo preferuje produkt syn, daje mieszaniny albo ulega rozkładowi. W przeciwieństwie do nich allylsilatran rutynowo dostarcza stosunki anti/syn powyżej 95:5 dla substratów zawierających grupy metoksy, izopropoksy, fenoksy, acetoksy, silyloksy i aminoksy, a także różne pierścienie aromatyczne i ketony cykliczne. Obliczenia sugerują ścieżkę bez chelatacji, w której masywna rama atranowa kieruje podejście fragmentu allylowego do konformacji przypominającej model Cram: podstawnik tlenowy leży naprzeciw karbonylu, podczas gdy odpychanie steryczne między klatką a pobliskimi pierścieniami fenylowymi faworyzuje trajektorię prowadzącą do produktu anti.
Implikacje dla syntezy leków i produktów naturalnych
Metoda sprawdza się także w bardziej sztywnych układach cyklicznych, gdzie objętość allylsilatranu zachęca do ataku z mniej zatłoczonych pozycji, oraz dla wyspecjalizowanych pochodnych przenoszących podstawione grupy allylowe z równie wysoką selektywnością anti. Ponieważ powstałe anti‑1,2‑diole z fragmentem homoallylicznym są powszechnymi motywami w molekułach o aktywności biologicznej, w tym w kandydatach na modulatory enzymów, ta transformacja oferuje chemikom niezawodny sposób dostępu do wariantów strukturalnych, które wcześniej wymagały wieloetapowych obejść lub były po prostu niepraktyczne. Co istotne, te same substraty można ukierunkować na otrzymanie produktów syn lub anti, przełączając się między chelatującym systemem cyny a nowym, niechelatującym systemem silatranu, co daje precyzyjną kontrolę nad kształtem molekularnym.
Co to oznacza w prostych słowach
W istocie badacze zbudowali inteligentne narzędzie do dostarczania grup allylowych, które uderza w docelowy węgiel z „niekorzystnej” strony, nie będąc przy tym złapanym przez pobliskie atomy tlenu. Dzięki starannemu zaprojektowaniu klatki wokół krzemu oddzielili siłę od „lepkości”: odczynnik jest na tyle silny, by zawiązać nowe wiązanie, ale nie tak „lepiący”, by chwytać otaczające atomy i psuć pożądaną geometrię. Dla niespecjalistów oznacza to, że chemicy mają teraz znacznie lepszą kontrolę nad rzeźbieniem trójwymiarowych struktur molekularnych, które leżą u podstaw wielu leków i produktów naturalnych, co poszerza przestrzeń projektową dla przyszłych leków i złożonych cząsteczek syntetycznych.
Cytowanie: Tsutsui, Y., Shiga, K., Konishi, A. et al. Non-chelation control in allylations of α-oxy ketones using group-14 allylatranes. Nat Commun 17, 2019 (2026). https://doi.org/10.1038/s41467-026-69732-2
Słowa kluczowe: stereoselektywna allylacja, ketony alfa‑oksy, allylsilatran, kontrola bez chelatacji, alkohole homoallyliczne