Clear Sky Science · pl
Region N-Myc MB0–MBI wchodzi w specyficzne i dynamiczne interakcje z N-płatkiem kinazy Aurora A
Dlaczego ma to znaczenie dla leczenia raka
Wiele agresywnych nowotworów dziecięcych polega na białku zwanym N-Myc, które utrzymuje wzrost komórek nowotworowych. Samo N-Myc jest trudne do zablokowania lekami, ponieważ zachowuje się bardziej jak wiotka nitka spaghetti niż sztywny zamek, do którego pasuje klucz. W tym badaniu po raz pierwszy szczegółowo pokazano, jak N-Myc wiąże się z innym białkiem, enzymem Aurorą kinazą A (AurA), aby zwiększyć jego aktywność i pomagać komórkom nowotworowym przetrwać. Mapując to partnerstwo, autorzy ujawniają realistyczny sposób na jego rozbicie przy użyciu małych cząsteczek.
Elastyczny sprawca znajduje stałego partnera
N-Myc należy do rodziny MYC — głównych przełączników kontrolujących wzrost, metabolizm i podziały komórkowe. Gdy jest nadmiernie produkowany, te przełączniki stają się potężnymi czynnikami onkogennymi, szczególnie w nowotworach układu nerwowego, takich jak wysokiego ryzyka neuroblastoma u dzieci. W przeciwieństwie do wielu enzymów czy receptorów, N-Myc sam z siebie nie układa się w stałą trójwymiarową formę; jest białkiem „wewnętrznie nieuporządkowanym”, które nieustannie się porusza i zmienia kształt. Ta elastyczność nadaje mu adaptacyjność, ale też sprawia, że jest wyjątkowo trudne do zaadresowania lekami. AurA natomiast jest dobrze zorganizowanym enzymem, który pomaga porządkować podział komórkowy. Wcześniejsze badania wykazały, że AurA stabilizuje N-Myc w komórkach nowotworowych i że oba białka wchodzą w fizyczną interakcję, ale dokładny charakter i znaczenie punktów styku pozostawały niejasne.
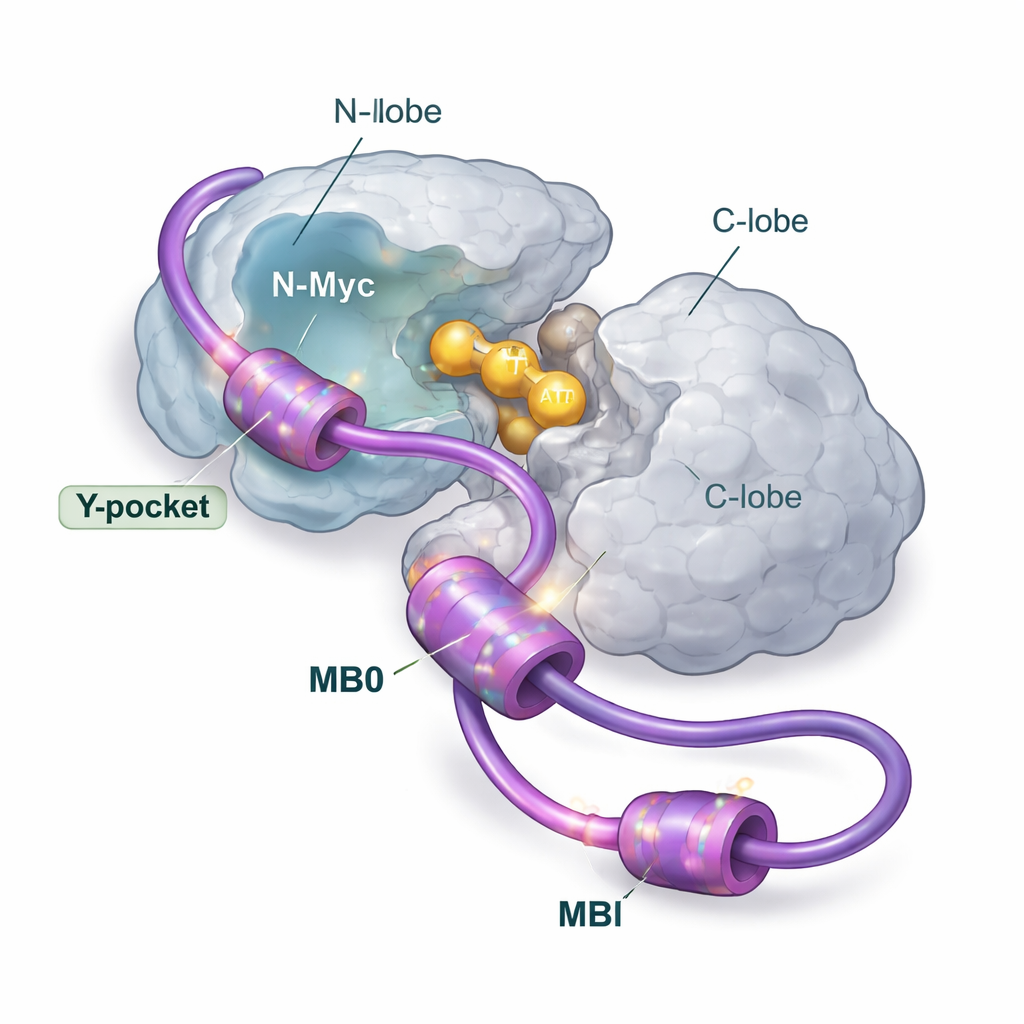
Wiele punktów uchwytu, jeden główny lądowisko
Wykorzystując szeroki zestaw metod strukturalnych i biofizycznych, w tym rezonans magnetyczny jądrowy, rozpraszanie rentgenowskie, spektrometrię mas, kalorimetrię i modelowanie komputerowe, autorzy rozłożyli na czynniki pierwsze sposób, w jaki N-Myc i AurA łączą się w roztworze. Skoncentrowali się na przednim końcu N-Myc, które zawiera dwa zachowane regiony zwane MB0 i MBI. Te krótkie fragmenty są bogate w aromatyczne elementy budulcowe (takie jak fenyloalanina, tyrozyna i tryptofan), które mają skłonność do wnikania w hydrofobowe kieszenie partnerów białkowych. Zespół wykazał, że N-Myc wiąże się z AurA głównie w układzie 1:1, przy czym MB0 i MBI działają jako główne strefy kontaktu. Inny fragment N-Myc, który przyciągał uwagę we wcześniejszych strukturach krystalicznych, okazuje się odgrywać tylko drugorzędną rolę, gdy obecny jest cały region MB0–MBI.
Dynamiczne uściskanie, które włącza enzym
Zamiast wpadać w jeden sztywny układ, N-Myc pozostaje w dużej mierze nieuporządkowany po związaniu z AurA. Dane wskazują na „mętny” kompleks: kilka segmentów N-Myc na zmianę kontaktuje się z różnymi płatkami N-AurA, szczególnie z rowkiem znanym jako kieszeń Y oraz z pobliską pętlą łączącą sygnały z miejscem aktywnym. Pomimo tej luźnej natury efekt jest jasny — wiązanie MB0 i MBI stabilizuje N-płatek AurA i zwiększa jego aktywność kinazy, czyli sprawia, że efektywniej przenosi grupy fosforanowe na swoje cele. Gdy badacze systematycznie zastępowali kluczowe aromatyczne reszty w MB0 i MBI alaniną, kompleks N-Myc–AurA osłabł, enzym był mniej stabilizowany, a jego aktywność spadła. Pokazuje to, że specyficzne aromatyczne „kotwice” w inaczej wiotkim łańcuchu N-Myc są niezbędne do zwiększania aktywności AurA.
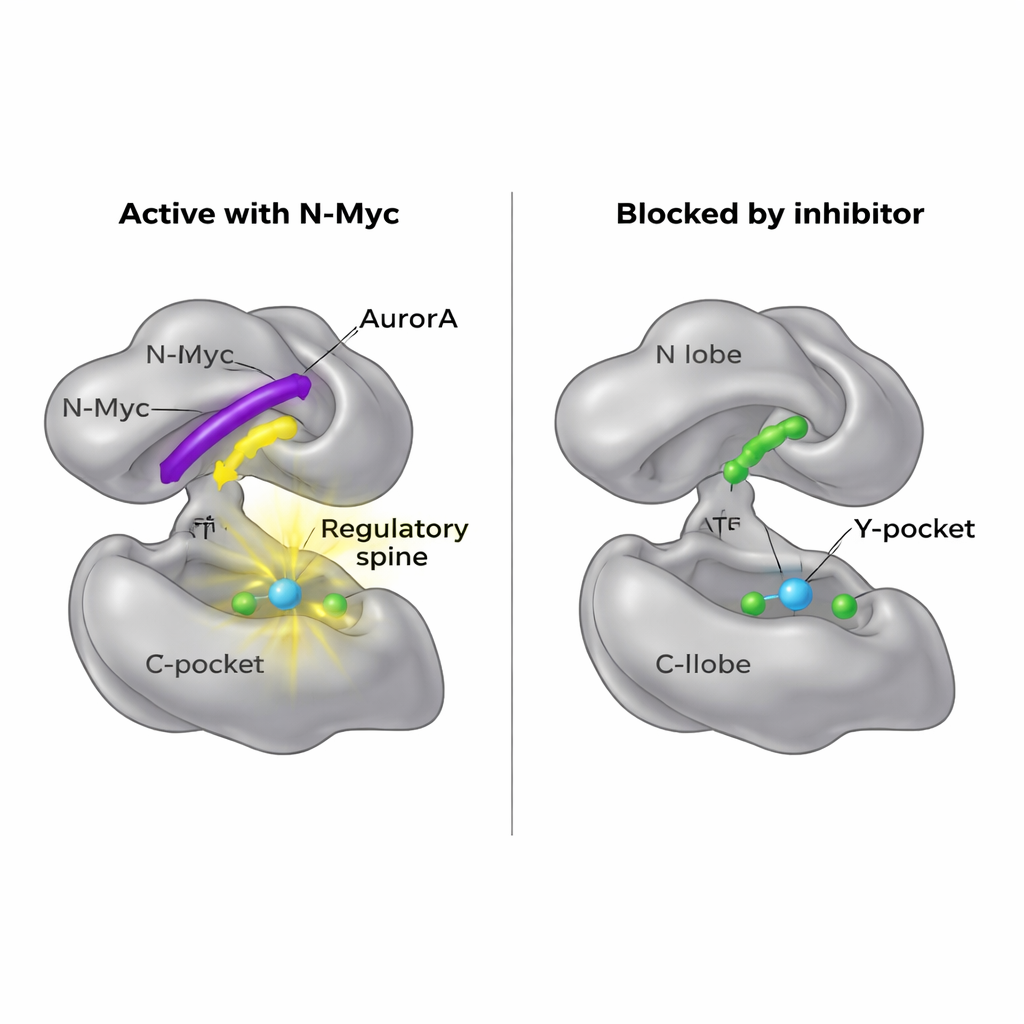
Odkrycie nowego punktu wejścia dla leków
Ponieważ samo N-Myc jest trudne do zaadresowania farmakologicznego, badacze zapytali, czy można zamiast tego zablokować jego punkt dokowania na AurA. Ich mapy strukturalne ujawniły, że MB0 i MBI zajmują ten sam ogólny obszar N-płatka, którego używa inny białkowy partner, TPX2, do aktywacji AurA. Mała cząsteczka nazwana AurkinA jest już znana z tego, że wciska się w kieszeń Y i wypiera TPX2. W eksperymentach wiążących AurkinA skutecznie konkurowała również z N-Myc o N-płatek AurA, uniemożliwiając przyłączenie zarówno fragmentów N-Myc1–69, jak i N-Myc1–100. Wynik ten pokazuje, że powierzchnia N-płatka, a zwłaszcza kieszeń Y, jest podatnym na działanie leku hotspotem, który kontroluje nie tylko klasycznych regulatorów jak TPX2, ale także nieuporządkowane onkoproteiny takie jak N-Myc.
Co to oznacza dla przyszłych terapii
Ta praca przekształca postrzeganie partnerstwa N-Myc–AurA jako dynamicznego, wielopunktowego uścisku skoncentrowanego na N-płatku AurA, zamiast pojedynczego, sztywnego miejsca wiązania. Dla osób niebędących specjalistami kluczowy przekaz jest taki, że nawet bezkształtne białko nowotworowe typu N-Myc można pośrednio zaatakować, celując w stałą płaszczyznę dokującą na jego enzymatycznym partnerze. Pokazując, że istniejące związki wiążące N-płatek mogą wypchnąć N-Myc z AurA, badanie otwiera jasną ścieżkę do leków, które selektywnie zakłócą tę interakcję. Takie związki mogłyby osłabić krytyczne wsparcie dla N-Myc w wysokiego ryzyka nowotworach dziecięcych i, po dalszym rozwoju, zaoferować nową drogę leczenia nowotworów długo uważanych za „nieuleczalne farmakologicznie”.
Cytowanie: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Słowa kluczowe: N-Myc, Aurora kinase A, białka wewnętrznie nieuporządkowane, neuroblastoma, inhibitory interakcji białko–białko