Clear Sky Science · pl
Spatial perturb-seq: genomika funkcjonalna pojedynczych komórek w zachowanej architekturze tkanki
Obserwowanie genów w działaniu w żywych obwodach mózgowych
Wiele chorób mózgu, od choroby Alzheimera po Parkinsona, wiąże się z genami zwiększającymi ryzyko, ale wciąż wiemy niewiele o tym, jak te geny wpływają na pojedyncze komórki w żywym mózgu. W tym badaniu zaprezentowano potężny sposób obserwacji tego, co się dzieje, gdy konkretne geny są wyłączane w pojedynczych komórkach, przy czym komórki te pozostają w swoich naturalnych sąsiedztwach w tkance mózgowej. Podejście nazwane Spatial Perturb-Seq pomaga powiązać ryzyko genetyczne z zaburzeniami zachowania komórek i komunikacji międzykomórkowej w nienaruszonym mózgu.
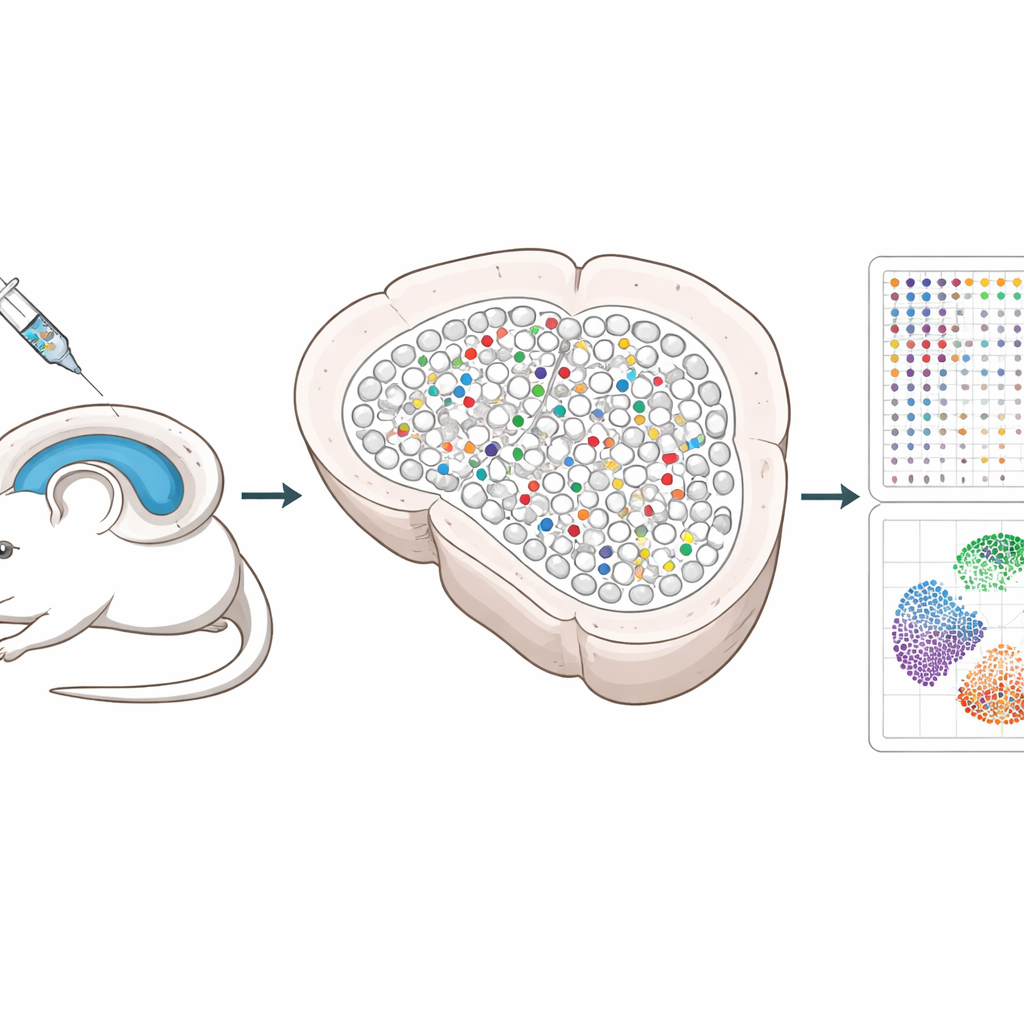
Nowy sposób testowania wielu genów jednocześnie
Naukowcy zbudowali system wykorzystujący narzędzia edycji genów CRISPR dostarczane za pomocą nieszkodliwych wirusów do hipokampa, części mózgu ważnej dla pamięci. Każdy wirus przenosi trzy prowadnice dezaktywujące wybrany gen, a także unikalny „kod kreskowy” DNA i znacznik fluorescencyjny, dzięki czemu zmodyfikowane komórki można potem zlokalizować. Mieszając te wirusy i podając je w niskiej dawce, edytowana zostaje tylko niewielka, rozproszona część komórek, podczas gdy większość sąsiadów pozostaje nietknięta. Ten rzadki wzór pozwala naukowcom odróżnić zmiany zachodzące wewnątrz edytowanych komórek od tych pojawiających się w pobliskich zdrowych komórkach.
Zachowanie mapy mózgu
Tradycyjne metody pojedynczych komórek wymagają rozdrabniania tkanek, co niszczy precyzyjne położenie komórek i może prowadzić do utraty kruchych neuronów. Spatial Perturb-Seq odczytuje aktywność genów bezpośrednio z cienkich skrawków mózgu, dzięki czemu położenie każdej komórki zostaje zachowane. Wykorzystując technologię zwaną Stereo-seq, zespół uchwycił pełne profile ekspresji genów dla ponad 200 000 komórek, jednocześnie odczytując kody CRISPR i zapisując współrzędne każdej komórki w tkance. Następnie użyto zaawansowanych algorytmów obrazowych do obrysowania każdej komórki oraz narzędzi obliczeniowych do identyfikacji typów komórek i lokalnych sąsiedztw, koncentrując się szczególnie na neuronach hipokampa i ich bliskich kontaktach.
Jak edytowane komórki wpływają na swoich sąsiadów
Majac mapę tkanki, naukowcy porównali edytowane neurony z nieedytowanymi neuronami, a oddzielnie z nieedytowanymi sąsiadami otaczającymi każdą edytowaną komórkę. Pozwoliło to rozróżnić efekty „autonomiczne komórkowo” (wewnątrz edytowanej komórki) od efektów „nieautonomicznych komórkowo” (w otaczającym mikrośrodowisku). Wyłączenie 18 różnych genów, wielu powiązanych z ryzykiem chorób neurodegeneracyjnych, wywołało charakterystyczne wzorce zmian ekspresji genów wewnątrz edytowanych neuronów. Niektóre modyfikacje, takie jak te ukierunkowane na gen Cfap410, wywołały także silne przesunięcia aktywności genów w pobliskich komórkach, odzwierciedlając zmienione lokalne sygnalizowanie i wsparcie.
Wskazówki dotyczące szlaków chorób neurodegeneracyjnych
Kilka genów dostarczyło szczególnie interesujących informacji. Wyłączenie Lrrk2, kluczowego genu związanego z ryzykiem choroby Parkinsona, spowodowało duże zmiany w edytowanych neuronach, w tym obniżone poziomy Bc1 — cząsteczki RNA ważnej dla regulacji produkcji białek przy synapsach. Równocześnie komórki sąsiadujące wykazały zmienioną ekspresję genów zaangażowanych w strukturę synaps, transport białek i gospodarkę wapniową, co sugeruje, że problemy związane z Lrrk2 rozchodzą się po lokalnych obwodach. Wyłączenie innego genu, Srf, zaburzyło sieć genów związanych z wzrostem i plastycznością neuronów oraz osłabiło konkretne szlaki sygnałowe ligand–receptor między neuronami, wskazując na zakłóconą komunikację międzykomórkową. Systematycznie punktując te pary sygnałowe, zespół mógł określić, które drogi komunikacji były najbardziej dotknięte dla każdego genu.
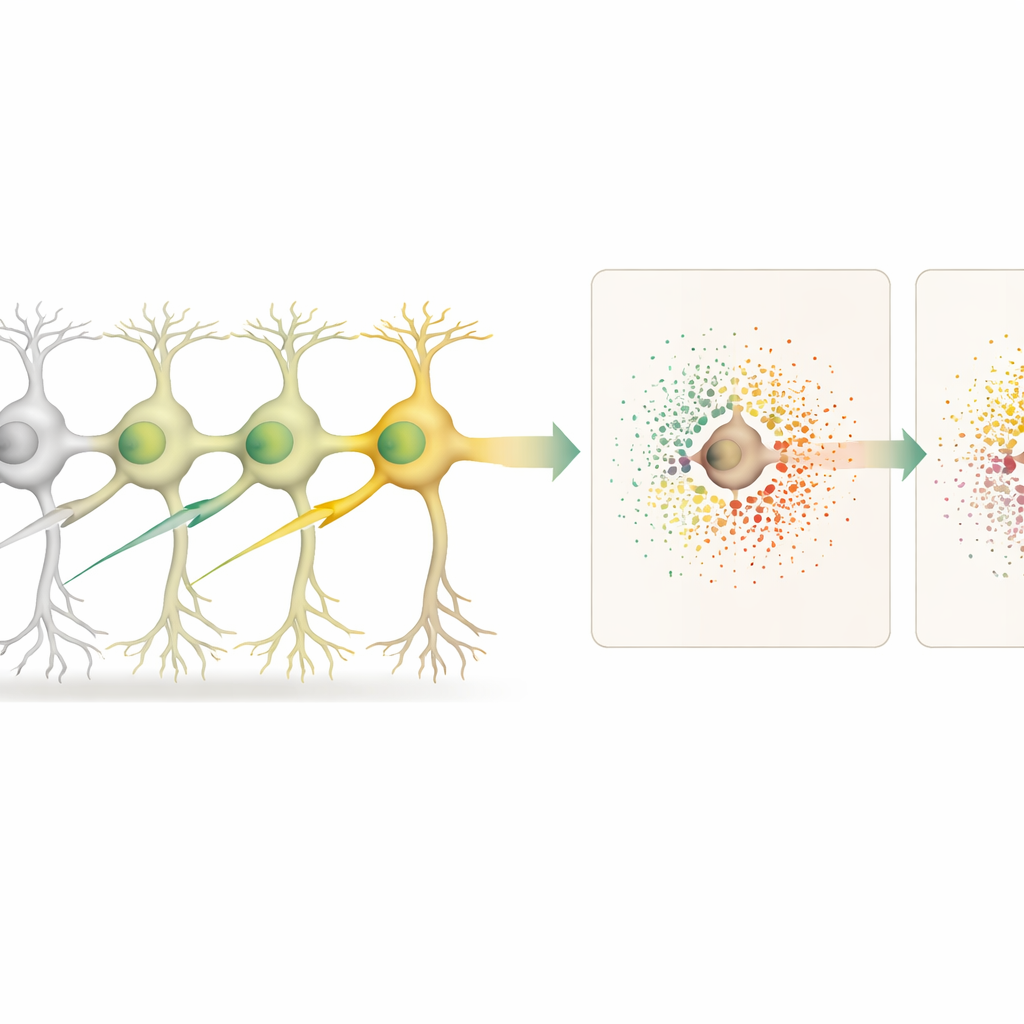
Elastyczne narzędzia do mapowania efektów genetycznych
Aby pokazać, że Spatial Perturb-Seq nie jest uzależnione od jednej platformy, badacze zaadaptowali je także do systemu obrazowania o nazwie Xenium. Tam gotowe panele sond i niestandardowe sondy z kodami kreskowymi odczytują wybrane geny i kody bezpośrednio w tkance. Choć to podejście celowane obejmuje mniej genów niż cały transkryptomowy Stereo-seq, wzorce zmian ekspresji dla kluczowych edycji, takich jak Lrrk2 i Srf, dobrze zgadzały się między obiema metodami i z dużym zewnętrznym atlasem mózgu. To wzajemne sprawdzenie wspiera rzetelność obserwowanych efektów genowych i sąsiedzkich.
Co to oznacza dla badań nad zdrowiem mózgu
Mówiąc wprost, Spatial Perturb-Seq pozwala naukowcom wyłączyć wiele różnych genów w pojedynczych komórkach mózgu, a następnie obserwować, jak te komórki i ich najbliżsi sąsiedzi reagują, przy jednoczesnym zachowaniu mapy połączeń tkanki. Umożliwia to śledzenie, jak czynniki ryzyka genetycznego zaburzają nie tylko pojedyncze komórki, lecz także rozmowy między nimi, które są kluczowe dla prawidłowego funkcjonowania mózgu. Z czasem, wraz z obniżaniem kosztów sekwencjonowania i przeprowadzaniem większych eksperymentów, to podejście może pomóc ujawnić, które geny i lokalne obwody są najważniejsze we wczesnych stadiach schorzeń takich jak Alzheimer, Parkinson czy ALS, wskazując drogi do bardziej precyzyjnych strategii leczenia.
Cytowanie: Shen, K., Seow, W.Y., Keng, C.T. et al. Spatial perturb-seq: single-cell functional genomics within intact tissue architecture. Nat Commun 17, 3018 (2026). https://doi.org/10.1038/s41467-026-69677-6
Słowa kluczowe: genomika przestrzenna, testy CRISPR, sekwencjonowanie pojedynczych komórek, choroby neurodegeneracyjne, komunikacja międzykomórkowa