Clear Sky Science · pl
FLEXTAG: mały i samoodnawialny system znakowania białek do obrazowania super-rozdzielczego w wielu kolorach odporny na blaknięcie
Widzieć to, co niewidoczne wewnątrz komórek
Współczesna biologia w dużej mierze opiera się na obrazowaniu cząsteczek, które podtrzymują życie komórek. Nawet najlepsze mikroskopy optyczne zmagają się jednak z prostym problemem: świetliste markery używane do uwydatniania białek szybko gasną, a oznaczanie wielu różnych celów jednocześnie bez zakłócania funkcji komórek jest trudne. W tym artykule przedstawiono FLEXTAG, nową rodzinę maleńkich, odnawialnych tagów, które świecą znacznie dłużej, obsługują wiele kolorów i działają z najsilniejszymi mikroskopami używanymi do obserwacji wewnętrznej architektury komórek.
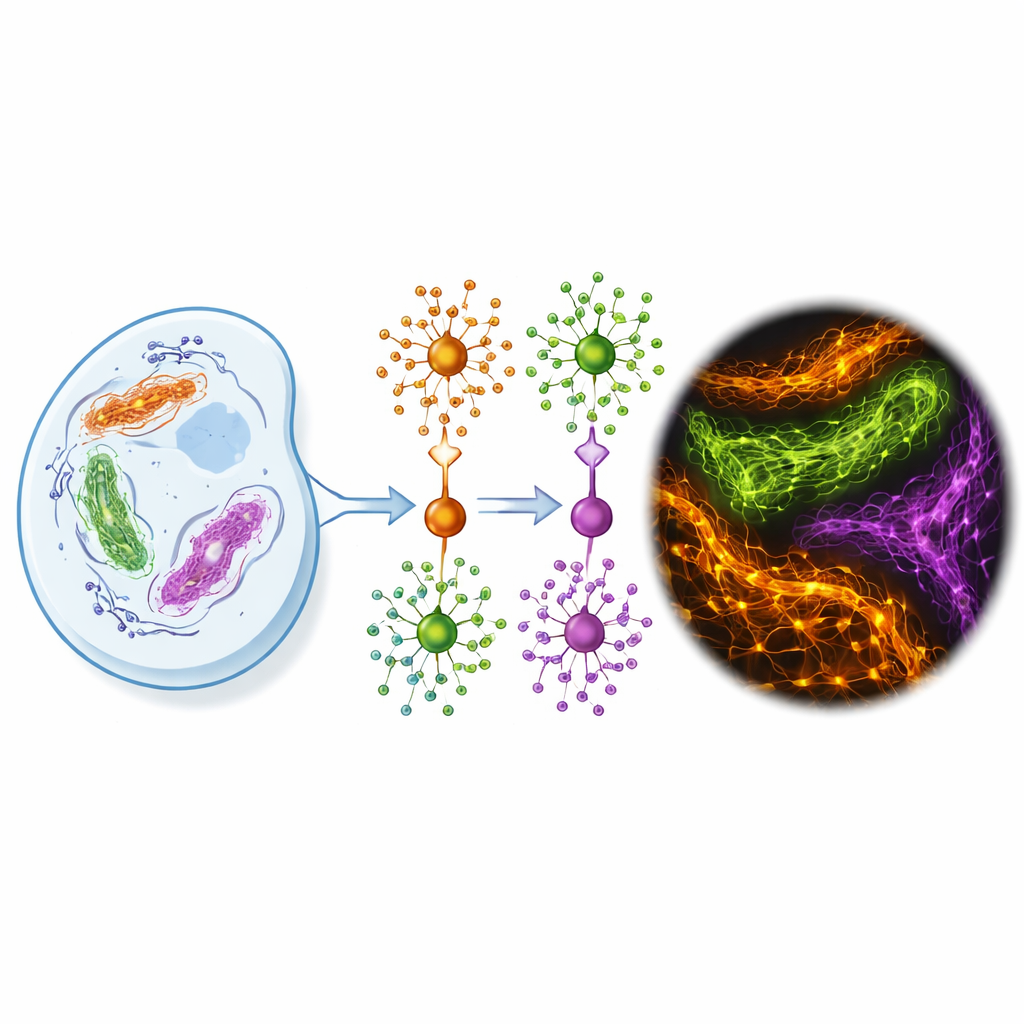
Dlaczego uzyskanie ostrzejszych zdjęć komórek jest tak trudne
Konwencjonalne mikroskopy fluorescencyjne ujawniają struktury o rozmiarze około ćwierci mikrometra, co wciąż jest znacznie większe niż większość pojedynczych białek. Metody super-rozdzielcze wyciskają więcej szczegółów, sięgając do kilku miliardowych części metra, ale tylko wtedy, gdy etykiety fluorescencyjne zachowują się niemal idealnie. Popularne dziś znaczniki białek to albo masywne przeciwciała, słabe białka fluorescencyjne albo chemiczne tagi, których barwniki szybko ulegają degradacji pod wpływem intensywnego światła wymaganego do tych technik. Utrwalanie komórek chemikaliami do szczegółowego obrazowania może też zespalać białka w sposób blokujący dostęp barwników do celów, a luźne cząsteczki barwnika mogą przylegać niespecyficznie, zamazując obraz tłem fluorescencji.
Nowy rodzaj uzupełnialnego tagu białkowego
Autorzy zaprojektowali FLEXTAG (skrót od Fluorescent Labeling for Exchangeable, X-resilient Tagging in Advanced Generic Nanoscopy), aby bezpośrednio sprostać tym ograniczeniom. FLEXTAG to nie pojedynczy tag, lecz skoordynowane trio — FLEXTAG1, FLEXTAG2 i FLEXTAG3 — każdy będący małym, zaprojektowanym białkiem (12–18 kilodaltonów, mniej więcej połowa wielkości klasycznych tagów jak GFP i znacznie mniejszy niż HaloTag). Każdy FLEXTAG wiąże dopasowany ligand małocząsteczkowy niosący jasny barwnik organiczny. Kluczowe jest to, że wiązanie jest odwracalne: cząsteczki barwnik–ligand nieustannie odchodzą i przyłączają się ponownie. Gdy jeden fluorofor ulegnie uszkodzeniu przez światło, świeży z otaczającego roztworu zajmuje jego miejsce, dzięki czemu sygnał skutecznie „samoodnawia się” zamiast stale blednąć.
Budowanie trzech zwartych i niezawodnych tagów
Aby stworzyć FLEXTAG1–3, zespół wykorzystał trzy dobrze znane szkielety białkowe z biologii komórki i projektowania leków, a następnie użył modelowania strukturalnego i testów obrazowych, aby przekształcić ich właściwości. FLEXTAG1 pochodzi od bromodomeny rozpoznającej zmodyfikowaną małą cząsteczkę; autorzy wprowadzili mutacje, które rozbijają skłonność do tworzenia par i agregatów, zachowując jednocześnie silne wiązanie z ligandem. FLEXTAG2 wywodzi się z bakteryjnej dihydrofolatreduktazy. Poprzez dodanie strategicznego mostka disiarczkowego i dopracowanie elastycznych łączników, ustabilizowali białko i dramatycznie zwiększyli odsetek tagów noszących barwnik w danym momencie, przy zachowaniu odwracalnego wiązania. FLEXTAG3 bazuje na ludzkim białku FKBP używanym w chemii biologicznej; tutaj zespół wyważył siłę i szybkość wiązania tak, aby barwniki odłączały się wystarczająco szybko, by mogły być zastąpione, a jednocześnie wiązały wystarczająco mocno, by dawać jasny sygnał i unikać nadmiernej agregacji.
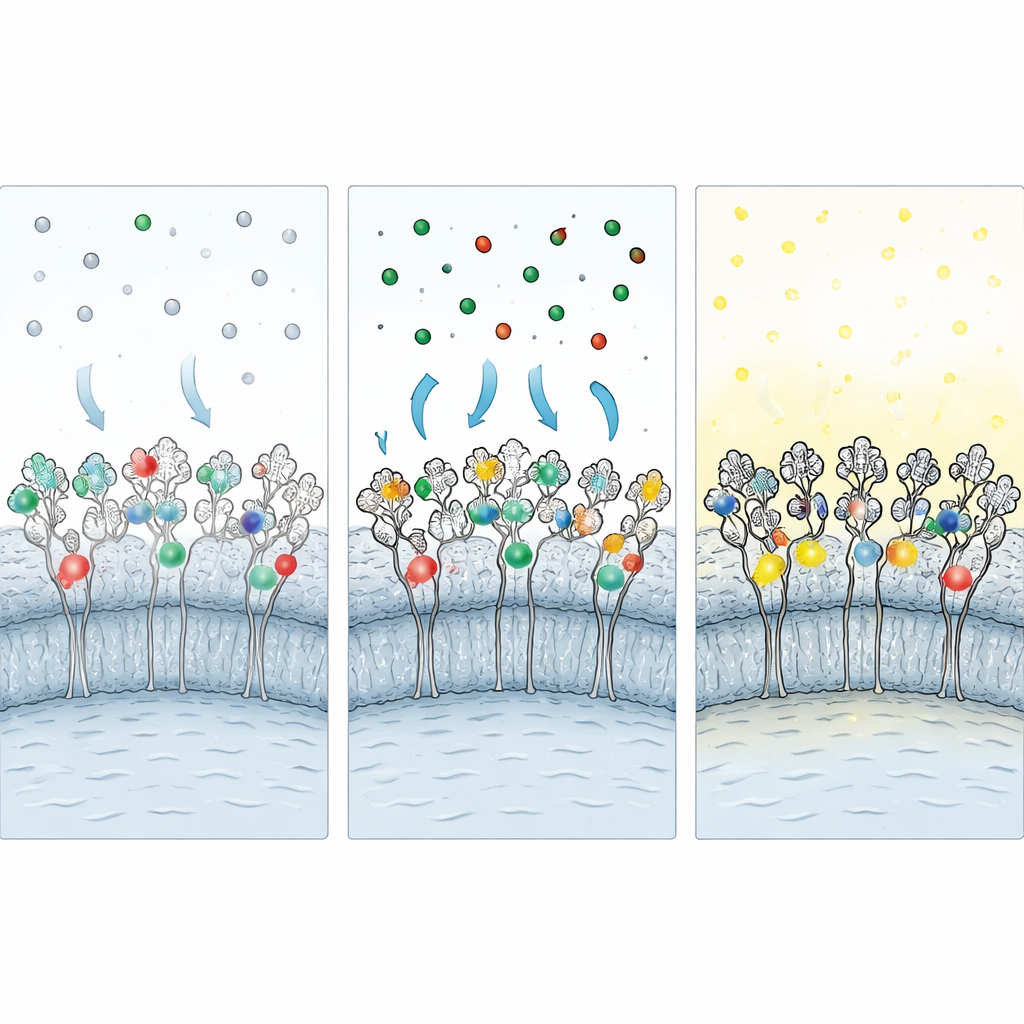
Ochrona tagów podczas utrwalania i zmniejszanie tła
Ponieważ wiele istotnych eksperymentów wymaga obrazowania utrwalonych komórek, badacze opracowali strategię „ochronnego utrwalania”. Przed dodaniem aldehydowych utrwalaczy nasycają żywe komórki niezaznaczonymi wersjami każdego ligandu, zatyczkując kieszeń wiążącą taga. Podczas utrwalania ochronne ligandy osłaniają wrażliwe aminokwasy przed tworzeniem mostków chemicznych. Po utrwaleniu ligandy ochronne są wypłukiwane i zastępowane fluorescencyjnymi, przywracając dostęp do taga. Dodatkowe kroki — redukcja chemiczna w celu zneutralizowania pozostałych grup reaktywnych oraz koktajl blokujący zawierający albuminę, detergent i sól chaotropową — dalsze ograniczają lepienie się i niespecyficzne wiązanie wolnych barwników. Razem te zabiegi zachowują około 60–70% znakowania obserwowanego w komórkach żywych, jednocześnie wyraźnie poprawiając stosunek sygnału do szumu.
Ostrzejsze, dłużej trwające filmy przy różnych metodach
Z ramą FLEXTAG autorzy przetestowali ją w głównych rodzinach mikroskopii super-rozdzielczej. W metodach z modulowanym oświetleniem, takich jak SIM i STED, FLEXTAGi umożliwiły obrazowanie wielokolorowe mitochondriów, mikrotubul, siateczki śródplazmatycznej i aktyny z dużo mniejszym blednięciem niż standardowe tagi kowalencyjne; w ciągu dziesiątek cykli obrazowania sygnał z konwencjonalnych tagów spadał o połowę lub więcej, podczas gdy sygnały FLEXTAG pozostawały niemal stałe. W metodach pojedynczych cząsteczek, takich jak PAINT i STORM, szybka wymiana ligandów FLEXTAG dawała bogłe, stabilne strumienie lokalizacji, które dało się przekształcić w trójwymiarowe, wielokolorowe mapy struktur podkomórkowych, nawet w komórkach żywych przez wiele minut. FLEXTAG2 wykazał szczególnie korzystne kinetyki dla PAINT, podczas gdy FLEXTAG3 wyróżniał się w długotrwałych filmach STORM. Ponieważ tagi są ortogonalne względem siebie i kompatybilne z szeroką paletą barwników, naukowcy mogą znakować kilka białek naraz, a następnie wybrać tryb obrazowania najlepiej pasujący do ich pytania bez zmiany podstawowych konstrukcji.
Co to oznacza dla obserwacji wnętrza komórek
FLEXTAG oferuje rodzaj uniwersalnego, uzupełnialnego łącza między białkami a jasnymi barwnikami. Jego niewielki rozmiar zmniejsza ryzyko, że tag zaburzy lokalizację lub funkcję białka, a samoodnawiające się barwniki pomagają obejść długoletni problem fotoblegnięcia w mikroskopach dużej mocy. Łącząc te tagi ze strategią ochronnego utrwalania i chemią tłumiącą tło, badacze mogą uzyskać czyściejsze, dłużej trwające i bardziej kolorowe obrazy rozmieszczenia i ruchu białek w komórkach. W praktyce oznacza to lepsze mapy architektury komórkowej, bardziej wiarygodne śledzenie interakcji molekularnych w czasie oraz wszechstronny zestaw narzędzi, który powinien przynieść korzyści zarówno podstawowej biologii komórki, jak i badaniom translacyjnym bazującym na obserwowaniu zmian związanych z chorobami w nanoskali.
Cytowanie: Zhang, H., Yao, Y., Wang, X. et al. FLEXTAG: a small and self-renewable protein labeling system for anti-fading multi-color super-resolution imaging. Nat Commun 17, 2156 (2026). https://doi.org/10.1038/s41467-026-69658-9
Słowa kluczowe: mikroskopia super-rozdzielcza, znakowanie białek fluorescencyjnych, obrazowanie komórek żywych, odporność na fotoblegnięcie, architektura komórkowa