Clear Sky Science · pl
Wydajne przetwarzanie metanolu na glikol etylenowy i gliceraldehyd przez rozbieżne sprzęganie C−C
Przekształcanie prostego paliwa w użyteczne cegiełki budulcowe
Metanol, prosty alkohol, który można wytworzyć z dwutlenku węgla, gazu ziemnego, węgla lub biomasy, jest już ważnym paliwem i surowcem chemicznym. Badanie pokazuje, jak wiązki światła i starannie zaprojektowane nanomateriały mogą przekształcać metanol w bardziej złożone, wartościowsze cząsteczki — jednocześnie uwalniając wodór jako nośnik czystej energii. Praca ujawnia nowy sposób sterowania jednym surowcem wyjściowym tak, by prowadził do dwóch różnych użytecznych produktów, po prostu zmieniając ułożenie pojedynczych atomów metalu na maleńkiej powierzchni katalizatora. 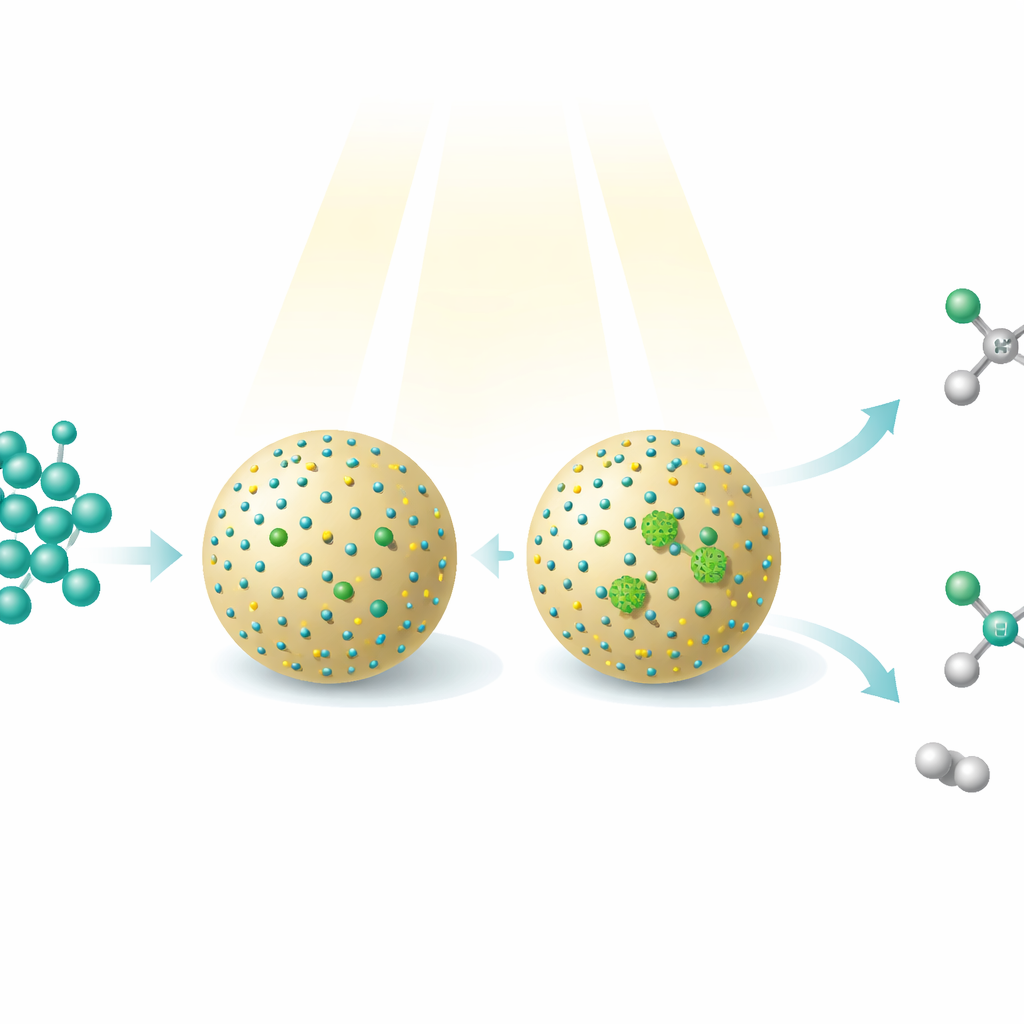
Dlaczego modernizacja metanolu ma znaczenie
W miarę jak świat poszukuje alternatyw dla ropy naftowej, metanol wyrasta na atrakcyjny płyn zdolny magazynować energię i węgiel. Jednak większość procesów przemysłowych zamieniających metanol w większe molekuły to narzędzia dosyć brutalne: wymagają wysokich temperatur, opierają się na drogach kopalnych i często generują wiele niepożądanych produktów ubocznych. Chemicy chcieliby łączyć cząsteczki metanolu z dużą precyzją, aby selektywnie otrzymywać tylko pożądane związki. Przeprowadzanie tego w łagodnych warunkach przy użyciu światła zamiast ciepła ułatwiłoby integrację produkcji chemicznej z odnawialnymi źródłami energii.
Aktywowane światłem nanosfery wykonują pracę
Naukowcy zbudowali fotokatalizator — dosłownie katalizator napędzany światłem — poprzez naniesienie maleńkich kropek siarczku kadmu (kropki kwantowe) na sferyczne cząstki krzemionki. Te kropki kwantowe pochłaniają światło i tworzą energetyczne elektrony i dziury, które mogą odrywać atomy wodoru od metanolu, tworząc wysoce reaktywne fragmenty. Następnie na kropki kwantowe osadzono atomy niklu na dwa różne sposoby. W jednym materiale nikiel występował głównie jako izolowane pojedyncze atomy; w drugim nikiel tworzył bardzo małe skupiska kilku atomów. Choć ogólny skład zmienił się nieznacznie, ta subtelna różnica w rozmieszczeniu niklu dramatycznie zmieniła, które reakcje zachodziły na powierzchni.
Dwa projekty niklu, dwa czyste produkty
Gdy katalizator z pojedynczymi atomami niklu był wystawiony na działanie światła w metanolu, sprzyjał parowaniu dwóch identycznych fragmentów pochodzących z metanolu, prowadząc głównie do glikolu etylenowego — dwuwęglowego diolu szeroko stosowanego w płynach przeciwzamarzaniowych i tworzywach. Ta ścieżka osiągnęła około 90% selektywności, co oznacza, że niemal cały przekształcony metanol kończył jako ten jeden produkt, podczas gdy gazowy wodór był wytwarzany w odpowiadającej ilości z usuniętych atomów wodoru. Dla porównania, katalizator ze skupiskami niklu kierował te same fragmenty metanolu inną drogą. Tutaj część metanolu ulegała dalszej utlenianiu do krótkotrwałego, podobnego do formaldehydu pośrednika, który następnie łączył się z innym fragmentem, tworząc gliceraldehyd — inny dwuwęglowy związek o wielu zastosowaniach w chemii specjalnej i potencjalnie w procesach biobazowanych. Ta ścieżka dostarczyła gliceraldehydu z 96% selektywnością, również wraz z wodorem. Nośnik z krzemionki pomagał kropkom kwantowym efektywniej zbierać światło i czynił cząstki bardziej trwałymi przez wiele cykli użycia. 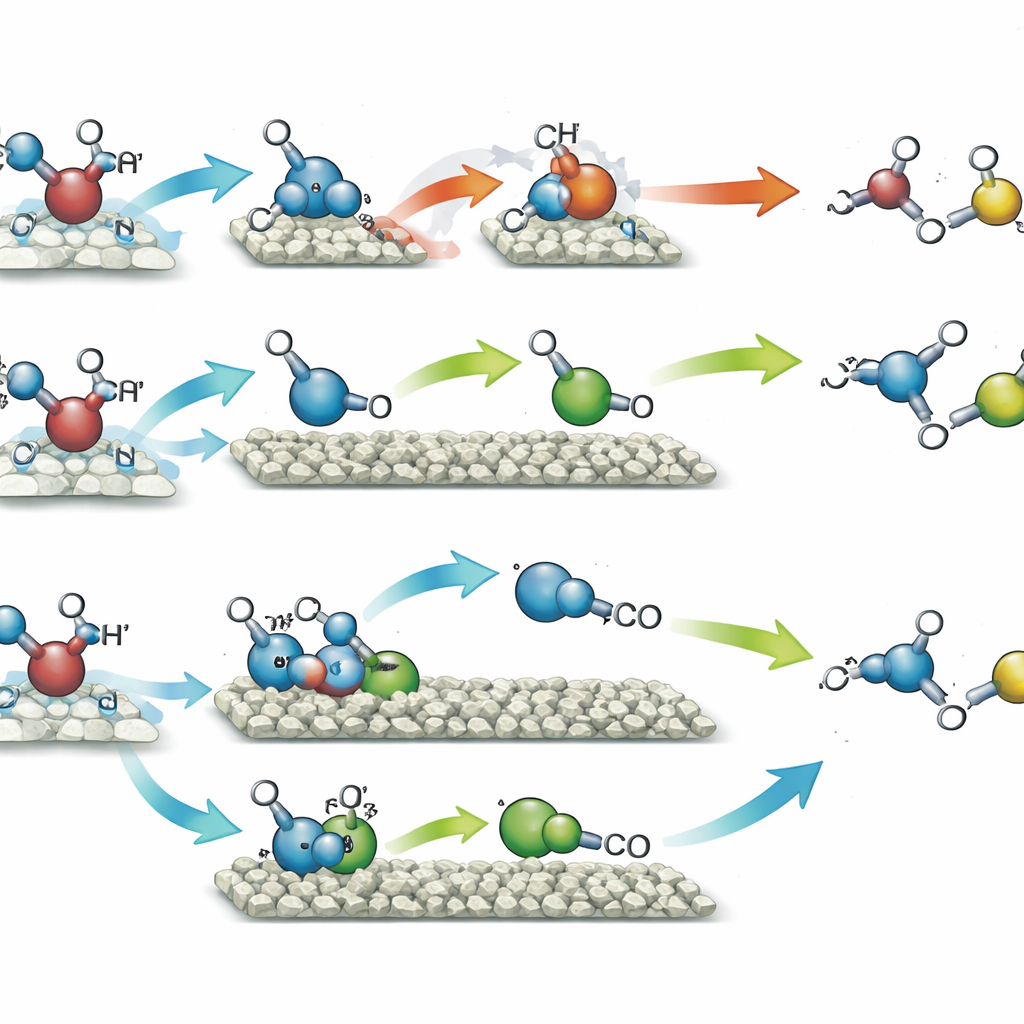
Zajrzeć pod maskę reakcji
Aby zrozumieć, dlaczego dwa rozmieszczenia niklu zachowywały się tak odmiennie, zespół połączył zestaw zaawansowanych pomiarów z symulacjami komputerowymi. Eksperymenty spektroskopii rezonansu paramagnetycznego elektronów pokazały, że oba katalizatory generowały pod wpływem światła rodniki pochodzące z metanolu, ale katalizator ze skupiskami sprzyjał również pękaniu wiązania tlen–wodór, prowadząc do bardziej różnorodnych fragmentów reakcyjnych i do pośrednika podobnego do formaldehydu. Testy z rozdzielczością czasową potwierdziły, że stężenie tego pośrednika najpierw rosło, a potem malało w miarę jego zużywania do tworzenia gliceraldehydu. Obliczenia kwantowo-chemiczne odwzorowały koszty energetyczne każdego małego kroku. Na pojedynczych atomach niklu bezpośrednie sprzęgnięcie dwóch identycznych rodników do utworzenia glikolu etylenowego było najłatwiejszą drogą. Na skupiskach niklu to samo sprzęgnięcie zbyt mocno wiązało produkt, utrudniając jego uwolnienie, podczas gdy ścieżka prowadząca najpierw przez asymetryczny pośrednik, a następnie do gliceraldehydu stała się preferowana energetycznie.
Nowa dźwignia dla czystszej produkcji chemicznej
Mówiąc prościej, praca ta pokazuje, że „gdzie” każdy atom niklu siedzi na powierzchni o rozmiarach nanometrów może zadecydować „co” z metanolu powstanie pod wpływem światła. Przełączając się między pojedynczymi atomami a małymi skupiskami niklu, naukowcy mogą zmieniać główny produkt z glikolu etylenowego na gliceraldehyd, oba otrzymywane wydajnie i czysto wraz z paliwem w postaci wodoru. Ta strategia projektowania katalizatorów atom po atomie oferuje obiecującą drogę do podnoszenia wartości prostych, odnawialnych surowców takich jak metanol do różnych użytecznych chemikaliów bez opierania się na ropie, surowych warunkach czy marnotrawnych reakcjach ubocznych.
Cytowanie: Qi, MY., Tan, CL., Tang, ZR. et al. Efficient methanol upcycling to ethylene glycol and glycolaldehyde via divergent C−C coupling synthesis. Nat Commun 17, 2835 (2026). https://doi.org/10.1038/s41467-026-69656-x
Słowa kluczowe: przekształcanie metanolu, fotokataliza, pojedyncze atomy niklu, glikol etylenowy, gliceraldehyd