Clear Sky Science · pl
Inżynieria genowa mikrośrodowiska guza indukowana przez LOAd703 w połączeniu z atezolizumabem w przerzutowym czerniaku złośliwym: badanie fazy I/II
Dlaczego to nowe badanie nad czerniakiem ma znaczenie
Dla osób z zaawansowanym czerniakiem skóry, który przestał reagować na obecne, skuteczne immunoterapie, opcje leczenia są ograniczone i często obciążające. To badanie sprawdza inne podejście: wstrzyknięcie do guzów wirusa zmodyfikowanego genetycznie, razem z istniejącym lekiem wzmacniającym odpowiedź immunologiczną, aby pobudzić obronę organizmu i odzyskać kontrolę nad rakiem. Wstępne wyniki sugerują, że tę terapię można stosować bezpiecznie i że może pomóc znaczącej grupie pacjentów, których choroba wcześniej była oporna na standardowe leczenie.
Uparty nowotwór skóry, który przechytrza leczenie
Czerniak jest jednym z najczęstszych poważnych nowotworów skóry w krajach zachodnich, a jego zapadalność gwałtownie wzrosła w ostatnich dekadach. Nowoczesne leki odblokowujące punkty kontrolne—które znoszą hamowanie limfocytów T—zrewolucjonizowały rokowania, podnosząc pięcioletnie przeżycie w zaawansowanym czerniaku do około połowy pacjentów. Mimo to wiele guzów z czasem przestaje odpowiadać. Często te oporne nowotwory otoczone są „zimnym” mikrośrodowiskiem komórek i cząsteczek, które blokuje napływ komórek odpornościowych lub je wycisza. Znalezienie sposobów przekształcenia tego mikrośrodowiska guza tak, aby limfocyty T mogły ponownie rozpoznawać i atakować nowotwór, jest jednym z głównych priorytetów badań.
Wirus zaprojektowany, by przestawić sąsiedztwo guza
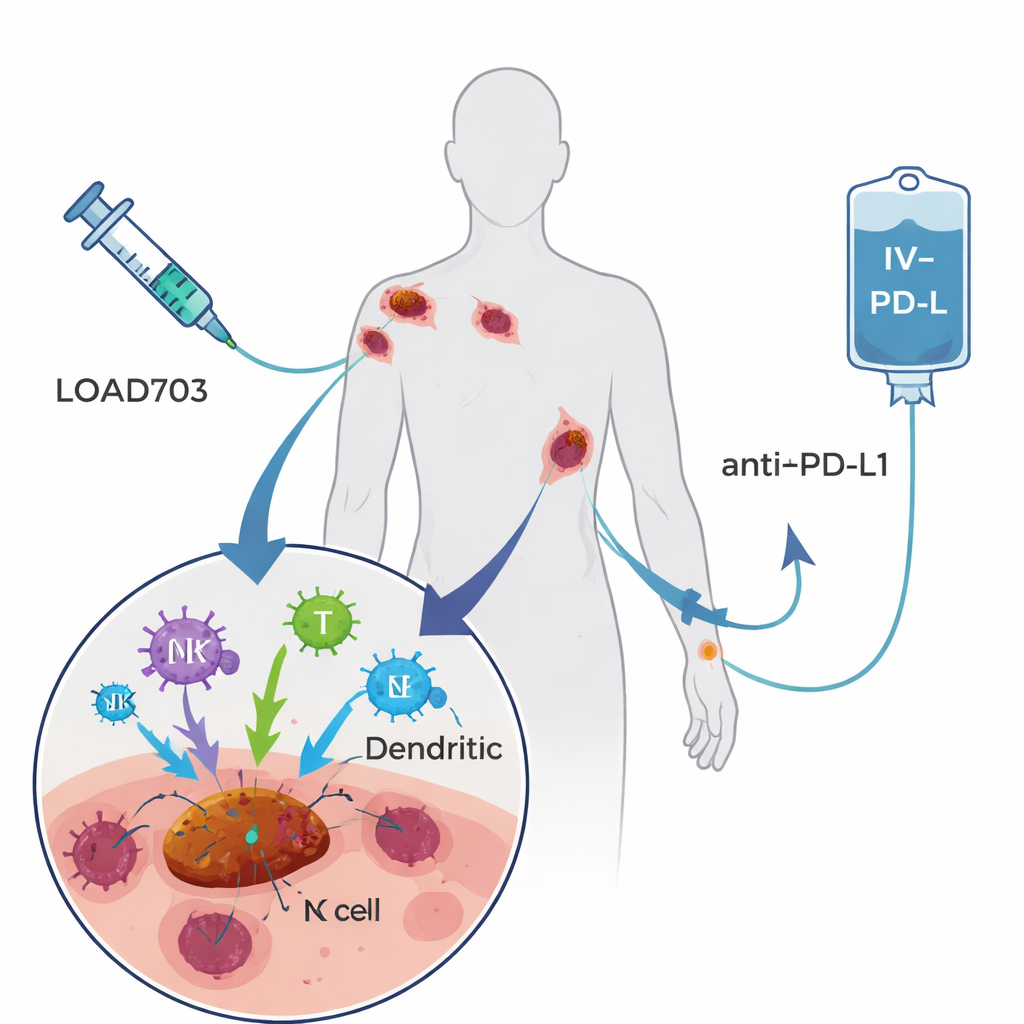
Leczenie testowane tu, nazwane LOAd703, to zmodyfikowany adenowirus—rodzaj wirusa przeziębienia—zaprojektowany do wykonywania dwóch zadań. Po pierwsze, preferencyjnie replikuje się w komórkach nowotworowych i je niszczy, co jest strategią znaną jako onkolityczna wirusoterapia. Po drugie, przenosi instrukcje genetyczne dla dwóch silnych sygnałów stymulujących układ odpornościowy umieszczonych na zakażonych komórkach. Te sygnały, CD40L i 4-1BBL, pomagają dojrzeć profesjonalnym strażnikom immunologicznym (komórkom dendrytycznym) i prezentować fragmenty guza oraz wzmacniają i poszerzają populacje limfocytów T i komórek NK walczących z rakiem. Pacjenci w badaniu otrzymywali LOAd703 wstrzykiwany bezpośrednio do jednego lub kilku guzów co trzy tygodnie, razem z atezolizumabem—ustanowionym przeciwciałem podawanym dożylnie, które blokuje hamulec PD-L1 na limfocytach T. Nadzieja polegała na tym, że wirus zamieni guzy w fabryki szczepionek wewnątrz organizmu, podczas gdy przeciwciało utrzyma ponownie ożywione limfocyty T w aktywności.
Kto był leczony i jak się to skończyło
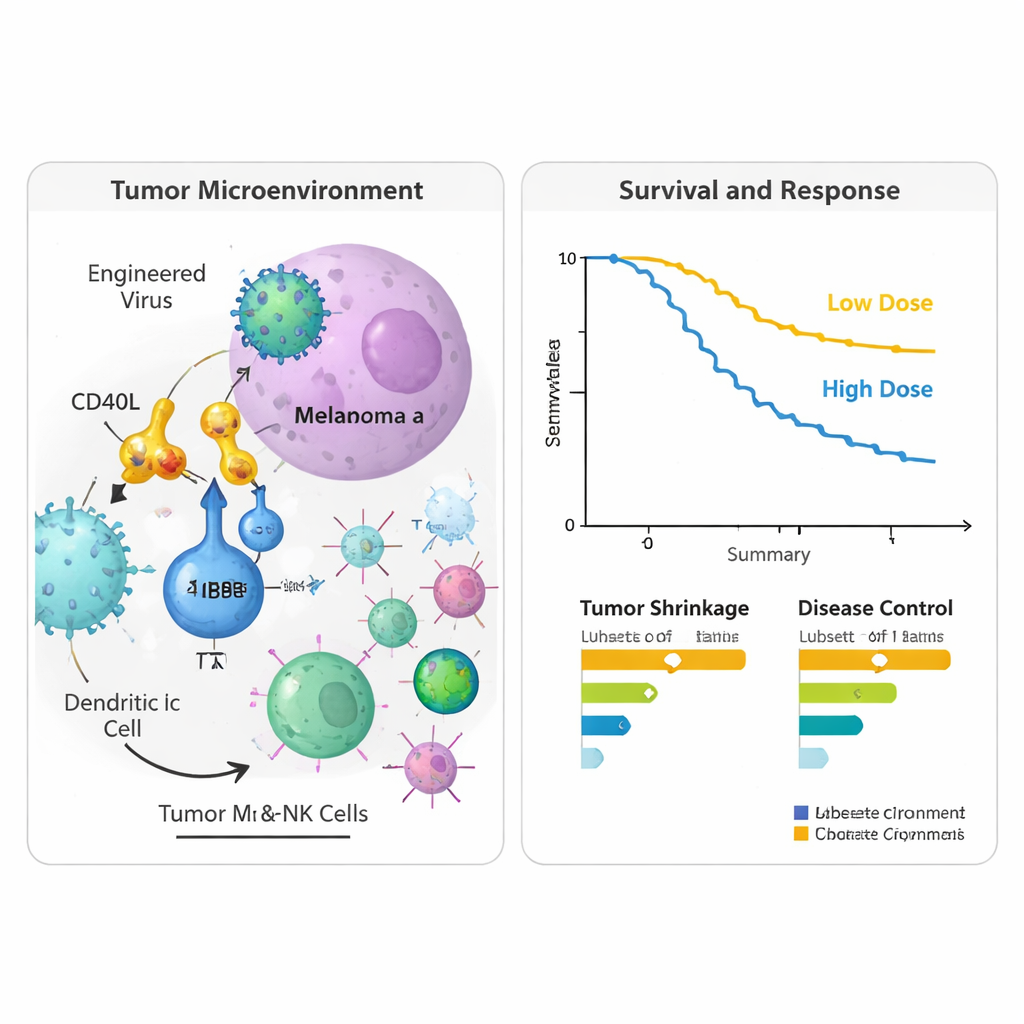
Badanie fazy I/II zrekrutowało 24 osoby ze stadium IV czerniaka, u których choroba wyraźnie postępowała pomimo przynajmniej jednego wcześniejszego leczenia blokującego PD-1; wielu pacjentów otrzymało kilka linii immunoterapii i leków celowanych. Testowano dwa poziomy dawki wirusa. Ogólnie kombinacja była dobrze tolerowana. Najczęstsze działania niepożądane powiązane z wirusem—gorączka, dreszcze, nudności i objawy przypominające grypę—były przeważnie łagodne i przemijające. Tylko u dwóch pacjentów wystąpiły poważniejsze, lecz odwracalne reakcje przy wyższej dawce, i nikt nie musiał przerwać leczenia z powodu problemów związanych z wirusem. Gdy badacze oceniali odpowiedzi guza, u czterech pacjentów (17%) stwierdzono mierzalne zmniejszenie nowotworów, a ponad połowa miała przynajmniej czasową stabilizację choroby. Po dwóch latach od wejścia do badania niemal połowa uczestników nadal żyła, w tym niektórzy, u których badania obrazowe wykazały długotrwałą kontrolę lub całkowite ustąpienie wykrywalnej choroby po zakończeniu terapii.
Sygnaly, że układ odpornościowy został ponownie zaangażowany
Aby sprawdzić, co działo się wewnątrz guzów i we krwi, zespół przeanalizował biopsje tkanki i próbki krwi pobrane przed leczeniem i około dziewięć tygodni po jego rozpoczęciu. W wstrzykniętych guzach zaobserwowano wyższą aktywność genów związanych z odpowiedzią immunologiczną typu 1, w tym markerów aktywowanych limfocytów T i komórek NK, oraz cząsteczek ułatwiających tym komórkom wnikanie do guzów z pobliskich naczyń krwionośnych. Zwiększyły się także sygnały związane z prezentacją antygenu—procesem, w którym fragmenty guza są prezentowane limfocytom T—co sugeruje, że terapia wirusowa przekształcała mikrośrodowisko guza ze stłumiającego w bardziej przyjazne dla układu odpornościowego. We krwi kilka białek związanych z odpornością, w tym sam PD-L1, wzrosło po terapii, zgodnie z szeroką aktywacją szlaków immunologicznych. Pacjenci, którzy żyli dłużej, mieli tendencję do wykazywania wzorców genowych związanych z silną funkcją limfocytów T i ochroną przeciwwirusową, podczas gdy u osób z krótszym przeżyciem dominowały wzorce powiązane z typami komórek o działaniu supresyjnym i sygnałami przebudowy tkanek.
Co to może oznaczać dla przyszłej opieki
Było to małe, jednokierunkowe badanie bez grupy porównawczej, dlatego dane dotyczące przeżycia i odpowiedzi należy interpretować ostrożnie. Mimo to kombinacja dobrej tolerancji, aktywacji immunologicznej w guzach i zachęcającej kontroli choroby u pacjentów silnie wcześniej leczonych sugeruje, że genetycznie zmodyfikowane wirusy onkolityczne, takie jak LOAd703, mogą pomóc ponownie uczulić czerniaka na blokadę punktów kontrolnych—oraz nawet samodzielnie utrzymywać guzy pod kontrolą. Wyniki uzasadniają większe, kontrolowane badania, potencjalnie łączące wirusa z dodatkowymi lekami ukierunkowanymi na układ odpornościowy, aby wyjaśnić, którzy pacjenci odnoszą największe korzyści i jak najlepiej włączyć tę strategię do terapii czerniaka.
Cytowanie: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Słowa kluczowe: czerniak, immunoterapia, wirus onkolityczny, mikrośrodowisko guza, oporność na inhibitory punktów kontrolnych