Clear Sky Science · pl
Leki zakleszczone w prolekach umożliwiają fotokatalityczne podwójne uwalnianie tlenku azotu i środków znieczulających dla przeciwbakteryjnej analgezji
Walka z drobnoustrojami i bólem jednocześnie
Infekcje bakteryjne nie tylko zagrażają zdrowiu; powodują też silny ból. Standardowe terapie zwykle atakują same bakterie, a pacjenci polegają dodatkowo na lekach przeciwbólowych, które mogą działać krótko lub wywoływać skutki uboczne. W tym badaniu przedstawiono lek kontrolowany światłem, który ma na celu jednoczesne zabijanie bakterii i łagodzenie bólu w jednym skoordynowanym kroku, oferując wizję bardziej inteligentnej i wygodnej opieki nad zakażeniami.
Koncepcja leku dwa w jednym
Naukowcy oparli podejście na tetrakainie, znanym miejscowym środku znieczulającym używanym do znieczulenia skóry i nerwów. Chemicznie przyłączyli do tetrakainy tlenek azotu, małą cząsteczkę gazu znaną z silnych właściwości przeciwbakteryjnych i przeciwzapalnych, tworząc prolek o nazwie TTC-NO, który jest w dużej mierze nieaktywny dopóki nie zostanie aktywowany. TTC-NO zapakowano następnie wraz z światłoczułym pomocnikiem do drobnych polimerowych pęcherzyków zwanych micelami, które mogą poruszać się w środowiskach wodnych, takich jak krew czy płyn tkankowy. 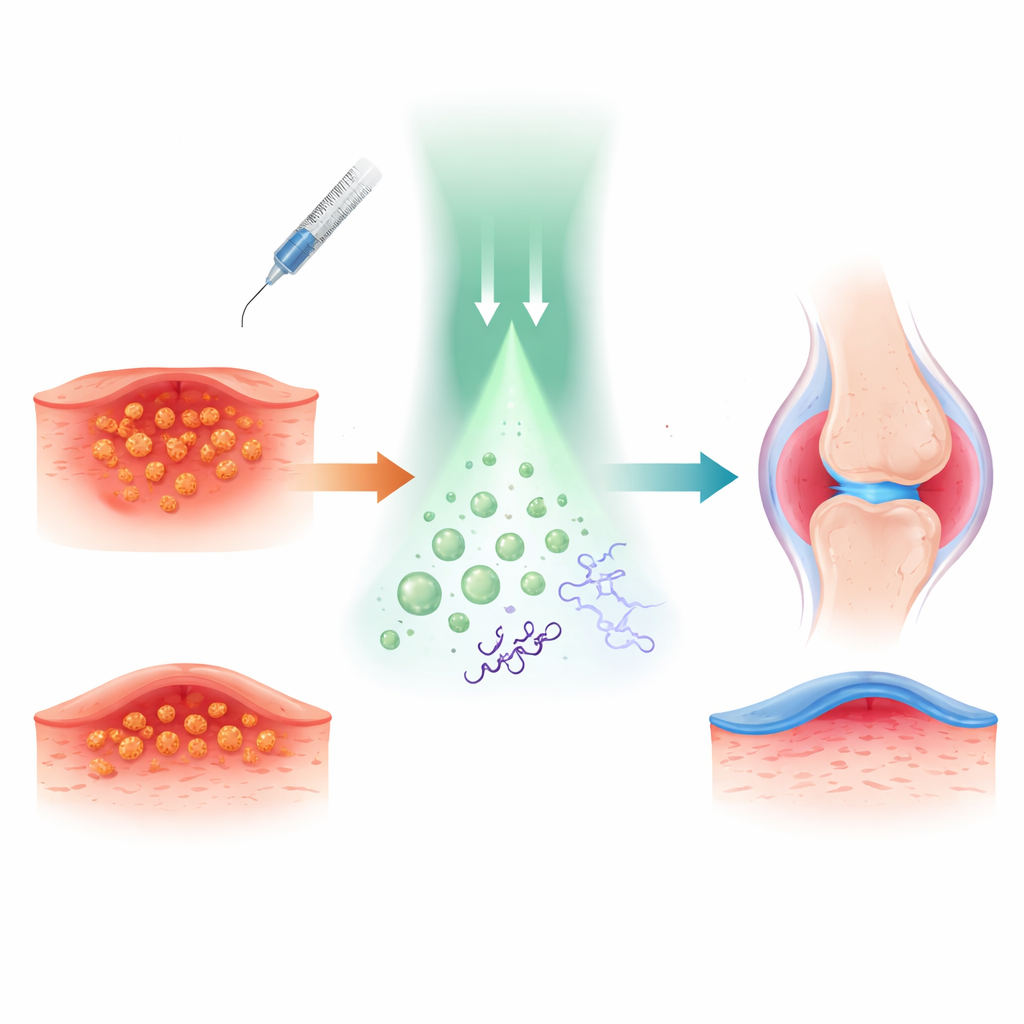
Włączanie leku łagodnym światłem
Aby zrozumieć, jak działa ten przełącznik świetlny, zespół badał chemię w roztworze. Wykazali, że fotokatalizator oparty na irydzie może przekazać elektron do TTC-NO po oświetleniu zielonym światłem. Osłabia to określone wiązanie, powodując uwolnienie tlenku azotu i przywrócenie tetrakainy do aktywnej postaci. Pomiarami za pomocą spektroskopii i chromatografii potwierdzono, że TTC-NO jest prawie całkowicie przekształcany w tetrakainę i tlenek azotu w tych warunkach, podczas gdy w ciemności pozostaje praktycznie niezmieniony. Gdy obie składowe zostały zamknięte w micelach, cząstki pozostały stabilne, miały około 80 nanometrów średnicy i uwalniały zawartość tylko po napromieniowaniu, udowadniając, że koncepcja „leku zakleszczonego w proleku” może być kontrolowana z zewnątrz za pomocą światła.
Przyspieszanie gojenia zakażonych ran
Zespół przeprowadził następnie badania na myszach z ranami skórnymi celowo zakażonymi metycylinoopornym Staphylococcus aureus (MRSA), problematycznym szczepem szpitalnym. Niektóre rany otrzymały standardowe terapie, takie jak antybiotyk czy czynnik wzrostu, podczas gdy inne leczono micelami TTC-NO, z naświetlaniem lub bez niego. Po włączeniu światła system TTC-NO znacznie zmniejszył liczbę bakterii, złagodził stan zapalny, sprzyjał tworzeniu nowych naczyń krwionośnych i zwiększał odkładanie kolagenu — wszystko to jest kluczowe dla prawidłowej regeneracji. Rany leczone w ten sposób zamykały się szybciej i bardziej kompletnie niż te poddane jedynie tetrakainie lub micelom trzymanym w ciemności, a ich przebieg był porównywalny z pierwszorzędowym antybiotykiem. Co ważne, testy bezpieczeństwa nie wykazały istotnych uszkodzeń narządów ani zaburzeń parametrów krwi.
Łagodzenie bólu i tłumienie sygnałów nerwowych
Ponieważ zakażenie i uszkodzenie tkanek silnie aktywują szlaki bólowe, naukowcy dokładnie mierzyli zachowania związane z bólem w tym modelu ran. Tradycyjna tetrakaina chwilowo zwiększała siłę potrzebną do wywołania odpowiedzi bólowej, ale efekt ustępował w ciągu kilku godzin. W przeciwieństwie do tego micele TTC-NO aktywowane światłem zapewniały ulgę nawet do 12 godzin. Badania mikroskopowe skupisk nerwów blisko rdzenia kręgowego oraz zapisy aktywności w korze sensorycznej mózgu wykazały, że skojarzone leczenie osłabiało wyładowania neuronów czuciowych odpowiedzialnych za ból długo po ustąpieniu działania samej tetrakainy. Dalsze eksperymenty sugerowały, że dodatkowy czas działania wynika ze zmniejszenia obciążenia bakteryjnego i stanu zapalnego za sprawą tlenku azotu, a nie tylko z miejscowego znieczulenia nerwów.
Ochrona bolesnych, zakażonych stawów
Naukowcy przetestowali także system u myszy z zapaleniem stawów o etiologii septycznej, poważnym zakażeniu MRSA w obrębie stawu kolanowego, które powoduje obrzęk, utratę kości i silny ból. Micela TTC-NO aktywowana światłem zmniejszyła szerokość stawu, obniżyła liczbę bakterii i ochroniła strukturę kostną, co potwierdzono obrazowaniem wysokiej rozdzielczości. Poziomy szkodliwych molekuł zapalnych we krwi spadły, podczas gdy podniosły się sygnały ochronne. W testach behawioralnych leczone myszy tolerowały większy nacisk mechaniczny na zainfekowaną łapę i poruszały się bardziej swobodnie na otwartej arenie, ponownie wykazując dłużej utrzymującą się ulgę niż po samej tetrakainie. Pomiar aktywności nerwów i mózgu odzwierciedlał te korzyści behawioralne, wskazując na szerokie tłumienie szlaków bólowych bez widocznej toksyczności miejscowej ani systemowej. 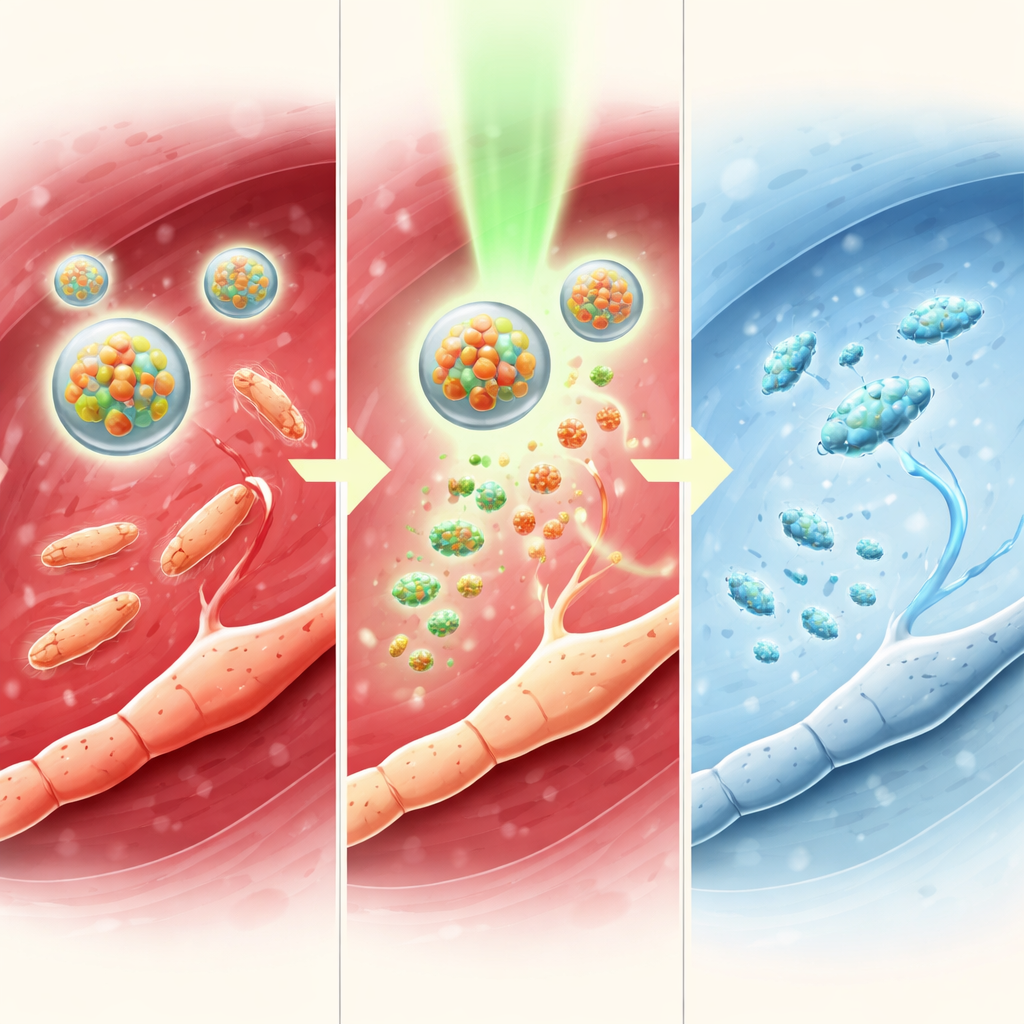
Co to może oznaczać dla pacjentów
Podsumowując, praca demonstruje pojedynczy, aktywowany światłem nanosystem, który jednocześnie usuwa oporne zakażenia bakteryjne i znacząco zmniejsza towarzyszący im ból. Poprzez chemiczne „zakleszczenie” środka znieczulającego wewnątrz struktury uwalniającej tlenek azotu i spakowanie tego w micelle, autorzy uzyskali lokalne, kontrolowane na żądanie uwalnianie dwóch korzystnych czynników przy użyciu łagodnego światła widzialnego. W modelach zwierzęcych ran skórnych i zakażeń stawów ten projekt przyspiesza gojenie i wydłuża ulgę przeciwbólową w porównaniu z konwencjonalnym środkiem miejscowo znieczulającym. Choć przed zastosowaniem u ludzi potrzeba jeszcze wielu badań, badanie podkreśla, w jaki sposób inteligentne, przełączalne leki mogą pewnego dnia uczynić leczenie infekcji jednocześnie skuteczniejszym i bardziej komfortowym.
Cytowanie: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Słowa kluczowe: terapia tlenkiem azotu, leki aktywowane światłem, przeciwbakteryjna analgezja, nanomedycyna, infekcje MRSA