Clear Sky Science · pl
Limfocyty T zaprojektowane przeciw kompleksowi Dickkopf-1-A2 mogą być stosowane w leczeniu nowotworów litych i hematologicznych u osób HLA-A2+
Nowa nadzieja dla trudno leczonych nowotworów
Wiele silnych, nowych immunoterapii działa dobrze w przypadku nowotworów krwi, ale napotyka problemy wobec guzów litych, takich jak rak trzustki, płuca czy piersi. W tym badaniu zaprezentowano specjalnie zmodyfikowane limfocyty T, które lokalizują molekularną „flagę” występującą w szerokim spektrum nowotworów, a w dużej mierze nieobecną w zdrowych tkankach, co daje możliwość jednego leczenia bezpiecznie celującego zarówno w nowotwory krwi, jak i guzy litych u pacjentów noszących powszechny typ układu zgodności immunologicznej.
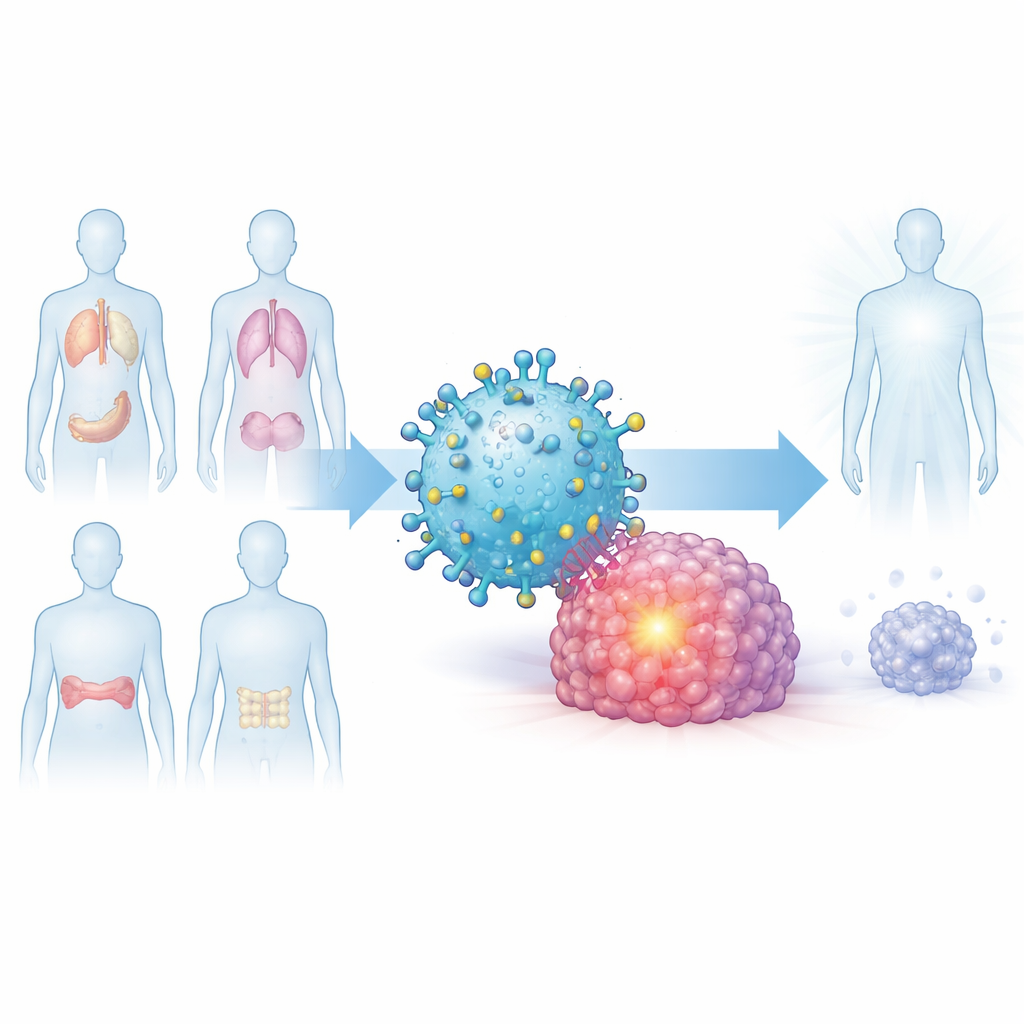
Wspólny sygnał obecny w wielu guzach
Naukowcy zaczęli od pytania, czy istnieje wspólna cecha molekularna pojawiająca się w różnych nowotworach, a rzadko obecna w zdrowych narządach. Skupili się na białku zwanym Dickkopf-1, w skrócie DKK1, które uczestniczy w regulacji szlaków wzrostu komórek i występuje w dużych ilościach w szpiczaku mnogim, raku trzustki, raku płuca oraz agresywnym raku piersi typu triple-negative. Przez analizę dużych publicznych baz danych genowych i badanie próbek guzów wykazali, że DKK1 jest znacznie bardziej obfite w wielu nowotworach niż w odpowiadających im tkankach zdrowych, a u pacjentów, których guzy produkują więcej DKK1, często obserwuje się gorsze przeżycie.
Przekształcanie flagi guza w precyzyjny cel
Ponieważ DKK1 zwykle występuje na zewnątrz komórek, nie jest oczywistym uchwytem dla limfocytów T, które rozpoznają krótkie fragmenty białek prezentowane na powierzchni komórek przez cząsteczki HLA. Wcześniejsze prace zidentyfikowały krótki fragment DKK1 prezentowany przez bardzo powszechny typ HLA znany jako HLA-A2. Zespół już wcześniej stworzył przeciwciało o nazwie C2, które rozpoznaje ten fragment DKK1, gdy jest on trzymany przez HLA-A2 na powierzchni komórki nowotworowej, ale nie na większości zdrowych komórek. W obecnym badaniu zbudowali chimeryczny receptor antygenowy (CAR) wykorzystując część rozpoznającą tego przeciwciała, łącząc ją z wewnętrznymi komponentami sygnalizacyjnymi limfocytu T, tak aby zwykłe limfocyty T mogły zostać przeprogramowane do rozpoznawania połączenia DKK1–HLA-A2, określanego jako kompleks DKK1-A2.
Zmodyfikowane limfocyty T, które odnajdują i niszczą guzy
Naukowcy przetestowali następnie komórki DKK1-A2 CAR-T na szerokim panelu ludzkich linii komórkowych nowotworowych w laboratorium, w tym komórkach szpiczaka mnogiego, raka trzustki, płuca i raka piersi typu triple-negative. Kiedy komórki nowotworowe prezentowały zarówno DKK1, jak i HLA-A2, zmodyfikowane limfocyty T intensywnie się namnażały, uwalniały silne molekuły immunologiczne i skutecznie zabijały komórki nowotworowe. Gdy DKK1 zostało usunięte z komórek nowotworowych lub gdy komórki nie miały HLA-A2, komórki CAR-T przestawały atakować, co dowodzi, że ich aktywność jest wysoce specyficzna wobec zamierzonego celu.
Dowód skuteczności w modelach in vivo
Aby sprawdzić, czy podejście to może zmniejszyć już rozwinięte nowotwory in vivo, zespół wykorzystał kilka modeli mysich przenoszących ludzkie guzy. Komórki DKK1-A2 CAR-T kontrolowały lub eliminowały szpiczaka mnogiego rozwijającego się w szpiku kostnym, guzy trzustki wszczepione w trzustkę, raka płuca rozprzestrzeniającego się drogą krwi oraz agresywne raki piersi, podczas gdy standardowe komórki CAR-T ukierunkowane na CD19 użyte jako kontrola miały niewielki efekt. Terapia zadziałała także przeciw guzom wyhodowanym z prawdziwych próbek raka trzustki pacjentów przeszczepionych do myszy, lepiej odwzorowując chorobę ludzką. Sfałszowana (humanizowana) wersja CAR, zaprojektowana pod kątem zastosowań klinicznych, wykazała jeszcze lepszą długotrwałą kontrolę, częściowo dlatego, że te limfocyty przyjęły stan podobny do pamięci immunologicznej, co pozwalało im utrzymywać się i reagować ponownie, gdy guzy się odradzały.
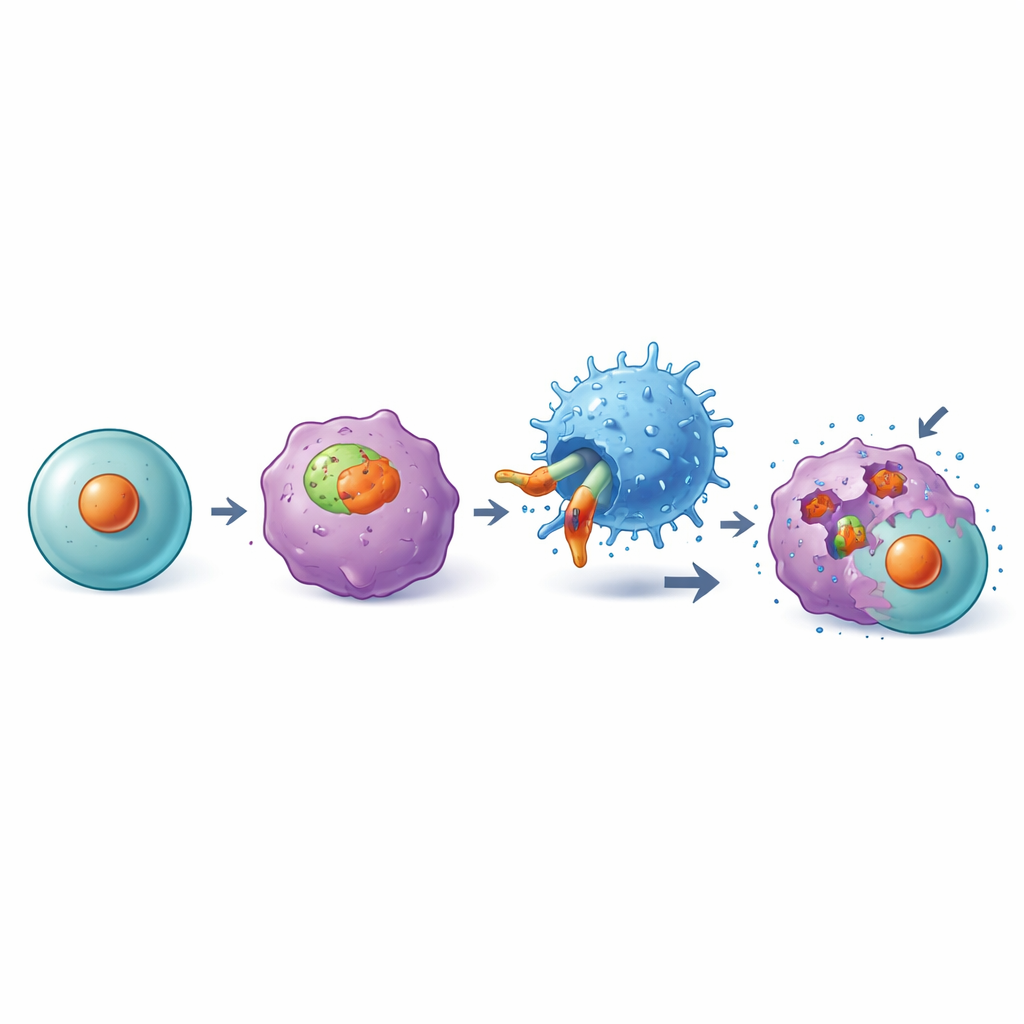
Sprawdzanie bezpieczeństwa wobec krwi i narządów
Każda terapia celowana musi oszczędzać zdrowe tkanki. Autorzy wybarwili z tego powodu dziesiątki rodzajów normalnych ludzkich tkanek i stwierdzili, że poza migdałkami kompleks DKK1-A2 był praktycznie nieobecny. W testach laboratoryjnych komórki DKK1-A2 CAR-T nie uszkadzały komórek krwi ani szpiku kostnego od zdrowych dawców HLA-A2–pozytywnych, w odróżnieniu od komórek CAR-T skierowanych przeciw CD19, które zgodnie z oczekiwaniami niszczyły normalne limfocyty B. W modelach mysich zmodyfikowanych tak, by ekspresjonować ludzki DKK1 i HLA-A2, nowe komórki CAR-T nie wywołały ubytku kluczowych populacji komórek krwi ani płytek krwi i powodowały mniej objawów niebezpiecznego uwalniania cytokin niż niektóre istniejące projekty CAR, co wspiera korzystny profil bezpieczeństwa.
Co to może znaczyć dla pacjentów
Podsumowując, wyniki sugerują, że kompleks DKK1-A2 jest obiecującym „celnym punktem”, który pojawia się w wielu trudno leczonych nowotworach, a w dużej mierze nie występuje w normalnych tkankach. Limfocyty T uzbrojone w CAR przeciw DKK1-A2 potrafiły rozpoznawać i niszczyć różnorodne guzy w modelach przedklinicznych, wykazując ograniczoną toksyczność. Jeśli te wyniki przełożą się na ludzi, podejście to mogłoby zaoferować nową, wspólną immunoterapię dla pacjentów HLA-A2–pozytywnych ze szpiczakiem mnogim, rakiem trzustki, płuca i niektórymi rakami piersi, rozszerzając stosowanie terapii CAR-T poza nowotwory krwi na obszar guzów litych.
Cytowanie: Zhang, Y., Xiong, W., Qian, J. et al. T cells engineered against Dickkopf-1-A2 complex can be used to treat HLA-A2+ solid and hematologic cancers. Nat Commun 17, 2818 (2026). https://doi.org/10.1038/s41467-026-69621-8
Słowa kluczowe: terapia komórkowa CAR-T, DKK1, rak trzustki, szpiczak mnogi, immunoterapia nowotworów litych