Clear Sky Science · pl
Izolowalny kationorodnik i dikation dialumenowy
Dlaczego ta historia o aluminium ma znaczenie
Chemicy nieustannie poszukują tańszych, bardziej powszechnych metali, które mogą wykonać zaawansowane zadania obecnie obsługiwane przez metale szlachetne, takie jak pallad czy platyna. Badanie to wykazuje, że aluminium – metal bardziej znany z puszek i konstrukcji lotniczych – można sprowokować do stworzenia niezwykle reaktywnych form zachowujących się nieco jak maleńkie przełączniki elektronowe. Zrozumienie i kontrola takich egzotycznych gatunków aluminium może ostatecznie pomóc w opracowaniu nowych katalizatorów dla czystszych procesów chemicznych i materiałów.
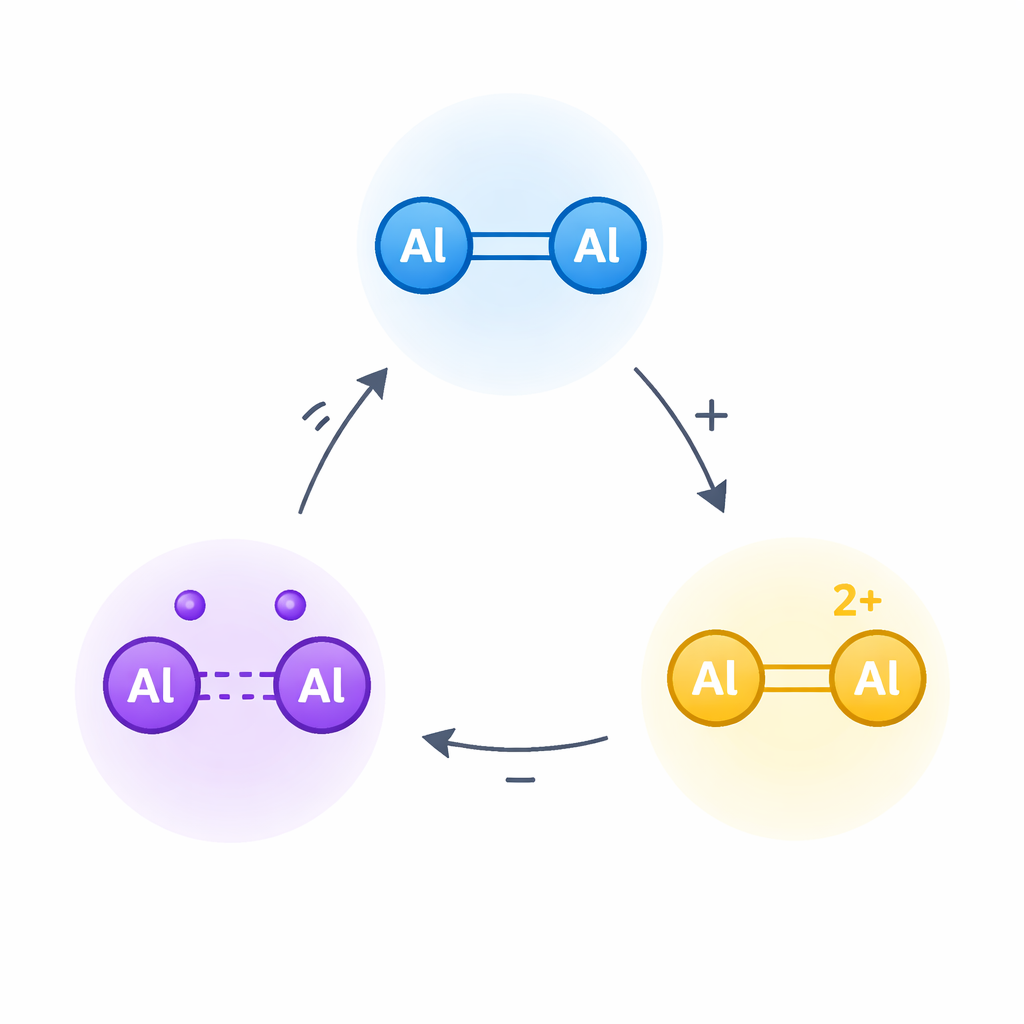
Przekształcenie znanego wiązania w przełącznik elektroniczny
Praca koncentruje się na dialumenie, cząsteczce, w której dwa atomy aluminium dzielą wiązanie podwójne, trochę jak wiązanie podwójne węgiel–węgiel w powszechnych alkenach. W chemii organicznej takie wiązania mogą być utleniane stopniowo, tworząc najpierw kationorodniki, a następnie dikationy – silnie naładowane, wysoce reaktywne formy leżące u podstaw wielu reakcji w elektrochemii i nauce o materiałach. Autorzy zastanawiali się, czy wiązanie aluminium–aluminium w dialumenie da się przeprowadzić przez podobny, dwuetapowy proces utleniania, mimo że aluminium jest silnie elektrono-chłonne i takie naładowane gatunki powinny być wyjątkowo niestabilne.
Projektowanie ochronnej ramy molekularnej
Aby ujarzmić tę reaktywność, zespół zbudował dialumen otoczony masywnymi grupami krzemo-organicznymi oraz silnymi donorami elektronów w postaci ligandów karbenowych. Działają one jak wypchana zbroja i elektroniczne poduszki: osłaniają delikatne centrum aluminium–aluminium przed niepożądanymi reakcjami i dostarczają gęstości elektronowej tam, gdzie jest potrzebna. Z neutralnego dialumenu, oznaczonego jako 1, użyli starannie dobranych utleniaczy do usunięcia najpierw jednego elektronu, a następnie drugiego, generując kationorodnik skoncentrowany na aluminium (2), a następnie dikation (3). Krystalografia rentgenowska dostarczyła migawkowych obrazów wszystkich trzech stanów, ukazując, jak wiązanie aluminium–aluminium stopniowo się wydłuża i zmienia charakter w miarę usuwania elektronów.
Dowód prawdziwego trójstopniowego cyklu redox
Kluczowe pomiary potwierdziły, że kationorodnik rzeczywiście niesie niesparowany elektron skoncentrowany między dwoma atomami aluminium, a nie na otaczających ligandach. Spektroskopia paramagnetyczna elektronów (EPR) pokazała wyraźny sygnał zgodny z jednym elektronem dzielonym przez oba centra aluminium. Studia obliczeniowe wspierały ten obraz, wskazując, że pozostający elektron wiążący zajmuje w dużej mierze orbital aluminium–aluminium. Gdy usunięto drugi elektron, tworząc dikation, wiązanie osłabło w kierunku wiązania pojedynczego, a ładunek dodatni nagromadził się na parach aluminium. Co ważne, badacze wykazali, że wszystkie te zmiany są odwracalne: dodanie elektronów reduktorem odtwarza najpierw kationorodnik, a następnie pierwotny dialumen, a zmieszanie form neutralnej i dwukrotnie naładowanej prowadzi do powstania kationorodnika przez proces komproporcjonowania. Razem te reakcje demonstrują solidny, izolowalny trójstanowy cykl redox w prostym układzie aluminium–aluminium.
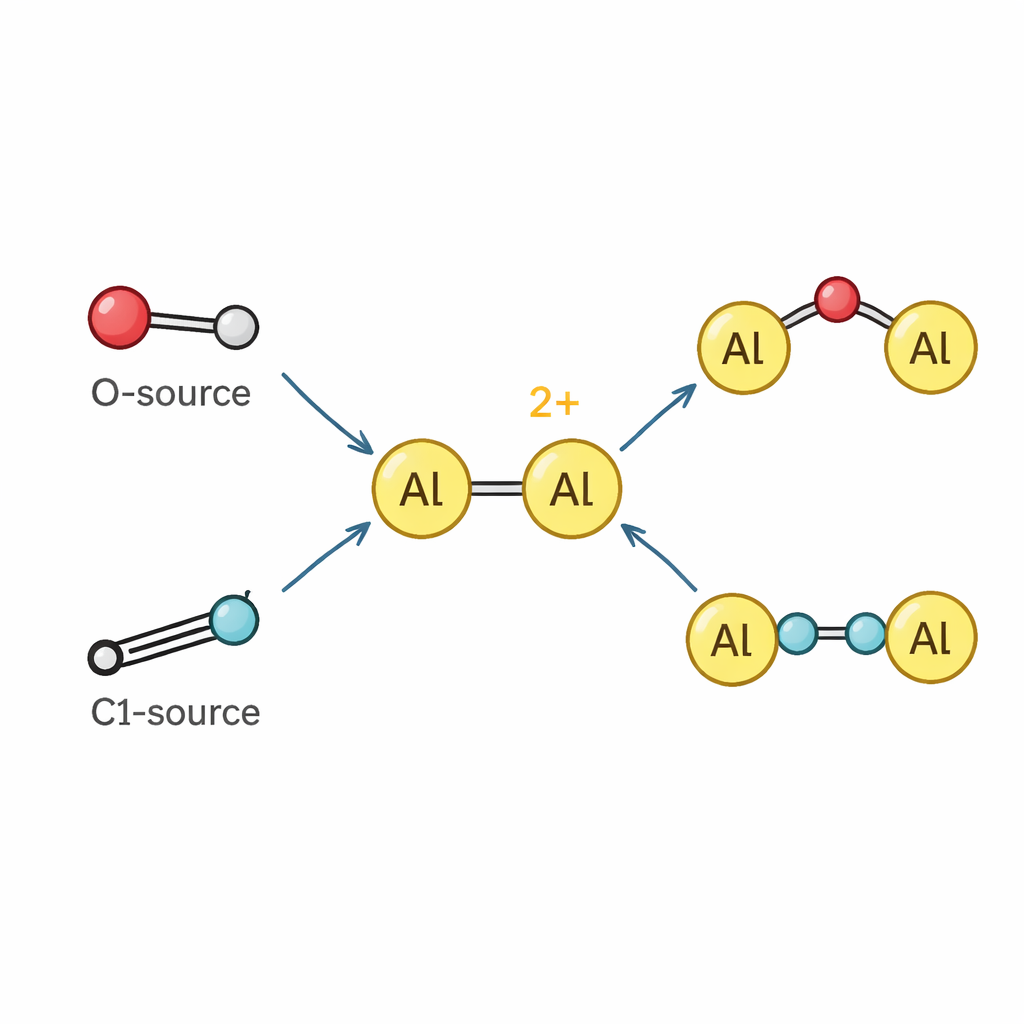
Zmiana roli aluminium w stronę metalu przejściowego
Majac dikation w ręku, zespół zbadał jego reakcje z innymi cząsteczkami. Ponieważ atomy aluminium są silnie ubogie w elektrony, dikation zachowuje się jak potężny kwas Lewisa, chętnie wiążąc zasadowe partnery, takie jak pirydyna i pokrewne molekuły, tworząc nowe kompleksy dialuminiowe. Poza zwykłym wiązaniem, dikation może rozszczepiać i wstawiać się w wiązania chemiczne. Wyciąga atomy tlenu z podtlenku azotu i tlenku pirydyny, tworząc stabilne gatunki, gdzie atom tlenu mostkuje dwa centra aluminium lub jest włączony w krótki łańcuch aluminium–tlen–krzem przypominający fragment ramy zeolitu. Reaguje także z izocyjanidami – małymi jednostkami węgiel–azot używanymi jako jednowęglowe cegiełki – sklejając je w dłuższe fragmenty N–C–C–N rozpięte między dwoma atomami aluminium, co stanowi rzadki przykład „homologacji” izocyjanidów napędzanej przez kation pierwiastka głównego.
Co to oznacza na przyszłość
Mówiąc prostymi słowami, badacze przekształcili wiązanie aluminium–aluminium w kontrolowalny, trójpozycyjny przełącznik elektroniczny, który można przełączać między stanami neutralnym, jednoelektronowo naładowanym i dwukrotnie naładowanym, z odmiennymi kształtami i reaktywnościami w każdym stanie. Wersja dwukrotnie naładowana jest szczególnie wszechstronna, przechwytując elektrony i małe fragmenty z innych cząsteczek w sposób zwykle przypisywany droższym metalom przejściowym. Pokazując, że takie zachowanie jest możliwe z udziałem aluminium i że różne stany można niezawodnie przekształcać, praca ta otwiera drogę do projektowania nowych, zrównoważonych katalizatorów i funkcjonalnych materiałów zbudowanych z jednego z najobficiej występujących na Ziemi metali.
Cytowanie: Liu, X., Kostenko, A., Körber, E. et al. Isolable radical cation and dication of dialumene. Nat Commun 17, 1937 (2026). https://doi.org/10.1038/s41467-026-69607-6
Słowa kluczowe: kataliza aluminium, cząsteczki przełączalne redox, chemia pierwiastków głównych, kationorodniki, aktywacja małych cząsteczek