Clear Sky Science · pl
Oś Treg-γδ T determinuje dimorfizm płciowy w wątrobotokarcynogenezie
Dlaczego niektóre nowotwory wątroby silniej dotykają mężczyzn
Lekarze od dawna wiedzą, że rak wątroby występuje u mężczyzn około dwa razy częściej niż u kobiet, jednak przyczyny wykraczają poza proste różnice w hormonach płciowych. To badanie zagłębia się w komórki układu odpornościowego zasiedlające guzy wątroby i odkrywa ukrytą komunikację między dwoma typami limfocytów T, która pomaga wyjaśnić, dlaczego wątroby mężczyzn są bardziej podatne — oraz jak te odkrycia mogą wskazać nowe, bardziej dopasowane terapie.
Immunologiczna przepychanka w obrębie guzów wątroby
Rak wątroby, w szczególności rak wątrobowokomórkowy, rozwija się w złożonym otoczeniu komórek odpornościowych, naczyń krwionośnych i zwłókniałej tkanki. Autorzy porównali guzy u mężczyzn i kobiet, zarówno u pacjentów, jak i w modelach mysich, i znaleźli uderzającą nierównowagę: guzy u samców były pełne komórek regulatorowych T, czyli Tregów, typu komórek, które normalnie tłumią nadmierne reakcje odpornościowe. Jednocześnie ogólna liczba innych powszechnych limfocytów T nie różniła się znacząco między płciami. Ponieważ wysokie poziomy Treg wiązały się z gorszym przeżyciem, zespół zasugerował, że te komórki nie są tylko biernymi obserwatorami, lecz aktywnymi współsprawcami pomagającymi guzom uciec przed atakiem immunologicznym. 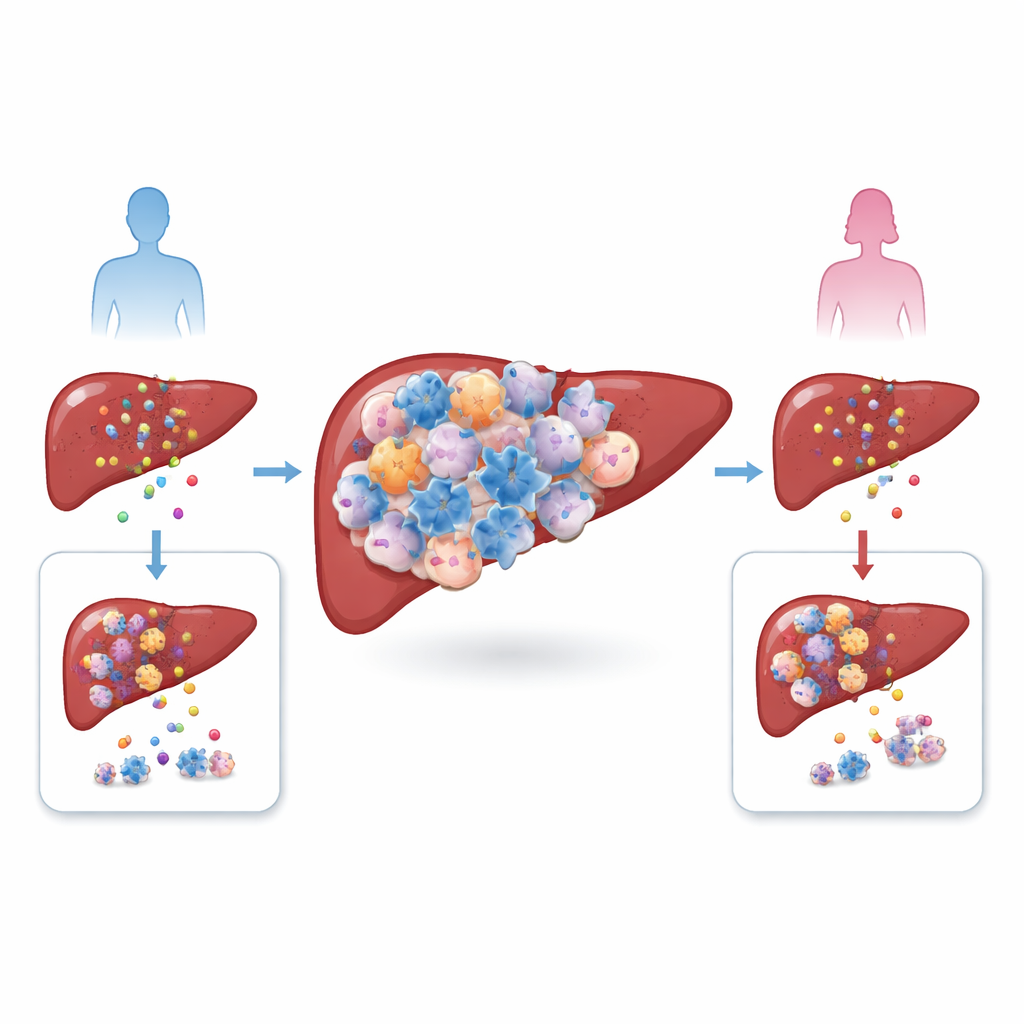
Jak męskie hormony przyciągają komórki tłumiące
Aby zrozumieć, dlaczego guzy u mężczyzn przyciągają więcej Tregów, badacze skupili się na sygnałach chemicznych wydzielanych przez komórki nowotworowe. Stwierdzili, że męskie guzy wątroby wytwarzały większe ilości cząsteczki zwanej Ccl2, podczas gdy Tregi miały więcej jej odpowiadającego receptora, Ccr2. To połączenie działa jak znak nawigacyjny, przyciągając Tregi do guza. Gdy sygnał Ccl2 lub receptor Ccr2 został usunięty u myszy, guzy zmniejszały się, a do wątroby napływało znacznie mniej Tregów, szczególnie u samców. Zespół wykazał następnie, że testosteron, główny męski hormon płciowy, napędza ten proces: aktywuje łańcuch białek w komórkach raka wątroby, który włącza gen Ccl2, wzmacniając chemiczny sygnał przywołujący Tregi. Kastracje u myszy samczych, które obniżają poziom testosteronu, prowadziły do mniejszej ilości Ccl2 w guzach i mniejszej obecności Tregów.
Komórki strażnicze, które mogłyby walczyć z rakiem — lecz są powstrzymywane
Inny typ limfocytów T, znany jako komórki gamma-delta, może działać jako szybka „straż”, rozpoznając i zabijając komórki nowotworowe bez typowego mechanizmu prezentacji antygenu. W zdrowej wątrobie te komórki są stosunkowo rzadkie, ale w raku wątroby mogą być silnymi pogromcami guza. Badanie wykazało, że guzy u kobiet zawierały więcej komórek gamma-delta, które były bardziej aktywne i lepiej uzbrojone w toksyczne cząsteczki. Usunięcie męskich hormonów u myszy zwiększało liczbę i sprawność komórek gamma-delta w guzach, przy jednoczesnym pozostawieniu klasycznych cytotoksycznych limfocytów CD8 w dużej mierze bez zmian. W hodowlach komórkowych komórki gamma-delta łatwo uszkadzały komórki raka wątroby, lecz efekt ten osłabiał się po dodaniu Tregów, co sugeruje, że Tregi specyficznie hamują tę obiecującą populację przeciwnowotworową.
Hipoksja, tajne przesyłki i uciszeni obrońcy
Bardziej wnikliwie, badacze pytali, jak Tregi potrafią wyciszać komórki gamma-delta. W guzach często brakuje tlenu — stan zwany hipoksją. W tych niskotlenowych warunkach Tregi w guzach samców zaczynały produkować duże ilości białka o nazwie S100a4. Zamiast działać bezpośrednio jako wolny czynnik, S100a4 był pakowany w małe pęcherzyki otoczone błoną, znane jako pozakomórkowe pęcherzyki (extracellular vesicles). Pęcherzyki te odrywały się od Tregów i były wychwytywane przez sąsiednie komórki gamma-delta. Po wejściu do środka S100a4 przestawiał komórkowe systemy kontroli genetycznej: zmniejszał dostępność regionów DNA kontrolujących kluczowe szlaki sygnałowe i molekuły zabijania oraz obniżał ich aktywność. Komórki gamma-delta stały się mniej zdolne do reakcji przez receptory T i mniej skuteczne w uwalnianiu toksycznych białek i cytokin, co skutecznie osłabiało ich przeciwnowotworową ostrość. 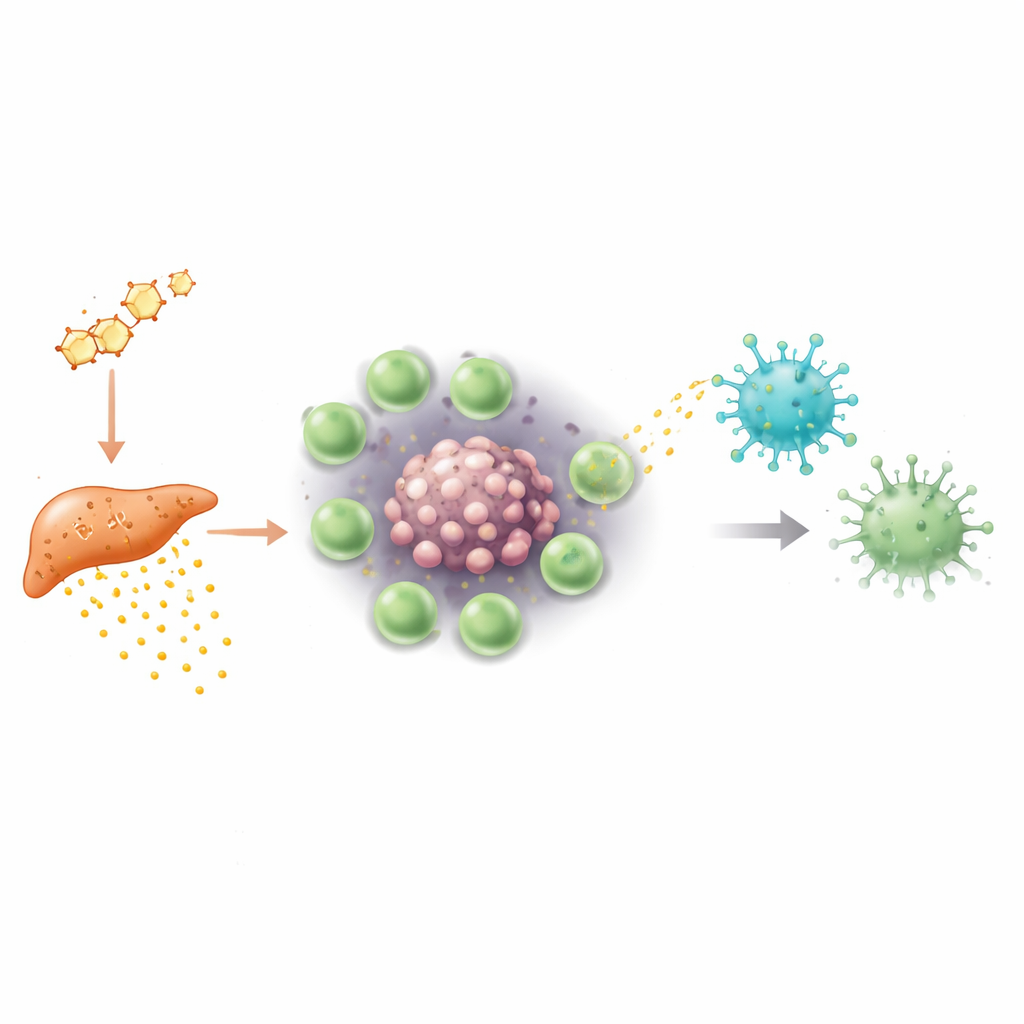
Przerwanie szkodliwego obwodu
Na koniec zespół sprawdził, co się stanie, gdy oś Treg–S100a4–gamma-delta zostanie zakłócona. U myszy zmodyfikowanych tak, że Tregy nie mogą wytwarzać S100a4, męskie guzy wątroby zmniejszyły się, ogólny poziom S100a4 w guzach spadł, a komórki gamma-delta stały się liczniejsze i bardziej aktywne. Co istotne, liczba Tregów w guzie nie zmalała — jedynie ich tłumiący wpływ na komórki gamma-delta został zniesiony. Ta zmiana niemal zatarła zwykłą różnicę w nasileniu guza między samcami i samicami, podkreślając, jak centralna dla różnic płciowych w raku wątroby jest ta ścieżka.
Co to oznacza dla przyszłych terapii
Mówiąc w przystępny sposób, badanie pokazuje, że męskie hormony skłaniają komórki raka wątroby do wysyłania silniejszych „sygnałów powitalnych” dla immunosupresyjnych Tregów. Gdy już znajdą się w guzie — i pod wpływem stresu związanego z niskim poziomem tlenu — te Tregy wysyłają pęcherzyki wypełnione S100a4, które cicho unieszkodliwiają pobliskie komórki gamma-delta, które mogłyby inaczej hamować rozwój nowotworu. Celowanie albo w sygnał Ccl2 przyciągający Tregy, albo w przekazy S100a4 wyciszające komórki gamma-delta może przywrócić własną obronę organizmu, zwłaszcza u mężczyzn. Praca ta sugeruje, że leczenie raka wątroby może zyskać, gdy będzie uwzględniać różnice płci i wykorzystywać, zamiast ignorować, unikalne możliwości komórek gamma-delta.
Cytowanie: Liang, Q., Zhang, Q., Zhang, W. et al. Treg-γδ T cell axis determines sexual dimorphism in hepatocarcinogenesis. Nat Commun 17, 2640 (2026). https://doi.org/10.1038/s41467-026-69603-w
Słowa kluczowe: rak wątrobowokomórkowy, komórki T regulatorowe, komórki T gamma-delta, różnice płci, immunologia nowotworów