Clear Sky Science · pl
Podwójne rekrutowanie dwóch cząsteczek CCM2 do KRIT1 tłumi ekspresję KLF4
Dlaczego naczynia krwionośne mózgu wymagają ścisłej kontroli
Naczynia krwionośne w mózgu muszą iść po cienkiej linii: muszą być wystarczająco wytrzymałe, by zapobiegać przeciekom, a zarazem na tyle elastyczne, by odpowiadać na potrzeby organizmu. Gdy ta równowaga zawodzi, u ludzi mogą powstawać malformacje jamiste mózgu — skupiska kruchych, pęcherzykowatych naczyń, które mogą krwawić i powodować drgawki lub udary. To badanie ujawnia wcześniej nieznane molekularne „uścisk dłoni” między trzema białkami, który pomaga utrzymać naczynia mózgowe w stabilnym stanie, oraz pokazuje, jak przerwanie tego kontaktu może prowadzić do choroby.
Bramkarze zdrowia naczyń
Komórki wyściełające naczynia krwionośne polegają na zestawie głównych przełączników, zwanych KLF2 i KLF4, które kontrolują geny utrzymujące wytrzymałość i tożsamość naczyń. Jeśli te przełączniki zostaną zbyt silnie włączone, naczynia stają się nieprawidłowe i podatne na uszkodzenia. Dwa inne białka, KRIT1 i CCM2, są znane z roli w ochronie tego systemu. Osoby dziedziczące wadliwe wersje któregokolwiek z tych białek są w wysokim ryzyku malformacji jamistych mózgu. Do tej pory jednak naukowcy nie rozumieli dokładnie, jak KRIT1 i CCM2 współdziałają, by powstrzymać KLF4.
Zaskakujący zespół trojga
Naukowcy użyli w laboratorium ludzkich komórek o cechach śródbłonkowych i selektywnie zmniejszyli ilość CCM2 lub KRIT1 przy użyciu narzędzi genetycznych. Gdy któreś z tych białek zostało usunięte, poziom KLF4 gwałtownie wzrósł, co odpowiada obserwacjom w modelach zwierzęcych i u pacjentów. Przywrócenie normalnego poziomu CCM2 lub KRIT1 obniżało KLF4 — ale tylko wtedy, gdy przywrócone białka wciąż potrafiły się ze sobą wiązać. Poprzez precyzyjne zmiany w regionach, w których CCM2 i KRIT1 wchodzą w interakcję, zespół wykazał, że ten fizyczny kontakt jest niezbędny do powstrzymania wzrostu KLF4. Eksperymenty te jasno umieszczają partnerstwo KRIT1–CCM2 w centrum układu kontrolującego ten potężny czynnik transkrypcyjny.
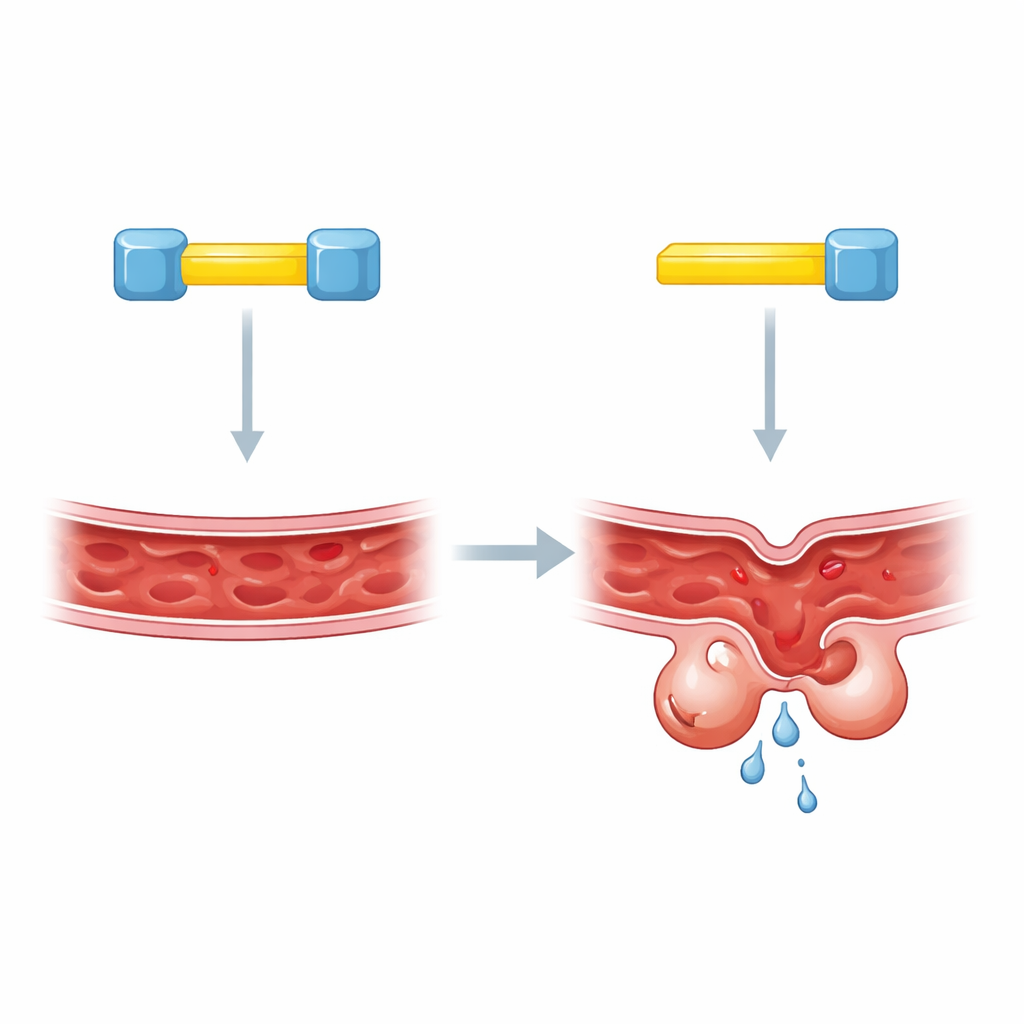
Dwa zamki na jednym kluczu
Aby zgłębić mechanizm, autorzy skupili się na krótkich odcinkach w KRIT1, które działają jak molekularne miejsca dokujące. Wcześniejsze prace sugerowały, że CCM2 przyczepia się do KRIT1 w jednym z tych miejsc, ale różne metody dały sprzeczne odpowiedzi, które. Nowe badanie ujawnia, że nieporozumienia wynikały z faktu, że prawdziwy obraz jest bardziej złożony: KRIT1 ma dwa blisko położone segmenty dokujące i oba są potrzebne. Gdy którykolwiek segment został zaburzony, poziomy KLF4 pozostawały nienaturalnie wysokie, tak jakby KRIT1 w ogóle nie było. Testy biochemiczne w zmodyfikowanych komórkach pokazały, że pojedyncze białko KRIT1 może połączyć jednocześnie dwie oddzielne cząsteczki CCM2, sugerując nieoczekiwaną trójskładnikową strukturę.
Widząc molekularną zacisk w szczegółach
Zespół oczyścił odpowiednie fragmenty CCM2 i KRIT1 i zbadał, jak łączą się w roztworze i w kryształach. Pomiary masy kompleksu wskazały, że dwie kopie kluczowego regionu CCM2 wiążą się z pojedynczym paskiem KRIT1 zawierającym parę miejsc dokujących. Obrazowanie strukturalne o wysokiej rozdzielczości potwierdziło to ułożenie 2:1: jedna wydłużona peptydowa sekwencja KRIT1 przechodzi między dwoma domenami CCM2, przy czym każde miejsce dokujące mieści się w podobnej kieszeni na innej cząsteczce CCM2. Krótki segment helikalny między miejscami dokującymi pomaga ustawić dwie domeny CCM2 obok siebie, tworząc ciasną, zaciskową strukturę. Tego typu podwójne zaangażowanie — dwie domeny wiążące przymocowujące się do tandemowych miejsc w jednym partnerze — nie było wcześniej obserwowane dla tej rodziny modułów białkowych.
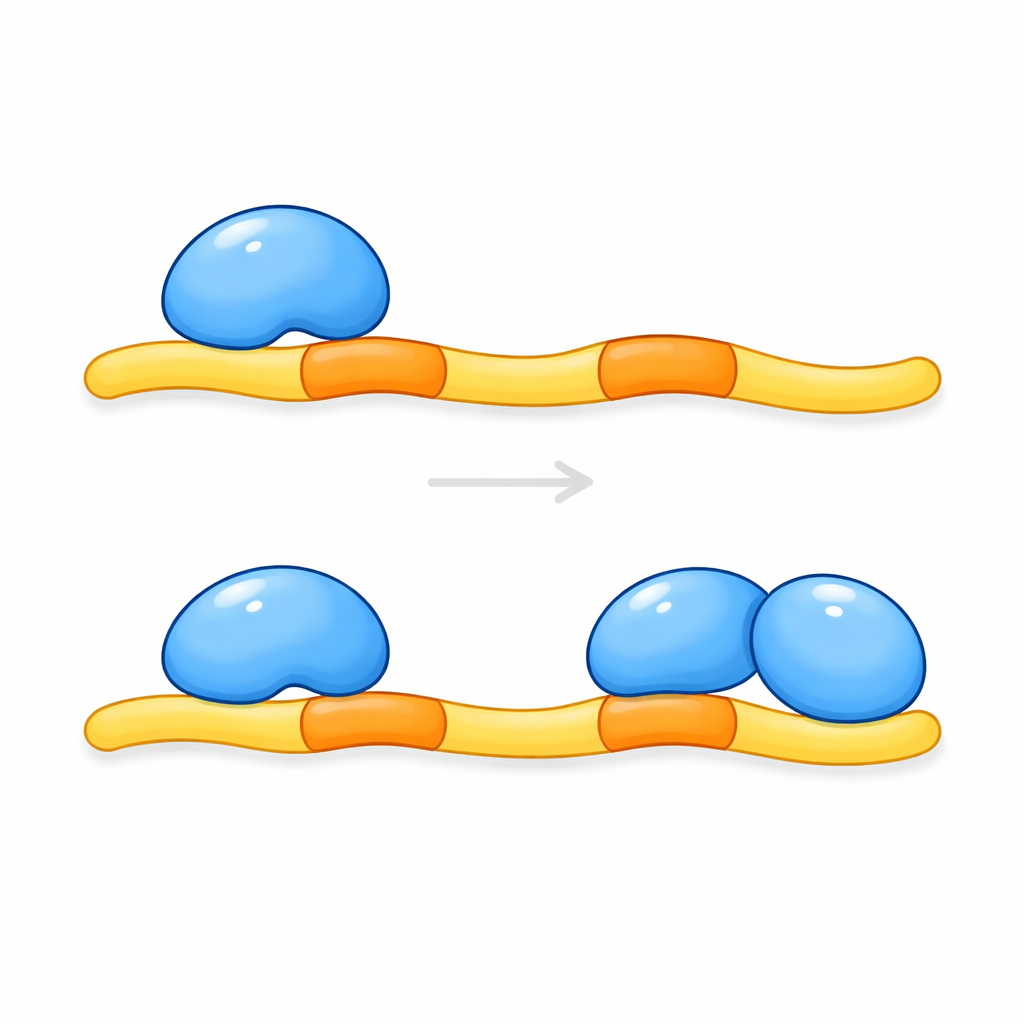
Implikacje dla chorób mózgu i nie tylko
Wyniki te pokazują, że KRIT1 nie wiąże po prostu jednej cząsteczki CCM2; działa raczej jako rusztowanie, które rekrutuje parę białek CCM2. Tylko gdy oba miejsca dokujące na KRIT1 są zajęte, kompleks może właściwie powstrzymywać produkcję KLF4 i w konsekwencji pomagać zapobiegać powstawaniu kruchych naczyń. Mutacje w KRIT1, które zaburzają którekolwiek z miejsc dokujących, prawdopodobnie osłabiają ten ochronny zacisk i mogą wyjaśniać niektóre formy dziedzicznych malformacji jamistych mózgu. Ponieważ wiele innych ludzkich białek nosi podobne bliźniacze motywy dokujące, badanie to sugeruje także szerszą zasadę: podwójne wiązanie przez pary spokrewnionych domen może być powszechnym sposobem, w jaki komórki precyzują sieci sygnałowe. Zrozumienie tej trójskładnikowej interakcji może ostatecznie poprowadzić do strategii stabilizowania naczyń krwionośnych u osób zagrożonych krwotokami mózgowymi.
Cytowanie: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
Słowa kluczowe: malformacje jamiste mózgu, komórki śródbłonka, KRIT1, CCM2, KLF4