Clear Sky Science · pl
Identyfikacja stanu bariery krew‑mózg w glejakach bez kontrastu za pomocą generatywnego AI dyfuzyjnego i MRI bez środka kontrastowego
Dlaczego to ważne dla pacjentów z guzami mózgu
Pacjenci z guzami mózgu rutynowo przechodzą badania MRI, a wielu z nich otrzymuje dodatkowo wstrzyknięty środek kontrastowy, by lekarze mogli ocenić, czy ochronna bariera krew–mózg została naruszona. Ta informacja kieruje decyzjami dotyczącymi operacji, radioterapii i rokowania — jednak środek kontrastowy wiąże się z ryzykiem, zwiększa czas i koszty badania oraz nie zawsze jest dostępny. W tej pracy przedstawiono system sztucznej inteligencji (AI), który analizuje rutynowe, pozbawione kontrastu skany MRI i wirtualnie odtwarza brakujące obrazy z kontrastem, umożliwiając lekarzom wnioskowanie o stanie bariery krew–mózg bez podawania środka kontrastowego.
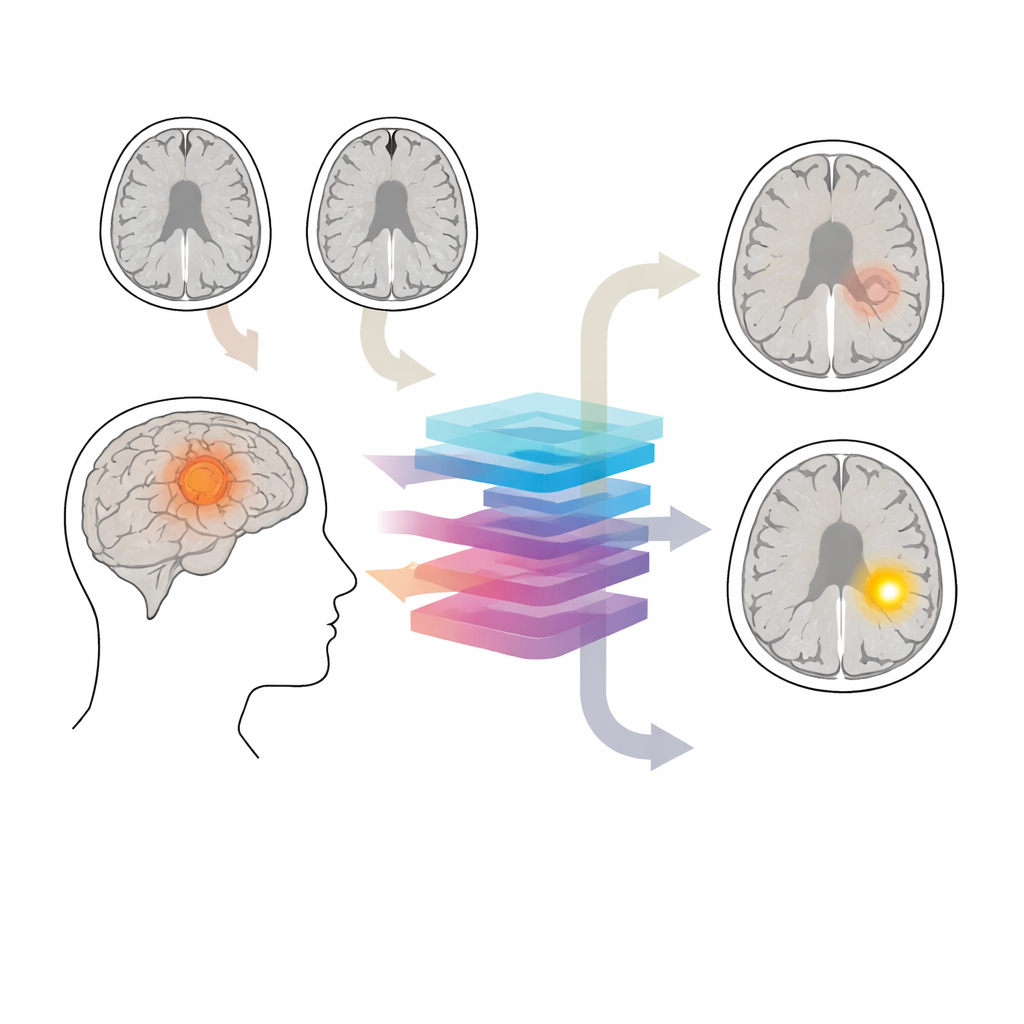
Ochronny strażnik mózgu
Bariera krew–mózg działa jak mikroskopijny filtr wokół naczyń krwionośnych w mózgu, przepuszczając jedynie bardzo małe cząsteczki. W wielu guzach glejakowych bariera ta staje się nieszczelna. Na standardowym MRI z kontrastem obszary nieszczelne uwidaczniają się po podaniu środka, podczas gdy obszary nieuszkodzone pozostają ciemne. Te wzorce wpływają na intensywność leczenia guza i pomagają określić, co usunąć chirurgicznie lub na co ukierunkować radioterapię. Jednak badania z kontrastem bywają pomijane — na przykład we wstępnej diagnostyce lub w długoterminowej obserwacji wolno rosnących guzów — a niektórzy pacjenci powinni całkowicie unikać kontrastu z powodu chorób nerek, reakcji alergicznych lub obaw o odkładanie gadolinowego w mózgu.
Przekształcanie zwykłych skanów w wirtualny kontrast
Autorzy postawili pytanie, czy skany MRI bez kontrastu, które są już powszechnie wykonywane, zawierają wystarczająco subtelnych informacji, aby AI mogła wnioskować, co pokazałby skan z kontrastem. Skoncentrowali się na dwóch powszechnych sekwencjach: T1 i T2‑FLAIR. Chociaż nie pokazują one bezpośrednio przecieku bariery krew–mózg, rejestrują strukturę guza, towarzyszący obrzęk i uszkodzenia tkanek, które często towarzyszą naruszeniu bariery. Zespół zbudował system o nazwie CBSI, który najpierw generuje syntetyczne obrazy z kontrastem z tych skanów bez kontrastu, a następnie wykorzystuje je wraz z oryginalnymi obrazami do oceny, czy bariera jest nienaruszona, czy uszkodzona w każdym z glejaków.
Jak działa nowy system AI
Rdzeniem CBSI jest model dyfuzyjny — rodzaj AI, który zaczyna od zaszumionych obrazów i iteracyjnie „odszumia” je, tworząc realistyczne obrazy. Tutaj uczy się on przekształcać dane wejściowe bez kontrastu w dwa alternatywne wirtualne obrazy z kontrastem: jeden zakładający nienaruszoną barierę i drugi zakładający barierę nieszczelną. Mechanizm wskazujący kieruje modelem, jaki wzorzec wzmocnienia ma osiągnąć, a dodatkowy etap segmentacji pomaga skupić się na obszarze guza. W drugiej fazie oddzielna sieć porównuje dwa syntetyczne wyniki dla każdego pacjenta i ocenia, który z nich jest bardziej spójny z oryginalnymi danymi MRI. Ta decyzja jest następnie przetłumaczona na przewidywany stan bariery krew–mózg.
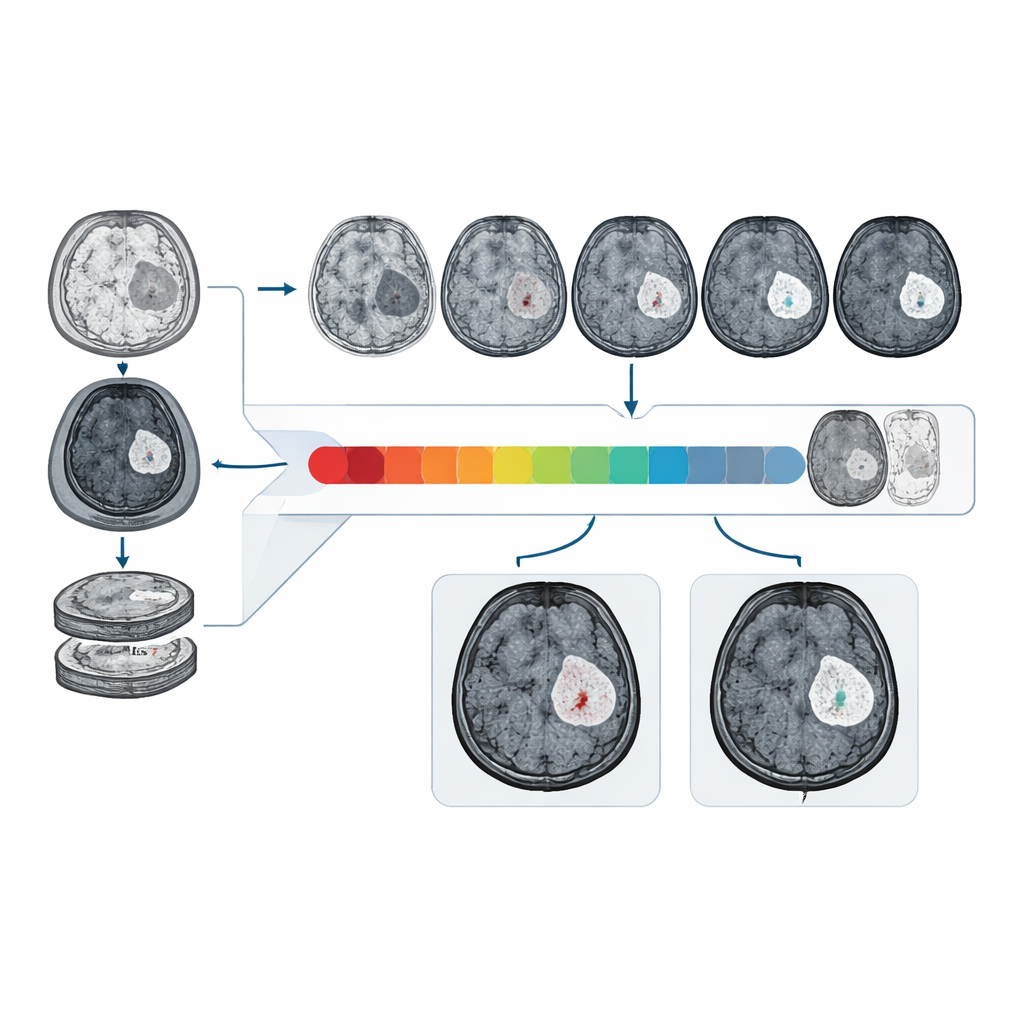
Jak dobrze działa na rzeczywistych i zróżnicowanych danych
Badacze trenowali i testowali CBSI na danych MRI od 1535 pacjentów z glejakami zebranych w wielu szpitalach oraz z międzynarodowych zbiorów publicznych. Na zewnętrznym, klinicznym zestawie testowym CBSI odróżniał barierę nienaruszoną od uszkodzonej z polem pod krzywą (AUC) około 81%, wyraźnie lepiej niż modele działające wyłącznie na obrazach bez kontrastu i zbliżając się do wyników modeli, które miały dostęp do rzeczywistych skanów z kontrastem. Radiolodzy, którym pokazano losowo pomieszane prawdziwe i syntetyczne obrazy z kontrastem wygenerowane przez system, ocenili ponad 90% syntetycznych obrazów jako wysokiej jakości diagnostycznej, a ich zdolność do identyfikacji wzmocnienia kontrastowego na obrazach syntetycznych była podobna do wyników na obrazach rzeczywistych.
Korzyści dla planowania leczenia i opieki przyszłej
Ponieważ syntetyczne obrazy z kontrastem wytwarzane przez CBSI oddają szczegóły guza i wzorce wzmocnienia, poprawiły one także zadania wtórne, takie jak wyznaczanie granic guza i oszacowanie stopnia złośliwości — oba silnie zależne od zachowania bariery krew–mózg. Metoda dobrze uogólniała się na różne aparaty, protokoły obrazowania i populacje pacjentów, w tym dane z Afryki Subsaharyjskiej i większych międzynarodowych kohort. Choć autorzy przyznają, że każdy system głębokiego uczenia pozostaje narzędziem statystycznym, a nie bezpośrednim oknem na biologię, ich wyniki sugerują, że wirtualne obrazowanie z kontrastem mogłoby zmniejszyć zależność od wstrzykiwanych środków, zwłaszcza u pacjentów wrażliwych lub w warunkach, gdzie badania z kontrastem są trudne do wykonania. W praktyce podejście AI może pozwolić lekarzom wydobyć kluczowe informacje kształtujące leczenie dotyczące bariery krew–mózg z badań, które pacjenci już przechodzą — bez dodatkowego wkłucia.
Cytowanie: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Słowa kluczowe: glejak, bariera krew‑mózg, MRI mózgu, AI w obrazowaniu medycznym, obrazowanie bez kontrastu