Clear Sky Science · pl
Współdzielone przez zacisk rozpoznawanie promotorów przez polimerazę RNA poxwirusa i jej partnera podobnego do TBP/TFIIB
Jak wirus przeprogramowuje kontrolę genów w naszych komórkach
Poxwirusy, w tym wirus historycznie odpowiedzialny za ospę prawdziwą, prowadzą całą ekspresję genów w cytoplazmie naszych komórek, daleko od komórkowego centrum kontroli DNA w jądrze. Aby to osiągnąć, przynoszą ze sobą własną miniaturową „fabrykę genetyczną”. To badanie ujawnia, na poziomie atomowym, w jaki sposób jeden z tych wirusów, Vaccinia, uruchamia specyficzną falę swoich genów w trakcie zakażenia, używając niespodziewanego białka o kształcie zacisku, które współdziała z wirusową maszyną kopiującą.
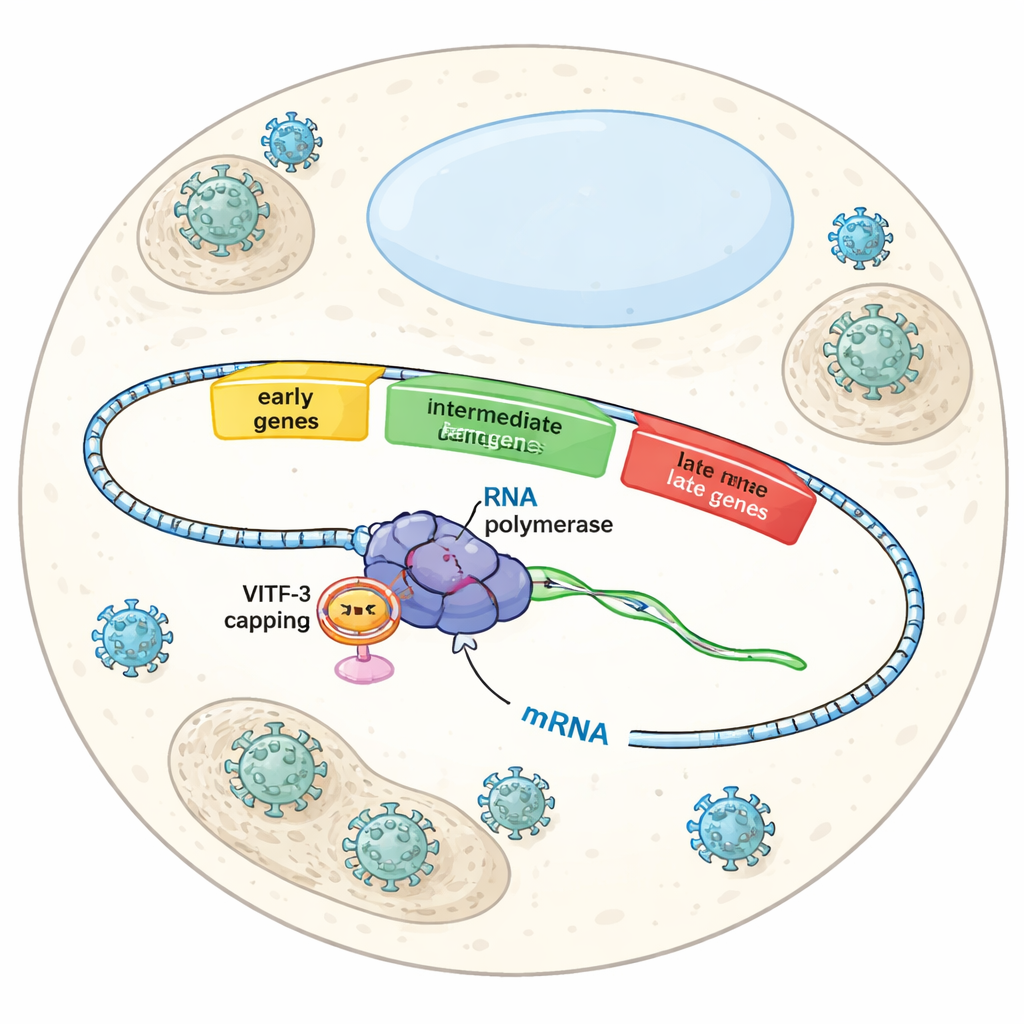
Trzy fale w wirusowym przejęciu kontroli
Kiedy Vaccinia zakaża komórkę, nie uruchamia wszystkich swoich genów naraz. Zamiast tego działa według precyzyjnie zaplanowanego scenariusza: geny wczesne, pośrednie i późne. Geny wczesne przygotowują grunt pod replikację wirusa, geny pośrednie pomagają zbudować aparaturę do produkcji nowych cząstek wirusowych, a geny późne kończą montaże i pakowanie. Każda fala zależy od tej samej wirusowej polimerazy RNA — enzymu, który odczytuje DNA, by wytworzyć RNA — ale różne czynniki pomocnicze informują polimerazę, którą grupę genów aktywować na danym etapie. Dotychczas naukowcy dość dobrze rozumieli kontrolę genów wczesnych, natomiast to, jak wirus rozpoznaje i aktywuje geny pośrednie, pozostawało zagadką.
Pomocnik w kształcie pierścienia, który potrzebuje partnera
Naukowcy skupili się na dwuczęściowym białku zwanym VITF‑3, znanym z konieczności do włączania genów pośrednich. Wiele organizmów, w tym ludzie, używa pary białek TBP i TFIIB, aby poprowadzić swoją polimerazę RNA do właściwego miejsca startu na DNA. Zespół wykazał, że VITF‑3 to wysoce zmodyfikowana wersja tej samej starożytnej pary. Jednak w odróżnieniu od komórkowych odpowiedników, VITF‑3 samodzielnie nie wiąże się z DNA. Zamiast tego jego dwie podjednostki zazębiają się, tworząc zamknięty pierścień, który jest w praktyce obojętny wobec DNA, chyba że obecna jest wirusowa polimeraza RNA. To było nieoczekiwane, ponieważ w większości systemów element podobny do TBP najpierw wiąże DNA promotora, a dopiero potem rekrutuje polimerazę; tutaj wirus wydaje się zmienić kolejność zdarzeń.
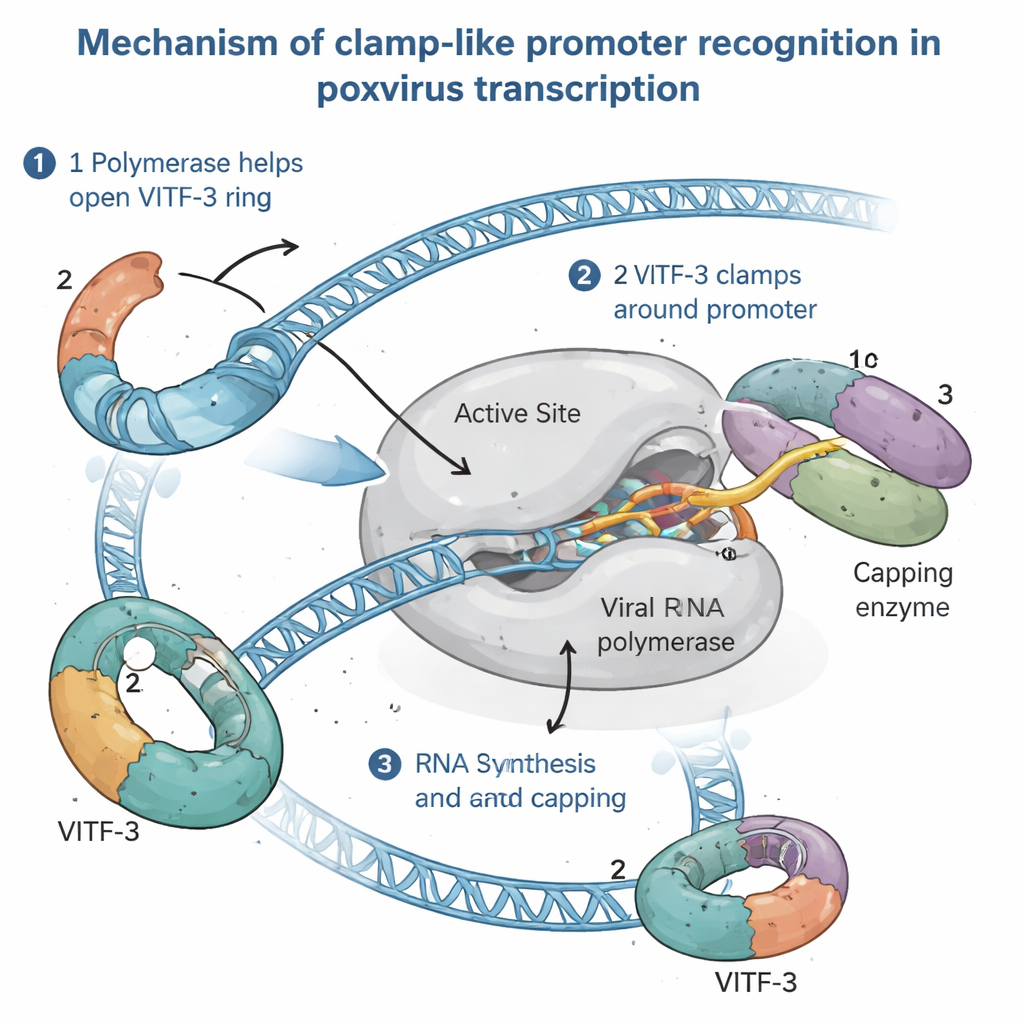
Obserwacja maszyny transkrypcyjnej pośredniego typu w akcji
Aby zrozumieć, jak działa to nietypowe ustawienie, autorzy wyizolowali cały pośredni kompleks preinicjacyjny — zespół gotowy tuż przed rozpoczęciem syntezy RNA — z zakażonych komórek ludzkich. Przy użyciu wysokorozdzielczej kryoelektronowej mikroskopii zwizualizowali kompleks w przybliżeniu z rozdzielczością 2,4 Ångströma, na tyle dokładnie, by dostrzec łańcuchy boczne aminokwasów i poszczególne zasady DNA. Obrazy ujawniły wirusową polimerazę RNA chwytającą DNA promotora, przy czym VITF‑3 tworzył ciasny pierścień wokół bogatego w AT odcinka DNA tuż przed miejscem startu. Ten pierścień silnie wygina DNA o około 90 stopni i prowadzi je do szczeliny w polimerazie. Jednocześnie wirusowe enzymatyczne białko kapujące — odpowiedzialne za dodanie ochronnej czapeczki na końcu 5′ wirusowego RNA — zadokowane jest przy polimerazie, gotowe modyfikować nowe transkrypty natychmiast po ich pojawieniu się.
Mechanizm ładowania zacisku zapożyczony w sensie
Łącząc strukturalne migawki z testami biochemicznymi, badanie proponuje, że wirusowa polimeraza RNA aktywnie zakłada VITF‑3 na DNA, działając jak „ładowacz zacisku”. Najpierw polimeraza wiąże się z promotorem pośrednim i pomaga rozchylić pierścień VITF‑3. Potem, razem z enzymem kapującym, zamyka pierścień wokół regionu bogatego w AT, zaciskając kompleks na miejscu. DNA jest naparowywane w pobliżu miejsca startu, a polimeraza bezpośrednio odczytuje krótki czteroznakowy sygnał (motyw TAAA), który dokładnie wyznacza miejsce rozpoczęcia syntezy RNA. W miarę wydłużania się RNA, podąża ono tą samą ścieżką, którą zajmowała część VITF‑3 w początkowym kompleksie, więc powstające RNA prawdopodobnie wypycha VITF‑3, umożliwiając polimerazie opuszczenie promotora i kontynuację wzdłuż genu, podczas gdy VITF‑3 może pozostać, by przyspieszyć ponowne użycie tego samego promotora.
Co to oznacza dla zrozumienia i celowania w poxwirusy
Mówiąc prosto, praca ta pokazuje, że wirus Vaccinia przeprojektował uniwersalny moduł kontroli genów w zacisk, który chwyta DNA tylko wtedy, gdy jego własna polimeraza RNA każe mu to zrobić. Ta sprytna modyfikacja pozwala wirusowi używać jednej podstawowej enzymaty do prowadzenia trzech bardzo różnych programów transkrypcyjnych, po prostu przez podmianę pomocników zależnych od etapu. Ponieważ tego rodzaju czynniki są zachowane w wielu poxwirusach, w tym patogenach ludzkich, nowo odkryty mechanizm ładowania zacisku i unikalny pierścień VITF‑3 oferują konkretne strukturalne cele dla strategii przeciwwirusowych mających na celu zakłócenie zdolności wirusa do harmonogramowania i kontroli swoich genów podczas infekcji.
Cytowanie: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Słowa kluczowe: transkrypcja poxwirusów, wirus Vaccinia, polimeraza RNA, rozpoznawanie promotora, czynniki transkrypcyjne