Clear Sky Science · pl
Dehydrogenaza fosfoglicerynianowa pośrednicząca w przekształceniu seryny zaostrza nadmierne zapalenie makrofagów w mysim zapaleniu płuc wywołanym Pseudomonas aeruginosa
Kiedy obrońcy organizmu idą za daleko
Zapalenie płuc wywołane bakterią Pseudomonas aeruginosa jest wyjątkowo trudne do leczenia, zwłaszcza u osób z osłabionymi płucami. Antybiotyki atakują mikroby, ale choroba ta bywa śmiertelna nie tylko z powodu samych bakterii, lecz także dlatego, że odpowiedź immunologiczna organizmu wymyka się spod kontroli. Badanie to ujawnia, jak jeden metaboliczny „przełącznik” w komórkach odpornościowych może przesunąć je z roli pożytecznej do szkodliwej — i sugeruje, że modulacja diety lub przemiany komórkowej może złagodzić zagrażające życiu zapalenie płuc.
Niebezpieczny taniec między zarazkiem a układem odpornościowym
Pseudomonas aeruginosa to pospolita bakteria Gram‑ujemna, która może wtargnąć do dolnych dróg oddechowych i wywołać ciężkie zapalenie płuc. Zwykle rezydujące w płucach komórki odpornościowe zwane makrofagami patrolują pęcherzyki płucne, pożerając najeźdźców i alarmując innych komórek za pomocą sygnałów chemicznych. Jednak przy dużym ładunku bakteryjnym komórki te rekrutują z krwiobiegu liczne dodatkowe makrofagi. W efekcie powstaje burza zapalnych mediatorów, które uszkadzają delikatną tkankę płuc, zaburzają procesy naprawcze i w ciężkich przypadkach prowadzą do niewydolności oddechowej i śmierci. Autorzy postawili pytanie, czy wewnętrzny metabolizm tych makrofagów może napędzać tę szkodliwą nadreakcję.
Enzym metaboliczny na gorącym krześle
Zespół skupił się na enzymie zwanym dehydrogenazą fosfoglicerynianową (PHGDH), kluczowym punkcie wejścia do szlaku, którym komórki syntetyzują aminokwas serynę z glukozy. W mysim modelu zakażenia płuc Pseudomonasem poziomy i aktywność PHGDH gwałtownie wzrosły w płucach, szczególnie w makrofagach. Gdy myszy leczono małocząsteczkowym inhibitorem PHGDH lub gdy gen PHGDH był usunięty specyficznie w komórkach mieloidalnych (w tym makrofagach), zwierzęta radziły sobie lepiej: przeżywały dłużej, miały mniejsze uszkodzenia płuc, nosiły mniej bakterii i wytwarzały mniejsze ilości silnie zapalnych cytokin, takich jak interleukina‑6 i interleukina‑1β. Na poziomie komórkowym blokada PHGDH przesuwała makrofagi z wyraźnie prozapalnego stanu, nie zwiększając jednocześnie przeciwnego, naprawczego fenotypu.
Podsycanie ognia: seryna i nadaktywne obwody sygnałowe
Dalej badacze wykazali, że zakażenie przeprogramowuje makrofagi, kierując więcej glukozy do syntezy seryny, a sama seryna z kolei potęguje stan zapalny. Dodatkowa seryna sprawiała, że makrofagi wydzielały więcej zapalnych cytokin i eksponowały więcej markerów aktywacji na powierzchni, podczas gdy diety ograniczające serynę chroniły zakażone myszy i obniżały liczbę bakterii. Mechanistycznie seryna zasilała cykl „jednego węgla”, który dostarcza grup metylowych komórce — chemicznych znaczników używanych w regulacji epigenetycznej. To zwiększało konkretną modyfikację histonów, trimetylację H3K27, w pobliżu genu hamującego białka DUSP4, które normalnie pomaga wyłączyć szlak sygnałowy ERK1/2. Gdy DUSP4 był stłumiony, ERK1/2 pozostawał włączony, wzmacniając sygnały zapalne. Hamowanie PHGDH lub obniżenie poziomu seryny odwracało ten łańcuch, przywracało DUSP4 i zmniejszało fosforylację ERK1/2.
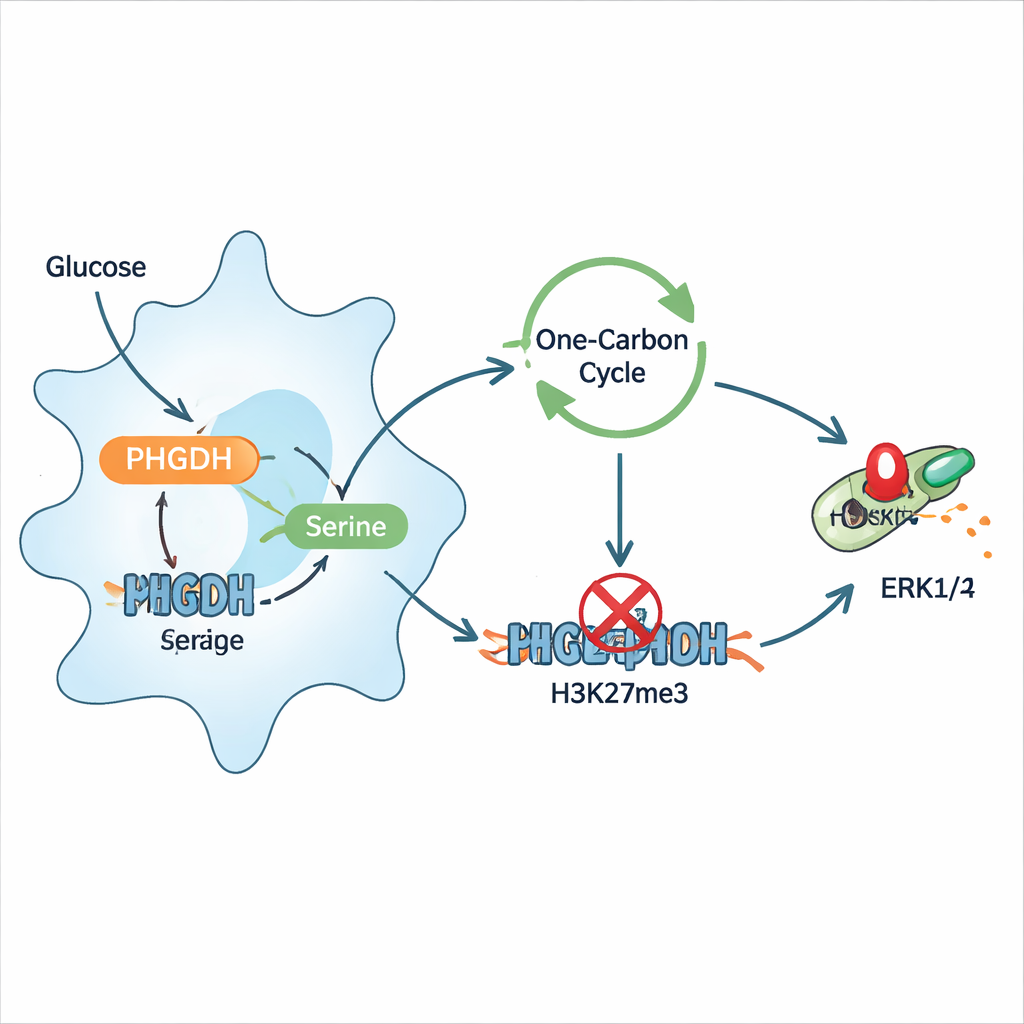
Przywracanie równowagi makrofagów bez osłabiania obrony
Co ważne, stłumienie PHGDH nie sparaliżowało po prostu układu odpornościowego. W rzeczywistości makrofagi pozbawione PHGDH były lepsze w pochłanianiu i zabijaniu Pseudomonas we wczesnej fazie zakażenia, jednocześnie wytwarzając mniej szkodliwych cytokin. Przeniesienie tych makrofagów pozbawionych PHGDH do normalnych myszy poprawiało wyniki po wyzwaniu bakteryjnym, co podkreśla, że korzyści wynikały z przeprogramowania odpowiedzi gospodarza, a nie z bezpośredniego działania przeciw drobnoustrojowi. Praca sugeruje również, że diety bogate w serynę mogą niezamierzenie sprzyjać hiperzapaleniu w trakcie ciężkiego bakteryjnego zapalenia płuc, podczas gdy kontrolowane ograniczenie seryny może być nowym sposobem ograniczenia nadmiernych uszkodzeń płuc.
Co to oznacza dla leczenia trudno uleczalnego zapalenia płuc
Mówiąc przystępnie, badanie pokazuje, że niektóre makrofagi w zapaleniu płuc wywołanym przez Pseudomonas spalają cukier w sposób prowadzący do nadprodukcji seryny, a ten metaboliczny objazd blokuje ich mechanizmy prozapalne w stanie nadmiernej aktywności. Blokując enzym PHGDH lub ograniczając serynę, badacze byli w stanie złagodzić tę nadreakcję, chronić tkankę płucną i jednocześnie pozwolić komórkom odpornościowym na usuwanie bakterii. Choć badania prowadzone są na myszach i daleko im do zastosowań klinicznych, wskazują obiecującą ideę: łączenie tradycyjnych antybiotyków z lekami lub podejściami dietetycznymi subtelnie modyfikującymi metabolizm komórek odpornościowych może przekształcić niszczycielski pożar odpornościowy w kontrolowany, bakteriobójczy płomień.
Cytowanie: Chen, R., Zeng, R., Shi, M. et al. Phosphoglycerate dehydrogenase-mediated serine reprogramming aggravates macrophage hyperinflammation in murine Pseudomonas aeruginosa pneumonia. Nat Commun 17, 1944 (2026). https://doi.org/10.1038/s41467-026-69539-1
Słowa kluczowe: Pneumonia Pseudomonas, metabolizm makrofagów, biosynteza seryny, zapalenie płuc, PHGDH