Clear Sky Science · pl
Syntetyczna komórka z zintegrowanym samopowielaniem DNA i biosyntezą lipidów
Budowanie życia od zera
Co sprawia, że żywa komórka to coś więcej niż tylko worek z cząsteczkami? Jedną z odpowiedzi jest jej zdolność do kopiowania informacji genetycznej i wytwarzania własnej ochronnej błony. To badanie stanowi duży krok w kierunku odtworzenia tej umiejętności w laboratorium. Autorzy zaprojektowali maleńkie pęcherzyki tłuszczu, znane jako liposomy, które potrafią odczytać fragment DNA, skopiować go i wytworzyć nowy materiał błonowy — wszystko wewnątrz tego samego miniaturowego przedziału. Ich praca przybliża nas do sztucznych komórek, które mogą rosnąć, adaptować się, a być może pewnego dnia samodzielnie ewoluować.
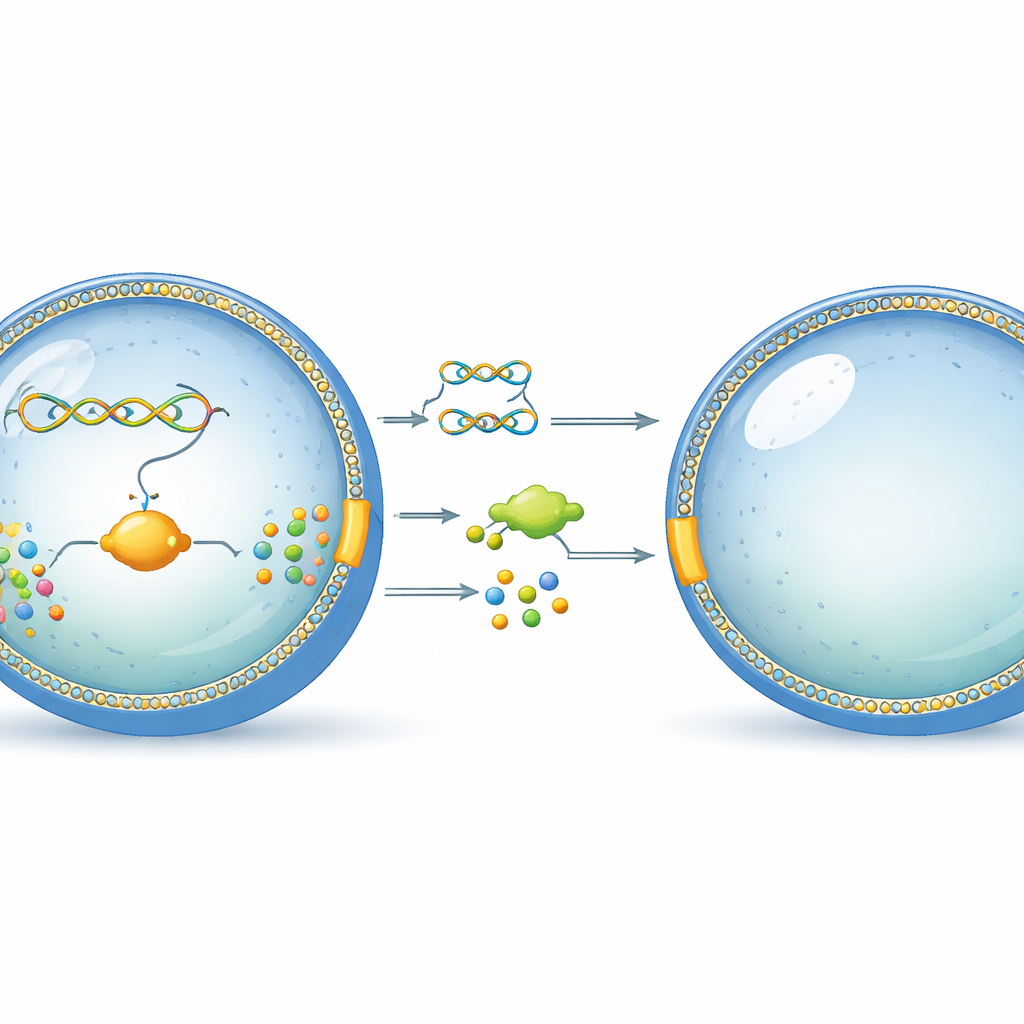
Maleńki pęcherzyk działający jak komórka
Naukowcy zaczynają od prostych, wielkości komórkowej pęcherzyków z fosfolipidów — tego samego typu cząsteczek, które tworzą zewnętrzną powłokę prawdziwych komórek. Do tych pęcherzyków wkładają starannie zaprojektowany odcinek DNA i zestaw oczyszczonych maszyn komórkowych zdolnych do odczytu DNA i wytwarzania białek. To układ zwany systemem ekspresji pozakomórkowej, działający jak odchudzony rdzeń żywej komórki, potrafiący przekształcać informację genetyczną w funkcjonalne molekuły bez udziału żywego organizmu. Kluczowa idea polega na umieszczeniu wszystkiego wewnątrz liposomu, tak aby program genetyczny i jego produkty pozostawały razem, podobnie jak w naturalnej komórce.
Specjalny program DNA z dwoma zadaniami
W sercu ich syntetycznej komórki znajduje się specjalnie skonstruowana cząsteczka DNA, którą autorzy nazywają DNArep-PLsyn. Ten DNA niesie instrukcje dla sześciu białek. Dwa z nich pochodzą od wirusa atakującego bakterie i razem potrafią kopiować sam DNA, tworząc wbudowany moduł samopowielania. Pozostałe cztery pochodzą od bakterii jelitowej E. coli i tworzą łańcuch reakcji przekształcający proste substraty w konkretny fosfolipid wykorzystywany w błonach. Aby zmontować ten nietypowy genom, zespół musiał posklejać fragmenty DNA w probówkach i w komórkach drożdży, a następnie przekształcić wynik w liniowy odcinek DNA, który maszyneria wirusowa rozpoznaje i może replikować.
Wytwarzanie i testowanie aktywności syntetycznej
Gdy DNA i mechanizmy wytwarzania białek zostaną zamknięte wewnątrz liposomów, pęcherzyki są ogrzewane do różnych temperatur i pozostawione do pracy. Zespół sprawdza następnie, co zaszło, używając markerów fluorescencyjnych: jedna barwnik świeci po związaniu się z DNA, ujawniając ilość materiału genetycznego, a inny przyłącza się do nowego fosfolipidu, jeśli zostanie wyprodukowany i wbudowany w błonę. Za pomocą cytometrii przepływowej i mikroskopii o wysokiej rozdzielczości mogą analizować dziesiątki tysięcy pojedynczych pęcherzyków. Stwierdzają, że wiele pęcherzyków skutecznie kopiuje genom, inne wytwarzają nowe elementy budulcowe membrany, a mniejsza, lecz istotna część osiąga oba te zadania jednocześnie. Dodatkowe testy z użyciem ilościowego oznaczania DNA i spektrometrii mas potwierdzają, że pełnej długości genom jest amplifikowany i że nowe cząsteczki fosfolipidów są rzeczywiście syntetyzowane, choć w umiarkowanych ilościach.
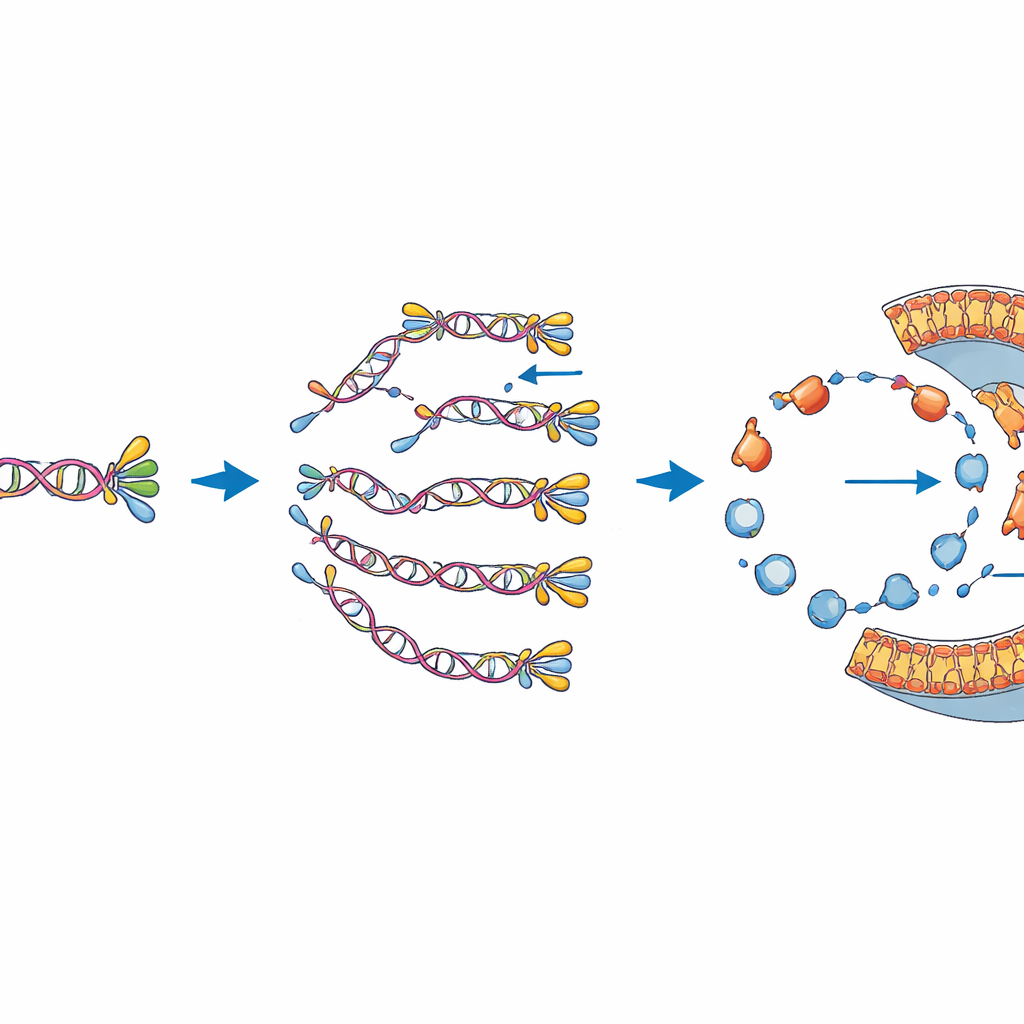
Zrównoważenie dwóch istotnych zadań
Autorzy badają następnie, jak te dwie funkcje wpływają na siebie nawzajem. Wyłączając lub włączając chemię kopiowania DNA albo syntezy błony poprzez kontrolę niezbędnych składników, pokazują, że każdy z procesów może działać w dużej mierze bez zakłócania drugiego. Jednak gdy oba moduły są kodowane na tym samym DNA, strona syntezy błony okazuje się bardziej krucha: mniej pęcherzyków wykazuje tę aktywność w porównaniu z pęcherzykami zawierającymi jedynie geny związane z lipidami. Podobnie połączony genom nie replikuje się tak efektywnie, jak mniejsza wersja zawierająca tylko geny replikacyjne. Sugeruje to, że nawet w tym uproszczonym systemie występuje konkurencja o wspólne zasoby i fizyczne miejsce na DNA, co odzwierciedla kompromisy obserwowane w prawdziwych komórkach.
Przygotowanie do ewolucji w probówce
Aby pójść dalej niż jednorazowa demonstracja, zespół zaprojektował system tak, by w zasadzie można go było ulepszać poprzez ewolucję. Wytwarzają czystsze, bardziej niezawodne wersje DNA przy użyciu plazmidów hodowanych w drożdżach i bakteriach, co zwiększa odsetek w pełni funkcjonalnych syntetycznych komórek. Pokazują też, że możliwe jest enkapsulowanie, selekcjonowanie i odzyskiwanie genomów z pęcherzyków, które wykonują zarówno kopiowanie DNA, jak i syntezę błony. To przygotowuje grunt pod przyszłe cykle, w których nieco odmienne genomy będą konkurować, a te działające lepiej będą wzbogacane i kopiowane.
Dlaczego to ma znaczenie dla rozumienia życia
Mówiąc prosto, badacze zbudowali mikroskopijny pęcherzyk, który potrafi odczytać własny przepis, wykonać jego kopie i użyć ich do naprawy i rozbudowy swojej zewnętrznej powłoki. Chociaż te syntetyczne komórki nie potrafią jeszcze znacząco rosnąć ani dzielić się jak organizmy żywe, praca ta pokazuje, że podstawowe cechy życia — przechowywanie informacji, samokopiowanie i podstawowa samobudowa — można połączyć w prostym, kontrolowalnym układzie. To kładzie ważne podstawy do badania, jak życie mogło powstać z nieożywionej chemii, oraz do inżynierii sztucznych komórek wykonujących użyteczne zadania, od inteligentnego dostarczania leków po samoodnawiające się miniaturowe fabryki.
Cytowanie: Restrepo Sierra, A.M., Ramirez Gomez, F., van Tongeren, M. et al. A synthetic cell with integrated DNA self-replication and lipid biosynthesis. Nat Commun 17, 2727 (2026). https://doi.org/10.1038/s41467-026-69531-9
Słowa kluczowe: komórki syntetyczne, samopowielanie DNA, biosynteza lipidów, życie sztuczne, biologia od podstaw