Clear Sky Science · pl
Gęstość ładunku zhydratowanego metalu jako uniwersalny deskryptor wyjaśniający mechanistyczne różnice w aktywacji periodianu w kierunku degradacji zanieczyszczeń
Oczyszczanie wody za pomocą „inteligentnej” chemii
Wiele leków i związków przemysłowych przedostaje się przez konwencjonalne oczyszczalnie i trafia do rzek oraz wody pitnej. W badaniu tym zbadano obiecującą metodę rozkładu takich uporczywych zanieczyszczeń przy użyciu powszechnego środka utleniającego — periodianu — i pokazano, że prosta właściwość jonów metali w wodzie pozwala przewidzieć, jak skuteczna i jak bezpieczna będzie ta chemia. Zrozumienie tej zasady może pomóc inżynierom w projektowaniu czystszych, bardziej wydajnych systemów oczyszczania dla różnych, rzeczywistych wód.
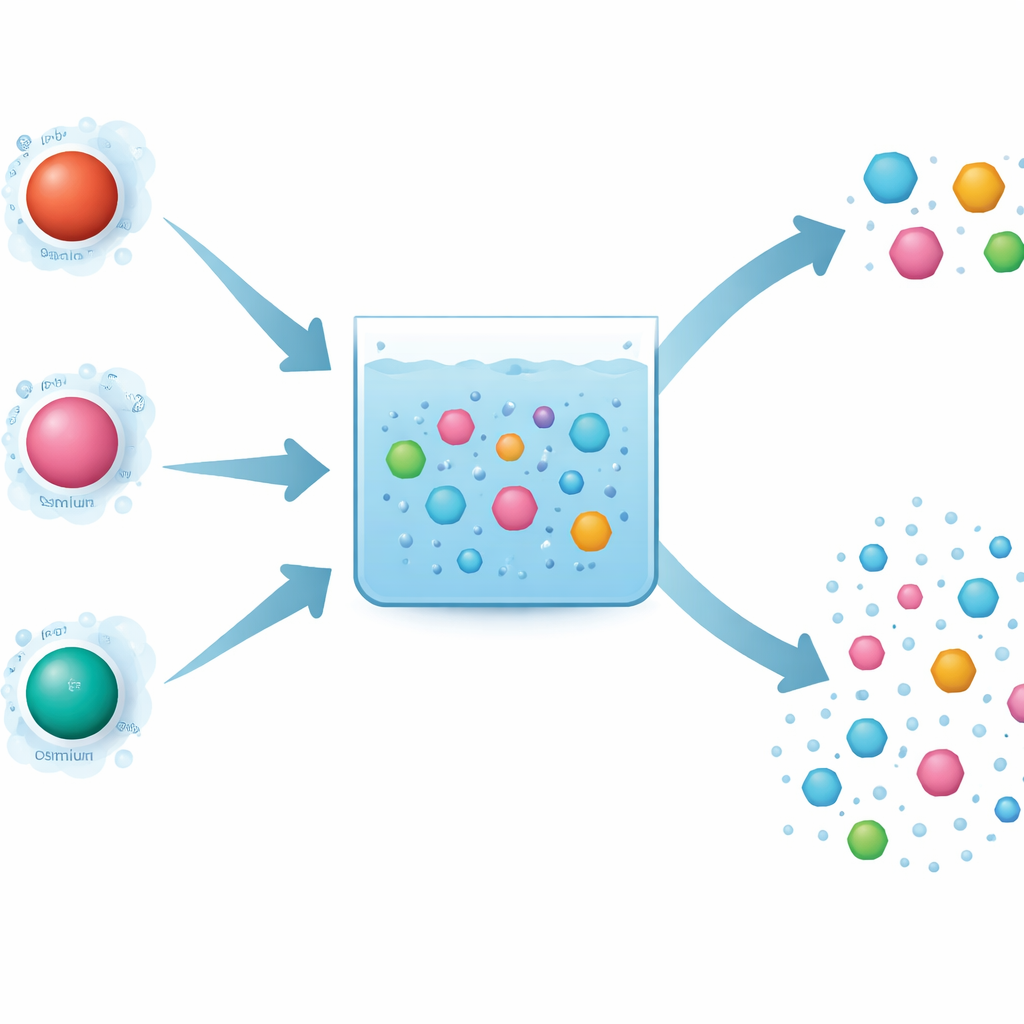
Dlaczego wybór metalu ma znaczenie dla rozkładu zanieczyszczeń
Zaawansowane procesy utleniania wykorzystują silne reaktywne gatunki do rozrywania cząsteczek organicznych. Periodian jest jednym z takich utleniaczy i może zostać „włączony” przez rozpuszczone jony metali. Autorzy porównali trzy blisko spokrewnione metale — żelazo, ruten i osm — które należą do tej samej kolumny układu okresowego i można by oczekiwać, że będą zachowywać się podobnie. Wszystkie trzy potrafią aktywować periodian i pomagać w niszczeniu testowego zanieczyszczenia, karbamazepiny. Eksperymenty wykazały jednak uderzające różnice: ruten działał niezwykle szybko, żelazo wolniej, a osm zajmował pozycję pośrednią. Co więcej, osm usuwał szeroką gamę zanieczyszczeń bez wyraźnych preferencji, podczas gdy żelazo i ruten były wybiórcze, atakując niektóre związki znacznie chętniej niż inne.
Dwie zupełnie różne ścieżki reakcji
Aby odkryć przyczyny tych różnic, zespół śledził, jakie krótkotrwałe gatunki utleniające pojawiają się w każdym układzie metal–periodian. W układach z żelazem i rutenem dominowały jednostki „metal–tlen”, które działają jak precyzyjne narzędzia, przekazując atom tlenu bezpośrednio do określonych miejsc w cząsteczce zanieczyszczenia. Te ścieżki miały skłonność do tworzenia produktów epoksydowych — struktur pierścieniowych, które dodają pojedynczy atom tlenu — co wskazuje na dużą selektywność reakcji. W układzie osmowym głównymi aktorami były jednak rodniki hydroksylowe, niezwykle reaktywne fragmenty, które atakują niemal każdą pobliską cząsteczkę organiczną, prowadząc do produktów hydroksylowanych i małych fragmentów po otwarciu pierścienia. Testy z sondami chemicznymi i spektroskopią spin‑trap potwierdziły, że to rodniki hydroksylowe i pokrewne reaktywne formy tlenu, a nie wysokozmatrycowe jednostki osm–tlen, odpowiadają za większość rozkładu zanieczyszczeń w obecności osmu.
Jak warunki wodne kształtują reakcje
Zespół zbadał także, jak pH i składniki naturalnej wody wpływają na te procesy. W przypadku osmu usuwanie zanieczyszczeń nasilało się wraz z alkalizacją wody, gdzie koordynacja dodatkowych jonów hydroksylowych wokół metalu ułatwia przemieszczanie elektronów i tworzenie się rodników. Przy wysokich dawkach metalu lub utleniacza układ osmowy ulegał jednak „samo‑tłumieniu”, ponieważ nowo powstałe rodniki były pochłaniane przez nadmiar reagentów zamiast przez zanieczyszczenia. Naturalna materia organiczna, która często zakłóca reakcje utleniania, miała zaskakująco niewielki wpływ na degradację napędzaną przez osm, co sugeruje, że ścieżka rodnikowa pozostaje odporna w realistycznych wodach. Dla porównania, żelazo i ruten działały najlepiej w warunkach kwaśnych, a naturalna materia organiczna silnie hamowała ich aktywność przez pochłanianie kluczowych utleniaczy metal–tlen.
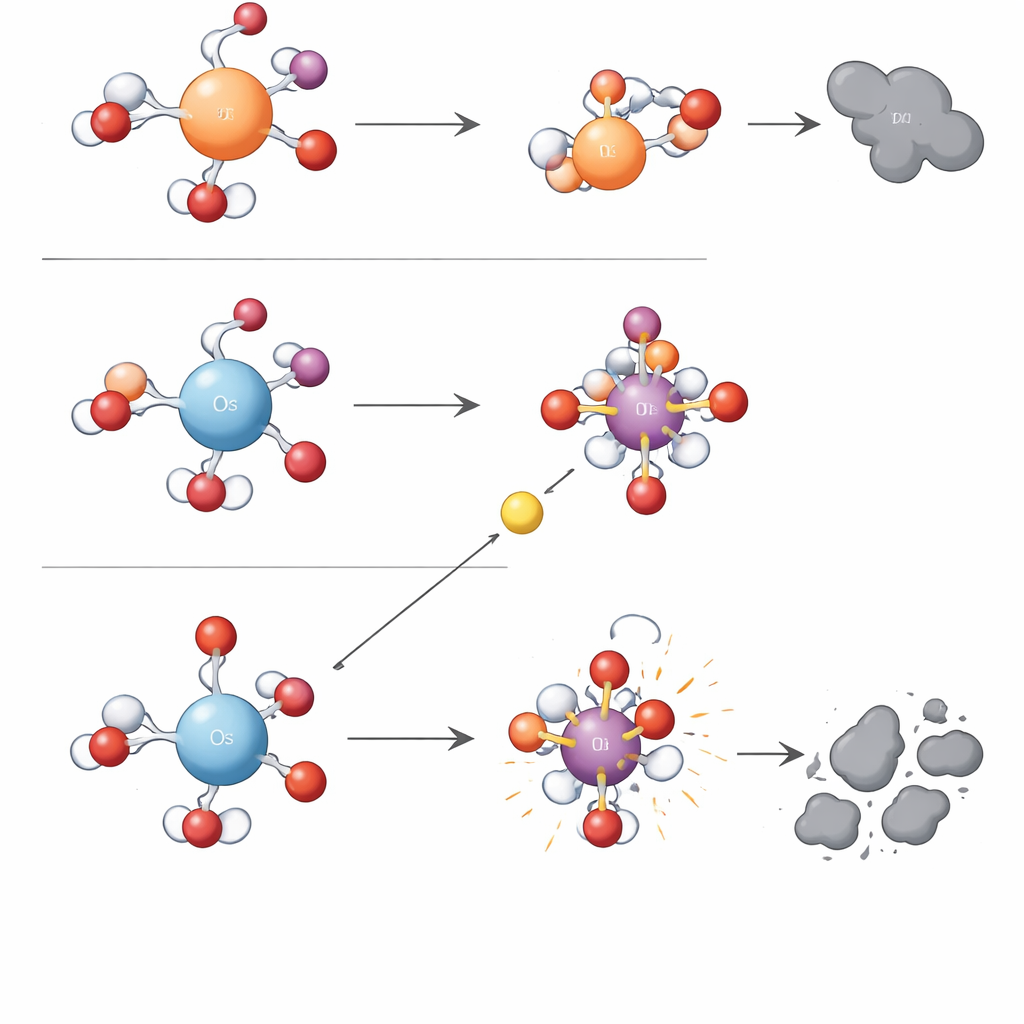
Prosta zasada ładunku stojąca za złożoną chemią
Aby wyjść poza metodę prób i błędów, badacze sięgnęli po obliczenia kwantowo‑chemiczne. Odkryli, że jedna cecha elektronowa — dodatnia gęstość ładunku zhydratowanego centrum metalu — potrafi wyjaśnić rozdział na oba typy reakcji. Osm w wodzie nosi wyżej skoncentrowany ładunek dodatni niż żelazo czy ruten. To silne dodatnie centrum mocno przyciąga związany z nim atom tlenu, czyniąc jednostkę metal–tlen stabilną, ale powolną w bezpośrednim przekazywaniu tlenu. Jednocześnie silne przyciąganie do pobliskiej wody i jonów obniża barierę energetyczną dla kroków jednoelektronowych, które ostatecznie zrywają wiązanie tlenu w periodianie i uwalniają rodniki hydroksylowe. Metale o niższej gęstości ładunku, jak żelazo i ruten, trzymają elektrony silniej, sprzyjając tworzeniu i wykorzystaniu selektywnych utleniaczy metal–tlen zamiast wolnych rodników. Autorzy nazywają tę organizującą ideę „Mechanizmem Kontroli Gęstości Ładunku” i pokazują, że racjonalizuje ona także trendy opisane dla innych metali, takich jak mangan.
Projektowanie lepszego oczyszczania wody za pomocą jednego pokrętła
Łącząc trudny zestaw obserwacji z jednym prostym deskryptorem — gęstością ładunku metalu otoczonego wodą — praca ta oferuje mapę drogową do dostosowywania zaawansowanych procesów utleniania. Metale o wysokiej gęstości ładunku powinny sprzyjać szerokiemu, rodnikowemu rozkładowi złożonych mieszanin zanieczyszczeń, zwłaszcza w wodach zasadowych lub bogatych w związki organiczne. Metale o niższej gęstości ładunku nadają się lepiej tam, gdzie pożądana jest selektywna, łagodniejsza oksydacja — na przykład do przekształcania konkretnych zanieczyszczeń bez nadreakcji z innymi składnikami. W praktyce oznacza to, że chemicy i inżynierowie mogą przesiewać lub projektować katalizatory do oczyszczania wody, regulując, jak ściśle centra metaliczne utrzymują ładunek w swoim wodnym otoczeniu, zamiast optymalizować każdy system metodą prób i błędów.
Cytowanie: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Słowa kluczowe: zaawansowane procesy utleniania, aktywacja periodianu, oczyszczanie wody, kataliza metali przejściowych, rodniki hydroksylowe