Clear Sky Science · pl
Wysokoprzepustowy przepływ pracy chemoproteomiki do profilowania dynamiki cytrulinizacji białek
Dlaczego zmiana składników białek ma znaczenie
Nasze komórki nieustannie dostrajają funkcje białek, dodając drobne chemiczne modyfikacje po ich syntezie. Jedna z takich modyfikacji, zwana cytrulinizacją, subtelnie zmienia ładunek popularnego aminokwasu i może przeorganizować sposób fałdowania białek, przyczepiania się do DNA lub interakcji z innymi cząsteczkami. Te drobne poprawki są coraz częściej powiązane z chorobami autoimmunologicznymi, infekcjami, rakiem i funkcjami mózgu — jednak są niezwykle trudne do wykrycia. W badaniu opisano wysokoprzepustowy przepływ pracy w laboratorium, który wreszcie umożliwia mapowanie cytrulinizacji w tysiącach białek, ujawniając, kiedy i gdzie pojawia się w tkankach i komórkach układu odpornościowego.
Ukryty przełącznik na białkach
Cytrulinizacja zachodzi, gdy enzymy nazywane PAD modyfikują chemicznie aminokwas argininę, usuwając jego dodatni ładunek. Ta pozornie niewielka zmiana może poluzować upakowanie DNA, zmienić sztywność białek strukturalnych albo wpłynąć na rozpoznawanie tkanek przez układ odpornościowy. Nieprawidłowa cytrulinizacja jest związana z reumatoidalnym zapaleniem stawów, zaburzeniami neurodegeneracyjnymi, infekcjami wirusowymi i rakiem. Jednak białka cytrulinizowane są rzadkie i łatwe do pomylenia z innymi, częstszymi modyfikacjami, więc standardowe metody spektrometrii mas często je pomijają. W efekcie badacze mieli dotąd jedynie fragmentaryczny obraz „cytrulinomu” — pełnego zestawu białek poddanych cytrulinizacji.
Strategia „oznacz i wyłap” w dwóch krokach
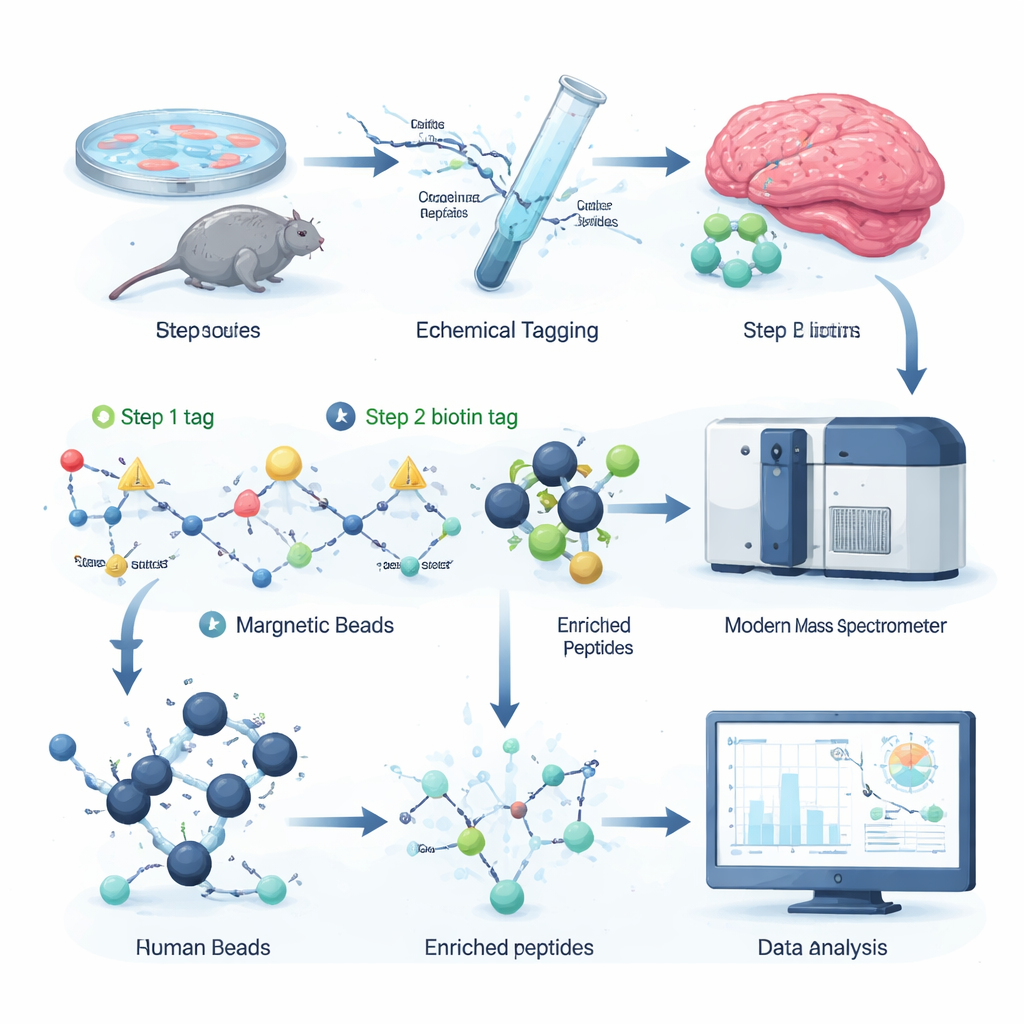
Autorzy opracowali chemiczną strategię znakowania, która selektywnie przyłącza odłączalny „uchwyt” do miejsc cytrulinizacji w peptydach, czyli fragmentach białek analizowanych przez spektrometrię mas. W pierwszym kroku mała reaktywna cząsteczka rozpoznaje cytrulinę i instaluje drobny znacznik. W drugim kroku naznaczany jest większy znacznik biotynowy metodą „click”, co pozwala wyłapać znakowane peptydy z mieszaniny przy użyciu kulek streptawidyny, powszechnego narzędzia biochemicznego. Delikatne traktowanie chemiczne odcina następnie masywną część znacznika, pozostawiając niewielką, dobrze określoną zmianę masy, którą spektrometr mas może łatwo wykryć. Ponieważ wszystkie odczynniki są komercyjnie dostępne, a cały protokół mieści się w płytach 96‑dołkowych, przepływ pracy jest szybki, skalowalny i zgodny z istniejącymi zestawami do proteomiki.
Widzieć więcej z cytrulinomu
Poprzez dosypanie znanych peptydów cytrulinizowanych do ekstraktów komórkowych i systematyczne ich rozcieńczanie, zespół wykazał, że ich strategia wzbogacania zwiększa sygnał peptydów cytrulinizowanych ponad dziesięciokrotnie, nawet gdy stanowią one mniej niż jedną z tysiąca cząsteczek. W złożonych próbkach liczba wykrytych miejsc cytrulinizacji i ich zmierzone intensywności wzrosły znacząco po wzbogaceniu. Zastosowanie metody do tkanki mózgowej myszy ujawniło dwukrotnie do trzykrotnie więcej odrębnych miejsc cytrulinizacji niż poprzednie, zaawansowane podejście, w tym wiele na podstawowym białku mieliny, które izoluje włókna nerwowe, oraz na białkach zaangażowanych w komunikację synaptyczną. Sugeruje to, że cytrulinizacja może wpływać zarówno na sposób, w jaki komórki nerwowe przesyłają sygnały, jak i na utrzymanie połączeń w mózgu.
Komórki odpornościowe tworzące lepkie sieci z białek
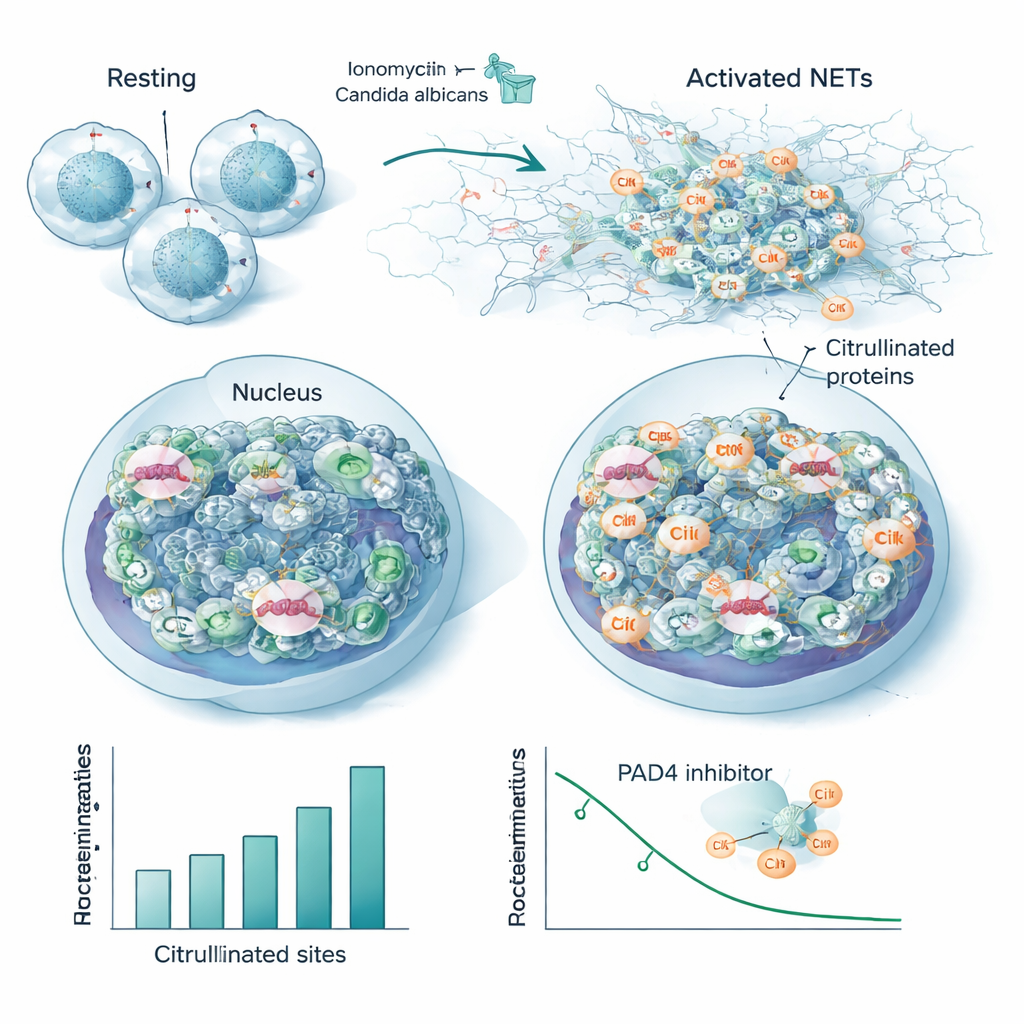
Neutrofile, typ pierwszej linii białych krwinek, mogą zwalczać intruzów, uwalniając lepkie sieci z DNA i białek zwane neutrofilowymi pułapkami zewnątrzkomórkowymi (NET). Tworzenie NET zależy od PAD4, enzymu cytrulinizującego, który poluzowuje chromatynę, aby DNA mogło wypłynąć na zewnątrz. Korzystając z nowego przepływu pracy, badacze śledzili, jak cytrulinizacja zmienia się w ludzkich neutrofilach eksponowanych na rosnące dawki chemicznego aktywatora. Wykryli do 1700 cytrulinizowanych fragmentów peptydowych w ramach 580 białek, z setkami miejsc rosnących lub malejących w sposób zależny od dawki, podczas gdy całkowite poziomy białek pozostawały stałe. Histony — białka porządkujące DNA — wykazywały szeroko zakrojoną cytrulinizację, nie tylko w kilku klasycznych miejscach, a warianty histonu łącznikowego H1 były szczególnie modyfikowane. Białka strukturalne takie jak regulatory aktyny i lamin B, kształtujący otoczkę jądrową, również stały się mocno cytrulinizowane, co wskazuje na skoordynowane rozluźnienie zarówno chromatyny, jak i rusztowań komórkowych podczas uwalniania NET.
Rdzeniowy sygnatur cytrulinizacji w infekcji
Aby naśladować rzeczywistą infekcję, zespół stymulował neutrofile zabitym termicznie Candida albicans, powszechnym patogenem grzybiczym. Chociaż doprowadziło to do mniejszej liczby zmodyfikowanych miejsc ogółem niż silny aktywator chemiczny, olbrzymia większość cytrulinizowanych białek i pozycji pokrywała się między dwoma czynnikami wywołującymi. To nakładanie się definiuje zachowany „rdzeniowy cytrulinom” związany z tworzeniem NET, obejmujący wiele białek jądrowych i cytoszkieletowych oraz kilka znanych autoantygenów — tych samych celów przeciwciał w chorobach autoimmunologicznych. Gdy badacze dodali lek blokujący PAD4, wiele z tych samych miejsc straciło cytrulinizację w sposób zależny od dawki, co bezpośrednio wiąże je z aktywnością enzymu i sugeruje, że mogą służyć jako czułe wskaźniki inhibicji PAD4.
Co to oznacza dla zdrowia i chorób
Przekształcając ulotną modyfikację w mierzalny sygnał, ten przepływ pracy umożliwia określenie, gdzie i kiedy zachodzi cytrulinizacja w tkankach, odpowiedziach odpornościowych i modelach chorobowych. Dla niespecjalistów kluczowy przekaz jest taki, że cytrulinizacja działa jak subtelny molekularny ściemniacz na białkach, a możliwość obserwowania jej wzorców w wysokiej rozdzielczości może pomóc wyjaśnić, jak zaczynają się choroby autoimmunologiczne, jak infekcje przekształcają komórki odpornościowe oraz jak białka mózgowe zmieniają się w czasie. Skalowalność metody i oparcie na standardowym sprzęcie laboratoryjnym sprawiają, że może być szeroko wdrożona, otwierając drogę do odkrywania nowych celów lekowych, diagnostyki precyzyjnej i głębszego zrozumienia, jak drobne chemiczne poprawki mogą mieć duże konsekwencje biologiczne.
Cytowanie: Meelker González, R., Laposchan, S., Riedel, E. et al. High-throughput chemical proteomics workflow for profiling protein citrullination dynamics. Nat Commun 17, 1982 (2026). https://doi.org/10.1038/s41467-026-69490-1
Słowa kluczowe: cytrulinizacja, choroba autoimmunologiczna, neutrofilowe pułapki zewnątrzkomórkowe, spektrometria mas, modyfikacja potranslacyjna