Clear Sky Science · pl
Patofizjologiczne znaczenie upośledzonej acetylacji histonu H3K14 zależnej od KAT7 podczas niedoboru cynku
Dlaczego drobne składniki odżywcze mają znaczenie dla naszego zdrowia
Cynk to pierwiastek śladowy, którego nasze ciało potrzebuje jedynie w niewielkich ilościach, a mimo to cicho wspiera setki białek niezbędnych do prawidłowego funkcjonowania komórek. Gdy cynku brakuje — z powodu diety, choroby lub starzenia się — wiązano to z problemami od zahamowanego wzrostu po osłabioną odporność i stłuszczenie wątroby. W tym badaniu postawiono głębsze pytanie: jak komórki rzeczywiście wykrywają, że cynku jest za mało, i w jaki sposób ten niedobór przekłada się na długotrwałe zmiany aktywności genów i zdrowia narządów?
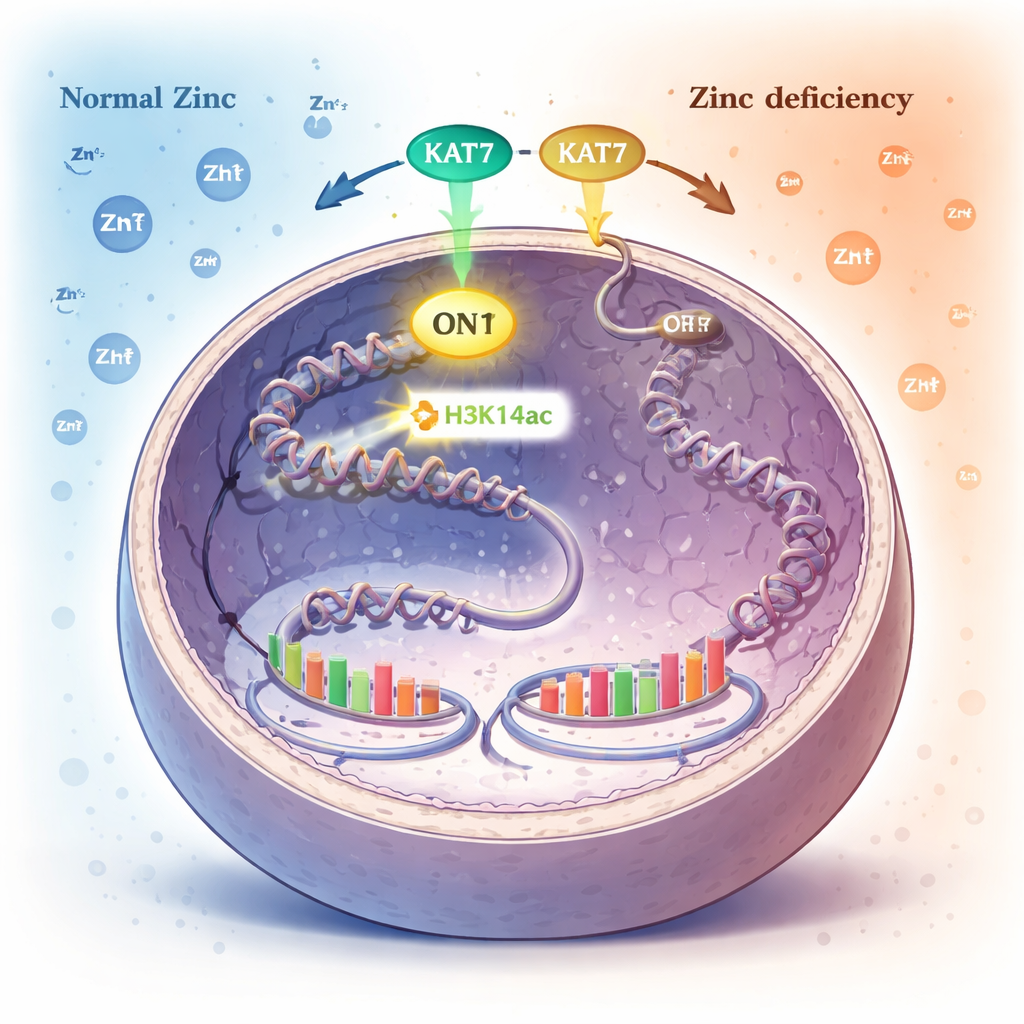
Chemiczny znacznik na opakowaniu DNA jako wewnętrzny alarm cynkowy
W jądrze DNA jest nawinięte na białkowe szpule zwane histonami. Komórki kontrolują, które geny są aktywne, dodając lub usuwając drobne chemiczne znaczniki na tych histonach. Jeden z takich znaczników, zwany acetylacją w określonym miejscu na histonie H3 (H3K14ac), jest dodawany przez enzym o nazwie KAT7. Autorzy odkryli, że gdy cynku staje się niewiele, poziom tego znacznika H3K14ac spada dramatycznie, podczas gdy wiele innych powszechnych modyfikacji histonów pozostaje bez zmian. Wskazywało to na H3K14ac i na enzym KAT7, który go tworzy, jako kluczowy sensor stanu cynku.
Jak cynk utrzymuje kluczowy enzym włączony
Systematycznie wyłączając różne enzymy, badacze wykazali, że KAT7 jest głównym źródłem H3K14ac w komórkach ludzkich. KAT7 zawiera w swoim miejscu aktywnym niewielką strukturę wiążącą cynk. Gdy komórki wprowadzono w stan niedoboru cynku, zdolność KAT7 do umieszczania znaku H3K14ac malała, mimo że sam białko pozostawało w jądrze i nadal współdziałało ze swoimi partnerami pomocniczymi. Szczegółowe testy z oczyszczonymi fragmentami KAT7 wykazały, że prawidłowo związany cynk w tym regionie jest niezbędny dla jego aktywności; zaburzenie wiązania cynku wyłączało enzym, a staranne dodanie cynku przywracało jego funkcję. W istocie KAT7 zachowuje się jak przełącznik zależny od cynku, kontrolujący specyficzny znak histonowy.
Przekuwanie utraty cynku w zmiany genetyczne, które przywracają poziom cynku
Co właściwie powoduje utrata tego znaku histonowego? Dzięki mapowaniu na poziomie całego genomu zespół wykazał, że H3K14ac jest szczególnie wzbogacony w regionach enhancerowych — regulacyjnych odcinkach DNA, które precyzyjnie modulują pobliskie geny. W warunkach niedoboru cynku H3K14ac była usuwana z wielu enhancerów, a im większa była utrata, tym silniejsza była zmiana aktywności sąsiadujących genów. Jednym z wyróżniających się genów był ZIP10, który koduje białko na powierzchni komórki importujące cynk. Gdy H3K14ac malała przy enhancerze ZIP10, poziom ZIP10 w błonie wzrastał, co umożliwiało większy napływ cynku do komórki. Zablokowanie KAT7 lub uniemożliwienie utraty H3K14ac zakłócało tę odpowiedź i zmniejszało pobór cynku, nawet po ponownym dodaniu cynku. To pokazuje, że komórki przekształcają niedobór cynku w sygnał epigenetyczny, który wzmacnia mechanizmy importu cynku, aby przywrócić równowagę.
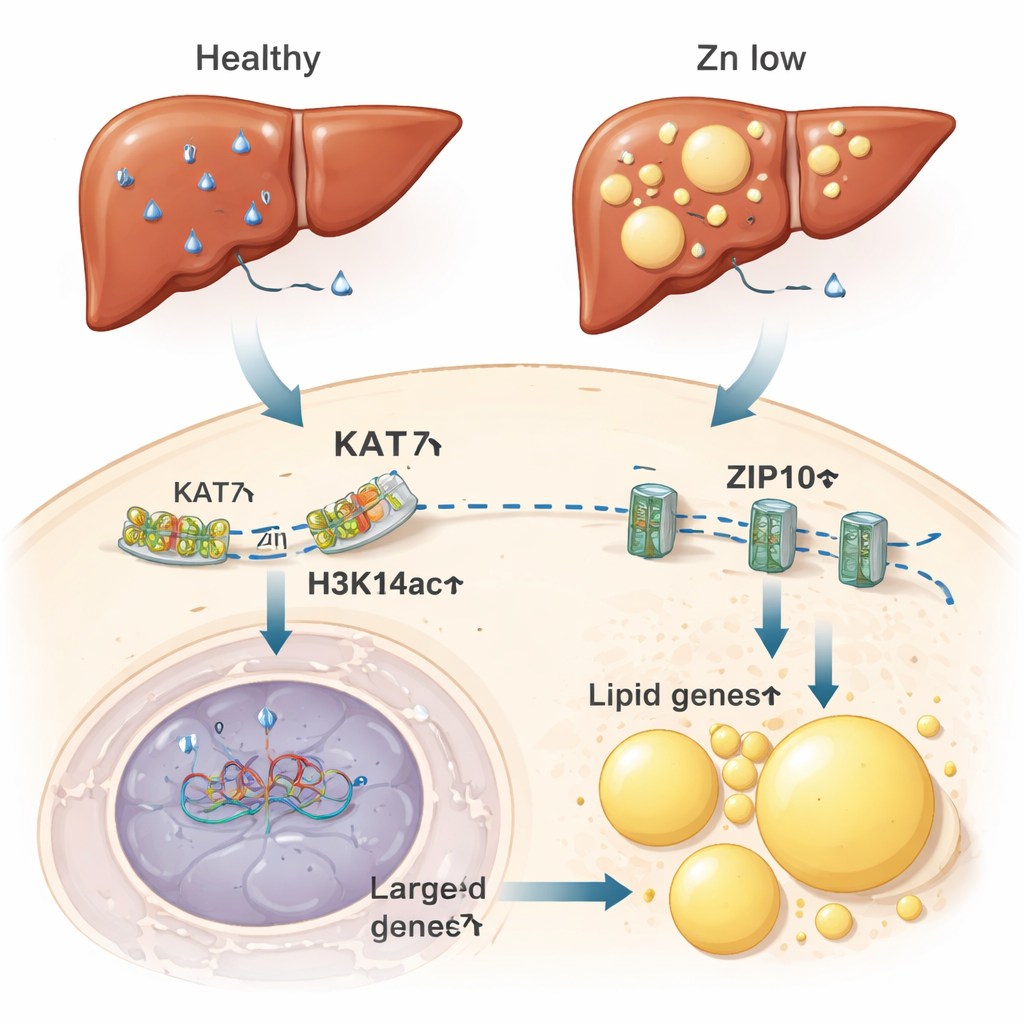
Od komórek spragnionych cynku do stłuszczonych wątrób
Autorzy zastanawiali się następnie, czy ten wrażliwy na cynk przełącznik ma konsekwencje w całych organizmach. U myszy karmionych dietą ubogą w cynk wątroba — centralne centrum metabolizmu cynku i tłuszczu — wykazywała obniżone poziomy cynku, niższe H3K14ac i osłabioną aktywność KAT7. Zmiany te zbiegały się z wyższą ekspresją genów promujących magazynowanie tłuszczu i powstawanie kropli lipidowych, mikroskopijnych pakietów tłuszczu wewnątrz komórek. Wątroby myszy z niedoborem cynku gromadziły tłuszcz w stopniu porównywalnym z myszami na diecie wysokotłuszczowej. Co istotne, samo obniżenie aktywności KAT7 za pomocą leku, nawet bez zmiany zawartości cynku w diecie, wystarczało do promowania gromadzenia tłuszczu w komórkach wątroby. Odwrotnie, dostarczenie dodatkowego cynku zmniejszało nagromadzenie tłuszczu wywołane dietą wysokotłuszczową.
Co to oznacza dla ryzyka chorób u ludzi
Umieszczając swoje ustalenia w kontekście klinicznym, badacze przejrzeli prace ludzkie mierzące poziomy cynku w tkance wątroby. W wielu raportach osoby ze stłuszczeniem wątroby i powiązanymi zaburzeniami miały znacznie mniej cynku w wątrobie niż zdrowe osoby kontrolne. W połączeniu z eksperymentami na myszach sugeruje to, że przewlekły niedobór cynku może sprzyjać chorobie stłuszczeniowej wątroby przez wyciszanie KAT7, usuwanie znaku H3K14ac i trwałe zwiększanie aktywności genów promujących magazynowanie tłuszczu. Mówiąc prostymi słowami, praca odsłania wewnętrzny obwód „cynk→epigenetyka”: gdy cynk spada, enzym zależny od cynku traci moc, zmieniając opakowanie DNA w sposób, który najpierw pomaga komórkom pobierać więcej cynku, ale z czasem może także popychać wątrobę w kierunku niezdrowego gromadzenia tłuszczu.
Cytowanie: Fujisawa, T., Takenaka, S., Maekawa, L. et al. Pathophysiological significance of impaired KAT7-dependent histone H3K14 acetylation during zinc deficiency. Nat Commun 17, 1710 (2026). https://doi.org/10.1038/s41467-026-69476-z
Słowa kluczowe: niedobór cynku, epigenetyka, tłuszcz w wątrobie, acetylacja histonów, transportery cynku