Clear Sky Science · pl
Mechanistyczne spojrzenie na termodynamikę nie-równowagową wiązania azotu za pomocą kawitacji akustycznej
Przekształcanie powietrza w użyteczny nawóz za pomocą dźwięku
Azot z powietrza jest niezbędny dla produkcji nawozów i żywności, ale przekształcenie tego opornego gazu w użyteczne formy zwykle wymaga ogromnych zakładów, bardzo wysokiej temperatury i dużego ciśnienia. To badanie bada zupełnie inne podejście: wykorzystanie intensywnych fal dźwiękowych do tworzenia maleńkich wybuchających pęcherzyków w wodzie, które mogą „wiązać” azot w warunkach dalekich od równowagi. Obserwując i modelując to, co dzieje się wewnątrz tych krótkotrwałych gorących punktów, badacze pokazują, jak pęcherzyki napędzane dźwiękiem mogą otworzyć nową drogę do produkcji związków azotowych bez tradycyjnych katalizatorów czy olbrzymich reaktorów.
Dlaczego wiązanie azotu jest tak trudne
Nasza atmosfera w większości składa się z gazu azotowego, ale jego atomy są związane jednym z najsilniejszych wiązań chemicznych w przyrodzie. Rozbicie tego wiązania w sposób wydajny jest powodem, dla którego proces Habera–Boscha wymaga potężnego sprzętu i zużywa ogromne ilości energii na całym świecie. Tradycyjne metody muszą znaleźć niezręczną równowagę: temperatury wystarczająco wysokie, by aktywować azot, ale nie tak wysokie, by pożądane produkty się rozkładały lub by równowaga przesuwała reakcję wstecz. W artykule argumentuje się, że zamiast utrzymywać stałą temperaturę, skuteczniejsze może być krótkotrwałe przekroczenie — wykorzystanie ultrakrótkich impulsów ciepła — a następnie bardzo szybkie schłodzenie, tak by użyteczne produkty zostały „zatrzymane” zanim ulegną rozpadowi.
Wykorzystanie ultradźwięków do tworzenia maleńkich komór reakcyjnych
Gdy silne ultradźwięki przechodzą przez wodę, tworzą mikroskopijne pęcherzyki gazu, które rosną, a następnie gwałtownie zapadają się — zjawisko znane jako kawitacja akustyczna. Każdy zapadający się pęcherzyk zachowuje się jak miniaturowy, krótkotrwały reaktor. W ciągu miliardowych części sekundy gaz wewnątrz jest sprężany do temperatur powyżej 5000 kelwinów, po czym ponownie bardzo szybko schładza się z prędkościami bliskimi 10^12 kelwinów na sekundę. W takich warunkach cząsteczki azotu w pęcherzyku mogą rozpaść się na reaktywne fragmenty, które następnie łączą się z fragmentami pochodzącymi z tlenu, wodoru lub wody, tworząc azotyny, azotany lub jony amonowe. Nowe produkty są następnie wyrzucane do otaczającej cieczy, gdzie kumulują się w czasie, podczas gdy powstaje i zapada się kolejne pokolenie pęcherzyków. 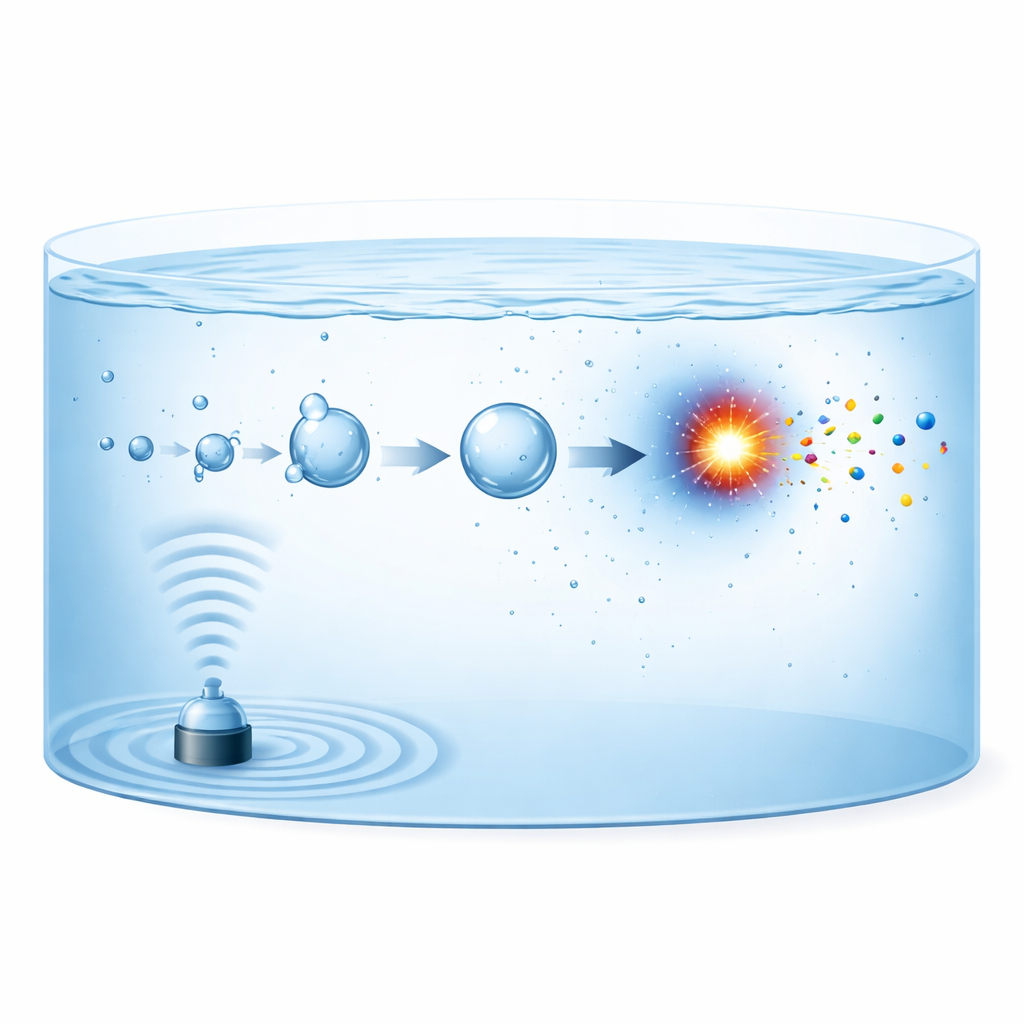
Dostrajanie pęcherzyków, by wybierać różne produkty
Zespół systematycznie zmieniał gazy zasilające pęcherzyki (azot z dodatkiem tlenu lub wodoru), siłę i częstotliwość ultradźwięków oraz obecność cząstek stałych ułatwiających tworzenie pęcherzyków. W mieszankach azotu i tlenu system głównie wytwarzał produkty utlenione, takie jak azotyny i azotany; w mieszankach azotu i wodoru dominował jon amonowy. Niewielkie ilości talku działały jak „nasiona” pęcherzyków, obniżając próg kawitacji i zwiększając powtarzalność reakcji. Poprzez regulację ciśnienia akustycznego i czasu reakcji badacze mogli przesuwać równowagę między azotynem a azotanem, pokazując, że część chemii zachodzi wewnątrz zapadającego się pęcherzyka, a część kontynuuje w otaczającej wodzie, gdy reaktywne fragmenty stopniowo przekształcają azotyn w bardziej utleniony azotan.
Zajrzeć do nano-skali impulsu cieplnego
Aby zrozumieć, dlaczego tak ekstremalne, krótkotrwałe warunki wciąż dają stabilne produkty, autorzy połączyli pomiary z szczegółowymi symulacjami i obliczeniami kwantowochemicznymi. Wynika z nich, że przy bardzo wysokich temperaturach azot może rozpadać się bezpośrednio w fazie gazowej, otwierając ścieżki reakcyjne normalnie niedostępne. Te same obliczenia jednak pokazują także, że utrzymywanie gazu w wysokiej temperaturze uczyniłoby produkty końcowe niestabilnymi. Kluczowe jest szybkie stłumienie: skok temperatury w pęcherzyku aktywuje azot, a niemal natychmiastowe schłodzenie stabilizuje pośrednie fragmenty i gotowe cząsteczki, takie jak amoniak i kwas azotawy, zanim ulegną rozpadowi lub zpowrotem przekształcą się w azot. Modelowanie pojedynczych pęcherzyków, zwłaszcza gdy domieszkowane są argonem podnoszącym temperaturę zapadania, potwierdziło, że wyższe temperatury szczytowe przesuwają skład produktów i zwiększają ogólne tempo wiązania azotu. 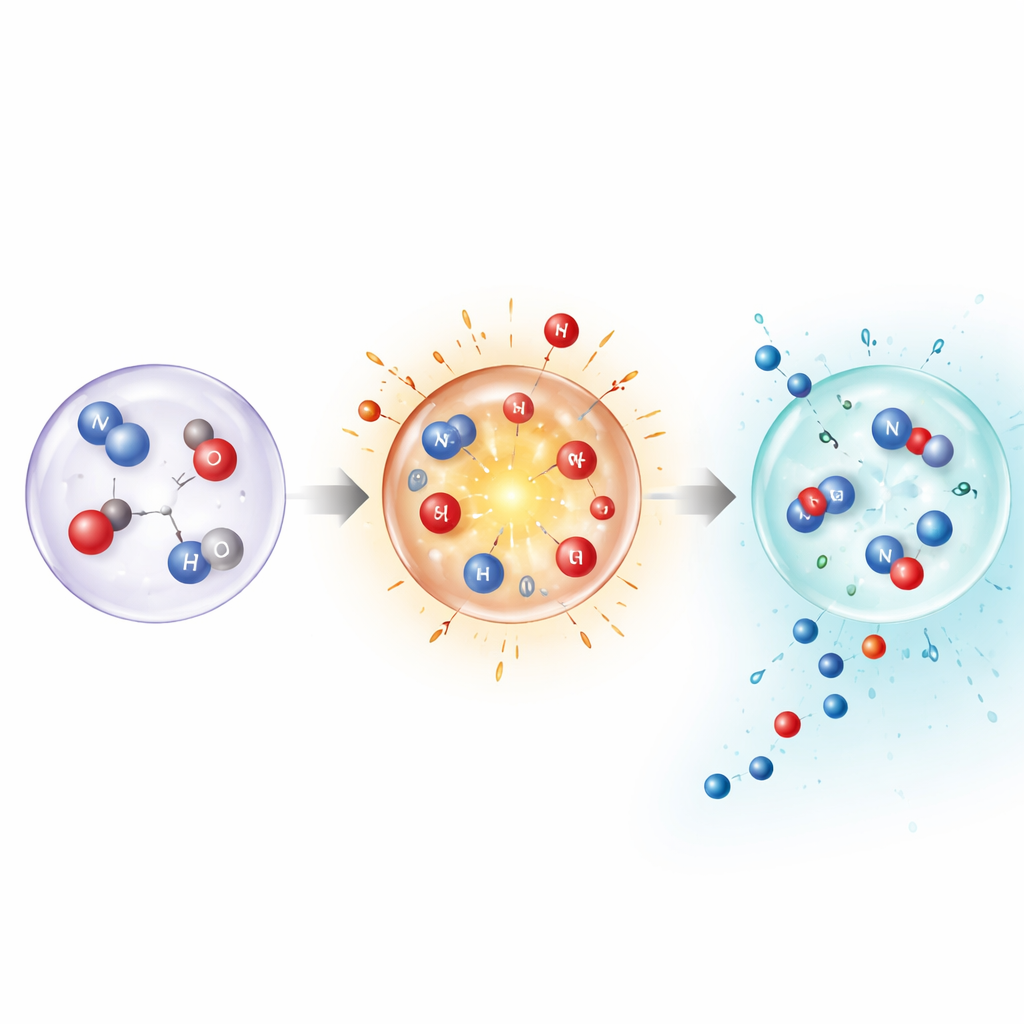
Zużycie energii i możliwości na przyszłość
Chociaż ta metoda napędzana dźwiękiem nie jest jeszcze tak energooszczędna jak najlepsze procesy przemysłowe, jej osiągi już dorównują historycznym podejściom z łukiem elektrycznym i niektórym współczesnym systemom plazmowym, a wszystko to przy pracy w warunkach otoczenia i bez użycia stałych katalizatorów. Co istotne, te same zdarzenia kawitacyjne rozszczepiają także wodę, uwalniając wodór, tlen i nadtlenek wodoru — produkty o wysokiej zawartości energii, które można by pozyskiwać równolegle związanemu azotowi. Autorzy podkreślają, że ich układ został zaprojektowany, by ujawnić mechanizmy, a nie maksymalizować wydajność, ale praca ta ustanawia kawitację akustyczną jako odrębną drogę wiązania azotu poprzez wykorzystanie ekstremalnie szybkiego cyklu termicznego w mikroskopijnych pęcherzykach. Dla osób niebędących specjalistami wnioskiem jest to, że starannie kontrolowany dźwięk może przemienić zwykłą wodę i powietrze w składniki nawozów poprzez sekwencję maleńkich, niewidocznych eksplozji, co wskazuje na bardziej zielone i elastyczne drogi produkcji kluczowych związków azotowych w przyszłości.
Cytowanie: Pan, X., Preso, D.B., Liu, Q. et al. Mechanistic insights into the non-equilibrium thermodynamics of nitrogen fixation via acoustic cavitation. Nat Commun 17, 2682 (2026). https://doi.org/10.1038/s41467-026-69466-1
Słowa kluczowe: wiązanie azotu, kawitacja akustyczna, sonochemia, produkcja nawozów, chemia ultradźwiękowa