Clear Sky Science · pl
Podpopulacja komórek mezenchymalnych indukowana przez makrofagi, wyrażająca Fcer1g, przyczynia się do włóknienia po urazie
Dlaczego niektóre rany zostawiają trwałe blizny
Większość z nas nosi blizny po skaleczeniach, operacjach czy wypadkach, lecz dlaczego niektóre rany goją się gładko, a inne pozostawiają grube, uniesione ślady, pozostawało zagadką. To badanie przygląda się temu problemowi od strony komórkowej, skupiając się na komórkach odbudowujących uszkodzoną skórę. Naukowcy odkrywają wcześniej nieopisany podtyp komórek tworzących blizny, które włączają się wcześnie po urazie pod wpływem komórek odpornościowych zwanych makrofagami. Zrozumienie tej ukrytej współpracy może wskazać drogę do terapii pozwalających skórze goić się z mniejszym bliznowaceniem przy jednoczesnym efektywnym zamykaniu ran. 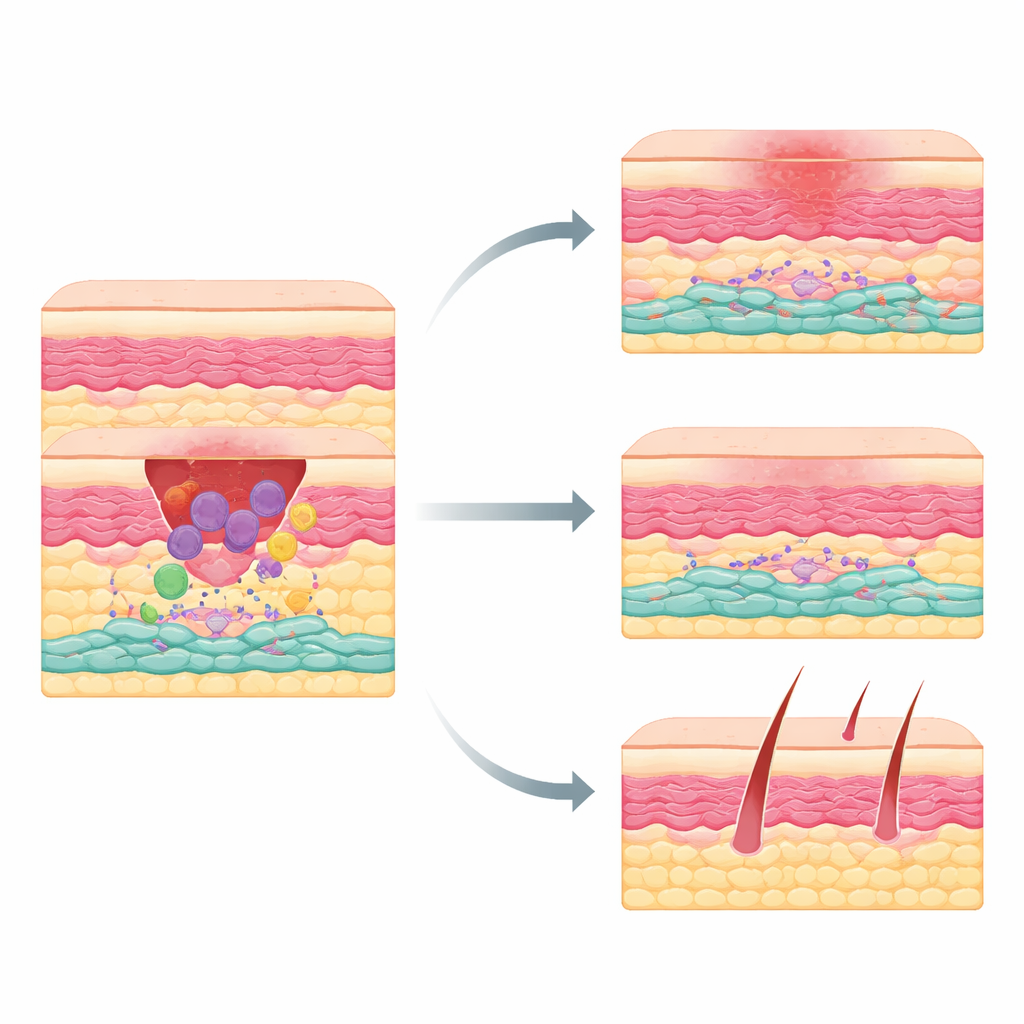
Ukryci gracze w gojącej się skórze
Gdy skóra zostaje przecięta, organizm przechodzi przez uporządkowaną sekwencję: najpierw stan zapalny oczyszczający uszkodzenie, potem wzrost tkanki, a na końcu przebudowę. Makrofagi pojawiają się wcześnie, by usuwać szczątki i wysyłać sygnały chemiczne mobilizujące inne komórki. Wśród responderów są komórki mezenchymalne — budowniczowie podobni do fibroblastów, odkładający kolagen i inne elementy podporowe. Ci budowniczowie nie są jednolici: jedne sprzyjają regeneracji, inne mają skłonność do nadprodukcji tkanki bliznowatej. Do tej pory naukowcy nie wyodrębnili wyraźnie, które dorosłe skórowe komórki mezenchymalne odpowiadają za powstawanie grubych blizn.
Komórki odpornościowe, które cicho przygotowują grunt pod bliznowacenie
Aby zbadać, jak makrofagi wpływają na bliznowacenie, zespół użył myszy, u których makrofagi można selektywnie usunąć w pierwszych dniach po zranieniu. Gdy wczesne makrofagi zostały usunięte, rany nadal się zamykały, ale powstawały znacznie mniejsze blizny o rzadszym ułożeniu kolagenu. Sekwencjonowanie RNA pojedynczych komórek — metoda profilowania aktywności genów w poszczególnych komórkach — wykazało, że większość podgrup mezenchymalnych nie zmieniała się po utracie makrofagów. Jednym wyjątkiem był wyraźny podzbiór komórek mezenchymalnych pozytywnych dla PDGFRα, który włączał gen o nazwie Fcer1g. Ta podpopulacja niemal zniknęła po usunięciu makrofagów, co sugeruje, że makrofagi są potrzebne do powstawania lub utrzymania tych komórek.
Szybko rosnąca populacja komórek napędzająca bliznowacenie
Dalsze eksperymenty odwzorowały, gdzie i kiedy pojawiają się te komórki mezenchymalne pozytywne dla Fcer1g. W nieuszkodzonej skórze były rzadkie, ale po urazie szybko się rozrastały — najpierw wokół brzegów rany, a potem skupiały się w dnie rany, gdzie do siódmego dnia stanowiły większość komórek PDGFRα-dodatnich. Te komórki dzieliły się szybciej niż inne komórki mezenchymalne i wykazywały niską migrację, co wskazuje, że ich przyrost napędza lokalna proliferacja. Gdy badacze użyli sprytnego systemu genetycznego do selektywnego eliminowania komórek wyrażających jednocześnie PDGFRα i Fcer1g, zamknięcie rany przebiegało normalnie — jednak blizny zmniejszyły się o ponad 20 procent, zawartość kolagenu spadła o około 30 procent, a sieć kolagenowa w naprawionej skórze przypominała bardziej skórę nieuszkodzoną. W tych wyczerpanych komórkach rany było też więcej mieszków włosowych, co sugeruje bardziej regeneracyjne gojenie. 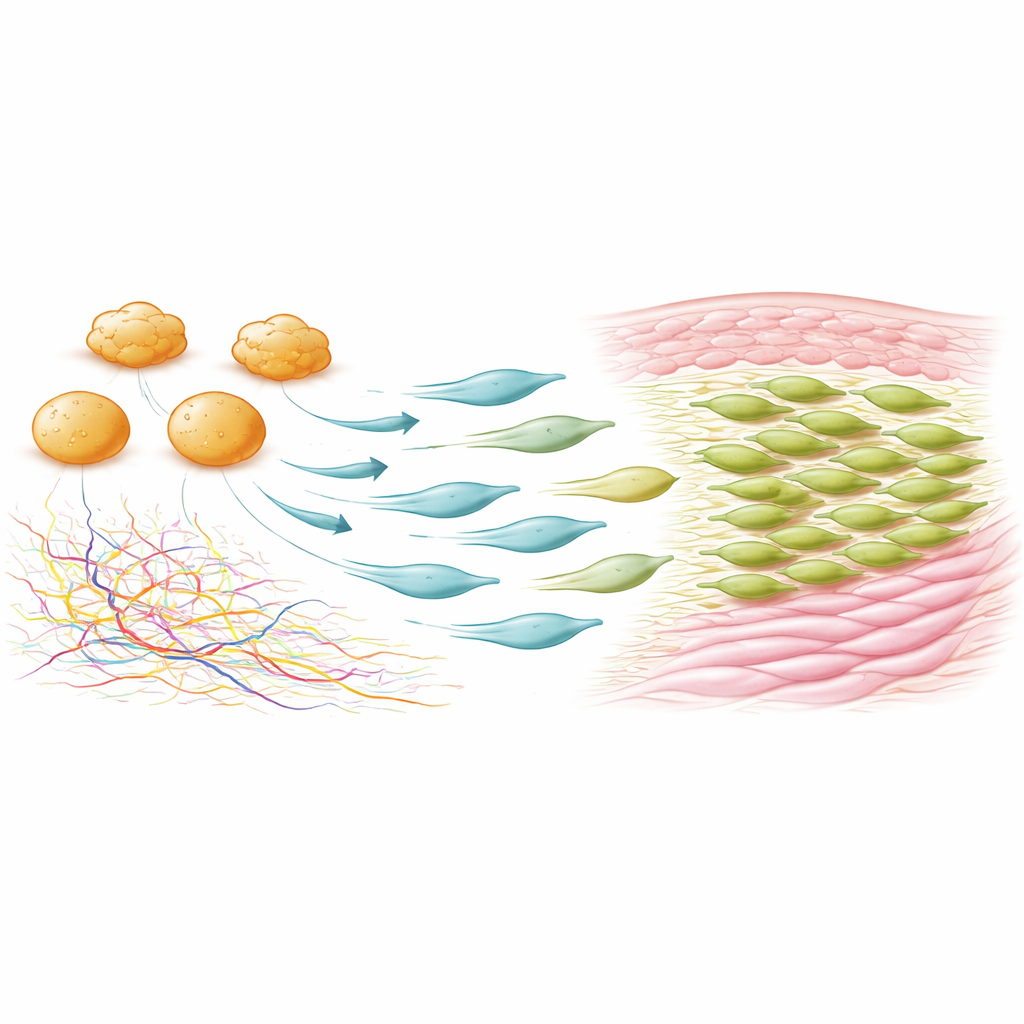
Jak makrofagi sygnalizują budowniczym nadmierne bliznowacenie
Aby zrozumieć, jak makrofagi wywołują ten podatny na blizny stan, zespół przeanalizował prawdopodobne drogi komunikacji między typami komórek. Głównym kandydatem była fibrylina (fibronektyna), lepka białkowa część tymczasowej macierzy w świeżych ranach. Makrofagi we wczesnych ranach były głównym źródłem fibronektyny, a jej poziomy spadły gwałtownie po usunięciu makrofagów. U myszy zaprojektowanych tak, by brakowało wersji fibronektyny związanej z raną (forma EDA), komórki mezenchymalne pozytywne dla Fcer1g były znacznie zredukowane, a blizny łagodniejsze. W hodowli bezpośredni kontakt z makrofagami wystarczył, by zwykłe fibroblasty skórne przekształciły się w komórki pozytywne dla Fcer1g i PDGFRα, co potwierdza, że makrofagi mogą bezpośrednio indukować ten stan.
Wspólny program bliznowacenia u myszy i ludzi
Aby sprawdzić, czy ten typ komórki ma znaczenie u ludzi, badacze ponownie przeanalizowali dostępne dane o uszkodzeniach skóry u ludzi na poziomie pojedynczych komórek i całych tkanek. Znaleźli odpowiadającą podgrupę mezenchymalną w ludzkich ranach, która wyrażała FCER1G i miała podobny podpis genowy, osiągając szczyt około tydzień po urazie — ten sam czas obserwowany u myszy. W ponad stu ludzkich próbkach obejmujących skórę prawidłową, ostre rany, rany przewlekłe i uniesione blizny, program genów związanych z FCER1G wyraźnie oddzielał tkankę zranioną i zbliznowaconą od skóry nieuszkodzonej i był najsilniejszy we wczesnym okresie po urazie. Ta podobieństwo międzygatunkowe sugeruje, że nowo zdefiniowany stan komórkowy jest ewolucyjnie zachowanym motorem naprawy włóknistej.
Kierunek: łagodniejsze gojenie z mniejszą liczbą blizn
Podsumowując, wyniki ujawniają wcześniej niedoceniony ciąg zdarzeń: makrofagi pojawiające się wcześnie wzbogacają ranę w fibronektynę, fibronektyna pomaga przekształcić lokalne komórki mezenchymalne w szybko dzielący się stan FCER1G-dodatni, a ta wyspecjalizowana podgrupa odkłada nadmiar kolagenu, który staje się tkanką bliznowatą. Ponieważ usunięcie tych komórek u myszy zmniejszyło bliznowacenie bez spowalniania zamknięcia rany, stanowią one atrakcyjny cel dla przyszłych terapii. Leki lub biologiczne środki przerywające sygnały tworzące lub podtrzymujące ten stan komórkowy — na przykład przez modulację zachowania makrofagów lub środowiska fibronektynowego — mogłyby w przyszłości pomóc pacjentom goić urazy skóry z minimalnymi, mniej widocznymi bliznami.
Cytowanie: Ma, X., Wang, E., Puviindran, V. et al. A macrophage-induced subpopulation of mesenchymal cells expressing Fcer1g contributes to wound-induced fibrosis. Nat Commun 17, 2686 (2026). https://doi.org/10.1038/s41467-026-69449-2
Słowa kluczowe: gojenie ran, włóknienie skóry, makrofagi, fibroblasty, powstawanie blizn