Clear Sky Science · pl
Pozytywna kooperatywność między domenami wiążącymi RAS i bogatymi w cysteinę reguluje kinetykę wiązania RAF z błoną poprzez boczne ponowne wiązanie
Dlaczego ten drobny molekularny taniec ma znaczenie
We wnętrzu naszych komórek decyzje o wzroście, podziale i przetrwaniu często zapadają na powierzchni błony komórkowej. Kluczowym graczem w tych decyzjach jest białko zwane RAF, które przekazuje sygnały wzrostu i bywa często nieprawidłowo aktywowane w nowotworach. W badaniu tym odkryto w niespotykanym dotąd kinetycznym detalu, jak RAF przyczepia się do błon komórkowych, jak długo tam przebywa oraz dlaczego zatłoczone okręgi innego białka, RAS, mogą utrzymywać RAF w stanie aktywnym dłużej niż oczekiwano.
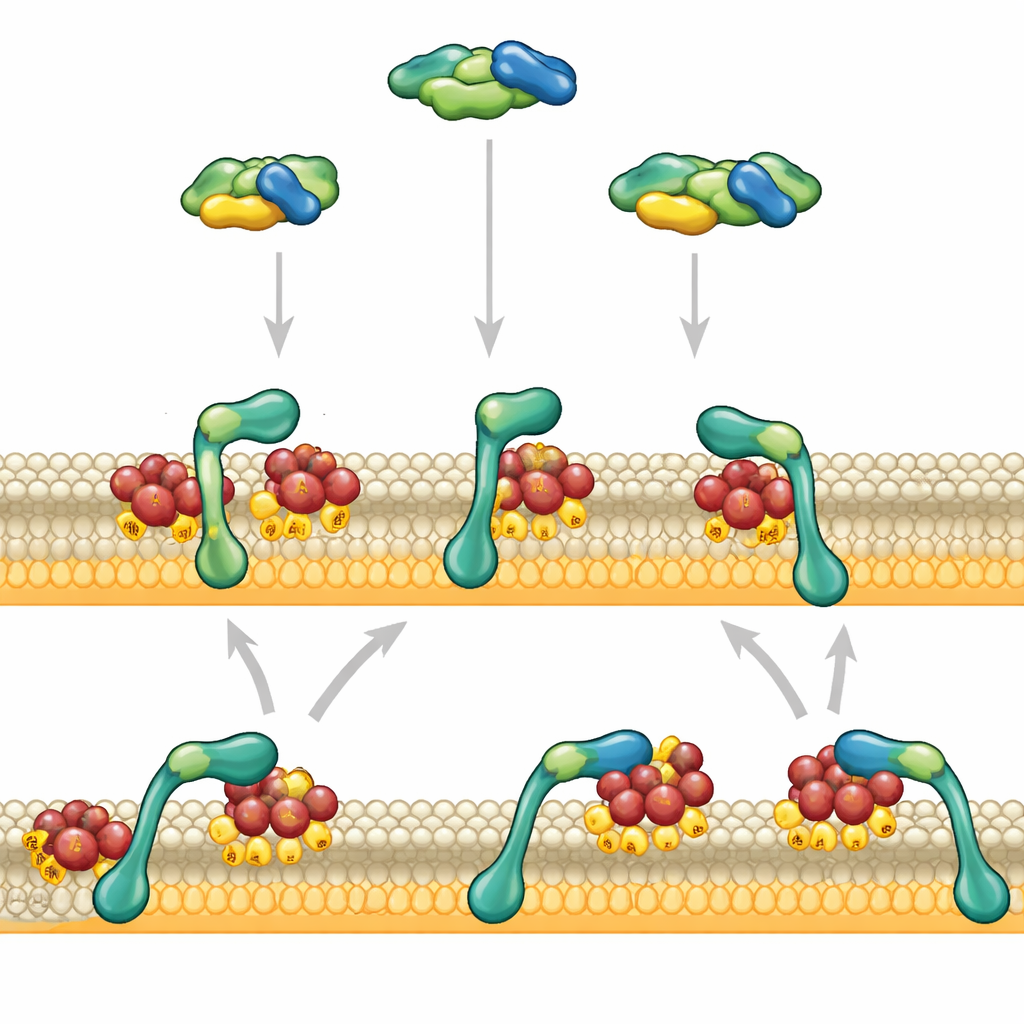
Sygnały spotykające się na powierzchni komórki
RAF działa w głównej szlaku sygnalizacyjnym znanym jako droga MAPK, która łączy zewnętrzne bodźce, takie jak czynniki wzrostu, ze zmianami aktywności genów. W stanie spoczynku RAF unosi się w cytoplazmie w złożonej, autoizolującej konfiguracji. Włącza się dopiero po spotkaniu z RAS, małym molekularnym wyłącznikiem zakotwiczonym w wewnętrznej warstwie błony komórkowej. RAS musi znajdować się w stanie „włączonym” i być osadzony w odpowiednim typie lipidów, aby RAF mógł zostać zrekrutowany i aktywowany. Ponieważ cząsteczek RAF jest stosunkowo niewiele w porównaniu z wieloma innymi składnikami sygnalizacji, sposób, w jaki angażują one błonę i unikają przedwczesnego odpadnięcia, silnie wpływa na to, czy komórka zareaguje słabo czy silnie na sygnał wzrostu.
Dwie dłonie do chwytania błony
Autorzy skupili się na dwóch obszarach na czołowym końcu RAF: jednym, który chwyta RAS, i drugim preferującym ujemnie naładowane lipidy błonowe. Używając sztucznych błon i oczyszczonych białek, obserwowali pojedyncze fragmenty RAF wiążące się z powierzchniami udekorowanymi RAS za pomocą zaawansowanej mikroskopii. Gdy region wiążący RAS działał samodzielnie, dotykał błony krótko i odłączał się w ciągu około sekundy. Region preferujący lipidy sam w sobie prawie w ogóle się nie przyczepiał. Jednak gdy oba regiony były połączone, zachowywały się zupełnie inaczej: RAF przyłączał się silnie i utrzymywał na błonie przez dziesiątki sekund, szczególnie gdy błona zawierała dużo ujemnie naładowanych lipidów podobnych do tych w rzeczywistych komórkach.
Współpraca, która spowalnia wyjście
Ta dramatyczna zmiana nie wynikała z szybszego znajdowania przez RAF błony, lecz z wolniejszego odchodzenia. Najpierw segment RAF wiążący RAS rozpoznaje aktywowany RAS i dokuje RAF przy błonie. Dopiero po tym pierwszym uścisku region wiążący lipidy w pełni angażuje otaczające lipidy, spowalniając boczny ruch RAF i mocniej go kotwicząc. Ten drugi kontakt stabilizuje z kolei pierwotną interakcję RAS–RAF, tworząc dodatnie sprzężenie zwrotne między kontaktami białko–białko a białko–lipid. Eksperymenty zmieniające krótki łącznik łączący te dwa regiony wykazały, że ich ciasna koordynacja przestrzenna jest kluczowa: zwiększenie elastyczności lub długości łącznika osłabiało zdolność RAF do pozostawania na błonie.
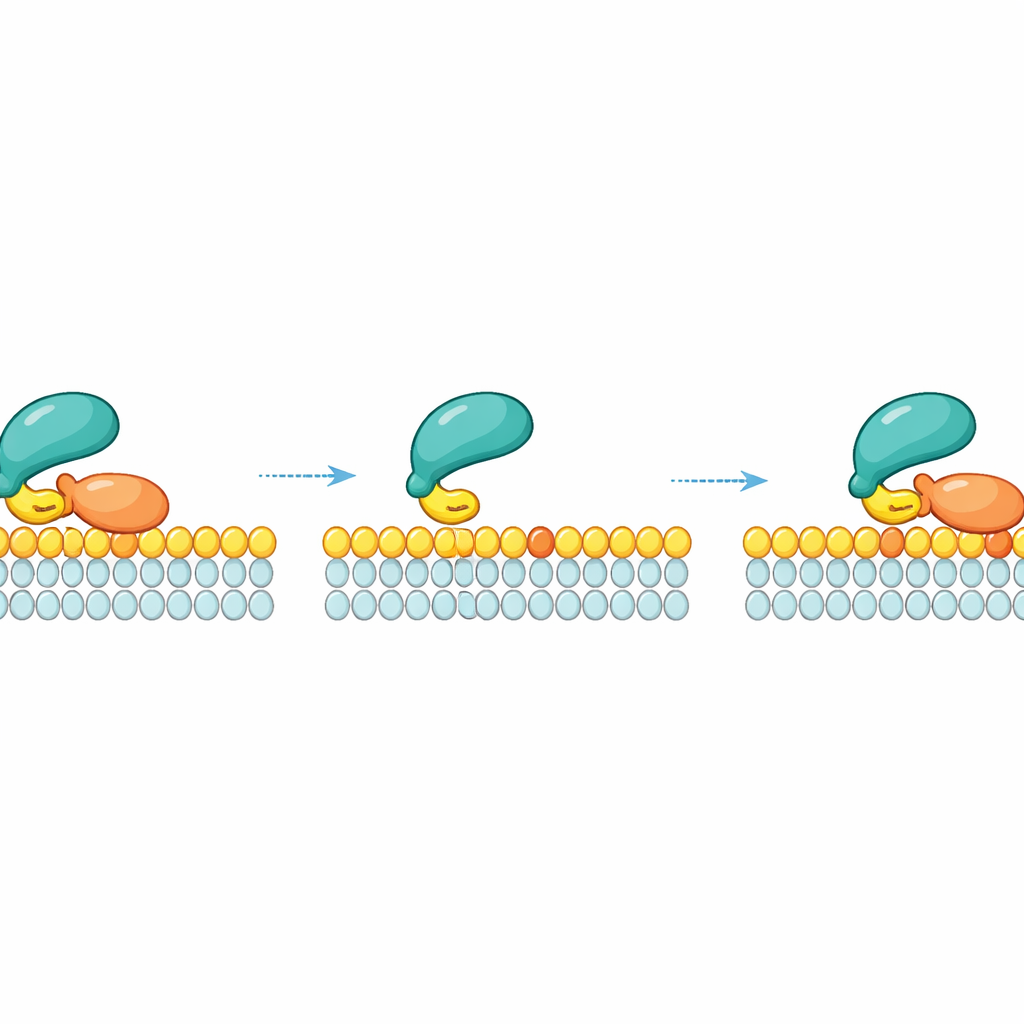
Boczne ponowne wiązanie: ślizganie zamiast odpadać
Kluczowym wnioskiem pracy jest to, że RAF nie odrywa się po prostu do otaczającego płynu, gdy odłącza się od konkretnej cząsteczki RAS. Zamiast tego, po uwolnieniu RAS, RAF może pozostać krótko przywiązany do błony przez słaby kontakt z lipidami i ślizgać się bokiem. W tym przejściowym stanie może „ponownie złapać” sąsiednią cząsteczkę RAS na tej samej płaszczyźnie błony. To boczne ponowne wiązanie tworzy kinetyczną siatkę bezpieczeństwa: przy wysokiej lokalnej gęstości RAS — na przykład w nanoklastrach, gdzie cząsteczki RAS są ściśle upakowane — RAF ma wiele szans na ponowne zaangażowanie RAS zanim odpłynie. Pomiary i symulacje pokazały, że im wyższa gęstość aktywnego RAS na błonie, tym dłużej RAF pozostaje związany z błoną dzięki tym powtarzającym się lokalnym ponownym przyłączeniom.
Od przedłużonych wizyt do niezawodnej aktywacji
Wydłużony czas przebywania RAF na błonie ma istotne konsekwencje. Aktywacja RAF nie jest pojedynczym zdarzeniem, lecz wieloetapową sekwencją obejmującą zmiany konformacyjne, usuwanie hamujących modyfikacji i parowanie dwóch cząsteczek RAF w aktywny dimer. Badanie sugeruje, że tylko cząsteczki RAF, które wystarczająco długo osiadają na błonie, mogą ukończyć ten ciąg zdarzeń — forma „kinetycznego sprawdzania poprawności”, która pomaga komórkom uniknąć przypadkowej aktywacji wywołanej przelotnymi, słabymi sygnałami. Ukazując, jak współdziałanie wiązania RAS, zaangażowania lipidów i bocznego ponownego wiązania determinuje czas pobytu RAF na błonie, praca ta opisuje ogólną strategię, dzięki której komórki mogą używać wielu małych, słabych interakcji na błonach do precyzyjnego regulowania silnych dróg sygnalizacyjnych.
Cytowanie: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Słowa kluczowe: RAS, kinaza RAF, sygnalizacja w błonie komórkowej, boczne ponowne wiązanie, kinetyczne sprawdzanie poprawności