Clear Sky Science · pl
Strukturalne i molekularne podstawy regulacji allosterycznej i sprzężenia katalitycznego ludzkiej fosforibosylformyloglicynamidyny syntazy
Dlaczego ten enzym ma znaczenie dla zdrowia
Każda komórka w twoim ciele potrzebuje puryn — małych cząsteczek, które zasilają reakcje, magazynują energię i przenoszą informacje genetyczne. Komórki nowotworowe, które dzielą się szybko, szczególnie intensywnie zużywają puryny i często przeorganizowują ich produkcję. W tym badaniu skupiono się na ludzkim enzymie zwanym FGAMS, kluczowym ogniwie w budowie puryn „od podstaw”. Ukazując trójwymiarową strukturę FGAMS oraz sposób, w jaki jego części się poruszają i komunikują, autorzy odkrywają mechanizmy włączania i wyłączania enzymu oraz wskazują, jak można by go zaatakować, by spowolnić wzrost guza.
Pod kontrolą: elementy budulcowe życia
Komórki wytwarzają puryny w wymagającej linii montażowej zwanej szlakiem de novo, która zużywa energię i wykorzystuje kilka enzymów do składania złożonego pierścienia. FGAMS katalizuje czwarty etap tej sekwencji i znajduje się w centrum większego zespołu enzymatycznego zwanego purinosomem, który ułatwia efektywne przekazywanie substratów. Ponieważ szybko rosnące komórki nowotworowe często wzmacniają ten szlak, enzymy takie jak FGAMS są atrakcyjnymi celami terapeutycznymi: ich blokada może pozbawić guzy nukleotydów niezbędnych do podziału, podczas gdy zdrowe komórki mogą polegać na szlakach recyklingu.
Maszyna molekularna zmieniająca kształt
FGAMS zbudowany jest z trzech powiązanych ze sobą części, czyli domen, z których każda pełni inną funkcję i musi współpracować w precyzyjnej kolejności. Jedna domena odcina amoniak od aminokwasu glutaminy, druga wykorzystuje ten amoniak do modyfikacji małej cząsteczki cukrowej, a trzecia działa jako centrum regulacyjne. Dzięki wysokorozdzielczej krio‑elektronowej mikroskopii (cryo‑EM) badacze uchwycili FGAMS w trzech odmiennych stanach pracy: związanym z nośnikiem energii, ze złapanym krótkotrwałym intermediatem reakcji oraz z wieloma substratami i intermediatami obecnymi jednocześnie. Porównanie tych stanów ujawniło, że elastyczne pętle i N‑terminalne „ramię” poruszają się gwałtownie, rekonfigurując enzym wraz z postępem reakcji.
Ukryty tunel i molekularne bramy
Kluczową zagadką było to, jak amoniak uwalniany w jednej domenie bezpiecznie przemieszcza się do odległego miejsca, gdzie jest używany, nie dyfundując i nie powodując szkód. Nowe struktury odsłaniają wcześniej nieznany wewnętrzny tunel łączący oba miejsca oraz serię „bram” tworzonych przez konkretne aminokwasy. Kiedy odpowiednie substraty wiążą się i powstaje intermediat, centralna pętla zatrzaskuje się w uporządkowanej pozycji, pociągając domenę N‑terminalną i przestawiając pobliskie pętle w domenie katalitycznej. Ta choreografia otwiera dwie bramy wejściowe, dzięki czemu glutamina może być przetworzona, i tymczasowo przeformowuje region stabilizujący wysokoenergetyczny intermediat niezbędny do rozerwania wiązań.
Sprzęganie chemii przez ruch
W miarę postępu reakcji enzym nie stoi biernie; traktuje każdy krok chemiczny jako sygnał. Gdy w domenie generującej amoniak powstaje kowalencyjny intermediat tioestrowy, wcześniejsze ruchy zostają częściowo odwrócone. To rozluźnia centralną pętlę i przestawia bramy tak, by zamknąć drogi ucieczki, podczas gdy dwie dodatkowe bramy na obu końcach tunelu otwierają się. Subtelne przesunięcia kilku reszt „wąskiego gardła” poszerzają wewnętrzne przejście, pozwalając cząsteczce amoniaku przejść tunelem bezpośrednio do drugiego centrum aktywnego, gdzie reaguje z uwięzionym intermediatem, tworząc końcowy produkt. Mutacje reszt bramowych powodują wyciek amoniaku lub rozłączenie dwóch etapów reakcji, co potwierdza, że ten system bramkowania i kanałów jest niezbędny dla wydajnej katalizy.
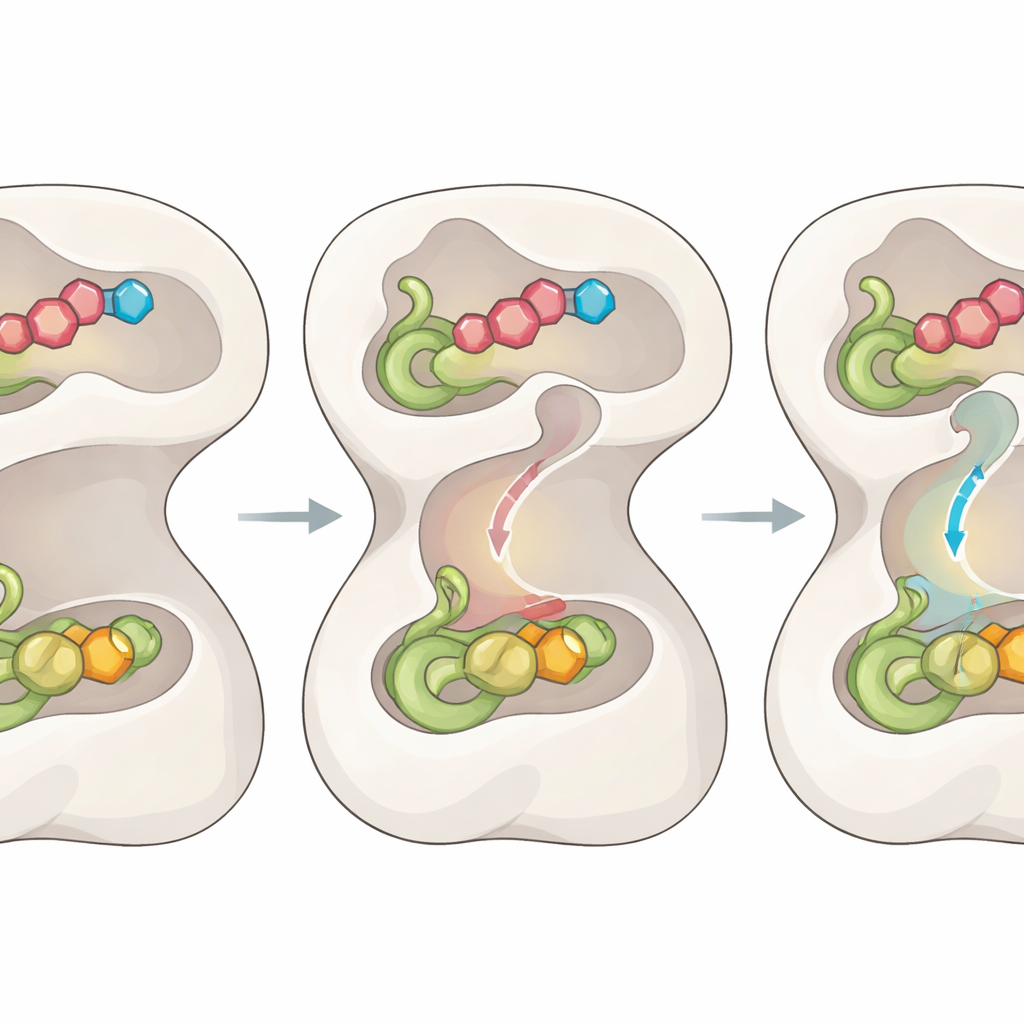
Od wglądu strukturalnego do dróg terapeutycznych
Śledząc FGAMS przez cykl katalityczny, badanie przedstawia szczegółowy obraz tego, jak ruchy domen, elastyczne pętle, wewnętrzne bramy i przejściowy tunel są ze sobą powiązane, aby skoordynować chemię. Dla czytelnika popularnonaukowego sedno sprawy jest takie: enzym działa jak maleńka programowalna fabryka — otwiera drzwi i wewnętrzny przenośnik tylko wtedy, gdy wszystkie właściwe elementy są na miejscu, zapewniając szybkość i bezpieczeństwo. Ponieważ FGAMS wspiera produkcję puryn w komórkach nowotworowych i wiąże się ze złym rokowaniem w nowotworach wątroby, opracowane plany strukturalne i nowo zidentyfikowane punkty kontroli oferują wiele możliwości zaprojektowania leków, które zatykają tunel, zamrażają bramy lub uwiężą kluczowe intermediacyj, co potencjalnie może dać nową klasę ukierunkowanych terapii przeciwnowotworowych.
Cytowanie: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Słowa kluczowe: synteza puryn, regulacja allosteryczna, kanałowanie amoniaku, metabolizm nowotworów, struktura cryo-EM