Clear Sky Science · pl
Molekularny mechanizm działania małocząsteczkowego związku SMT-738 na transporter lipoprotein bakteryjnych LolCDE
Dlaczego ten nowy antybiotyk ma znaczenie
W miarę jak coraz więcej zakażeń szpitalnych staje się opornych na najlepsze antybiotyki, lekarze pilnie potrzebują leków, które zabijają groźne bakterie, nie niszcząc przy tym przyjaznych mikroorganizmów, które nosimy. To badanie wyjaśnia, w jaki sposób obiecujący związek eksperymentalny o nazwie SMT-738 blokuje kluczową maszynerię transportową w zewnętrznej powłoce niektórych trudno leczących się bakterii. Pokazując dokładnie, gdzie i jak ten lek zatyka mechanizm, praca wskazuje drogę do mądrzejszych antybiotyków, które zwalczają superbakterie, oszczędzając jednocześnie dużą część mikrobioty jelitowej.
Zewnętrzna zbroja szkodliwych bakterii
Wiele z najbardziej niebezpiecznych patogenów szpitalnych należy do grupy zwanej bakteriami Gram-ujemnymi. Trudno je zabić, ponieważ otaczają się podwójną, warstwową zewnętrzną powłoką. Ta warstwa jest budowana i utrzymywana przez kilka maszynerii molekularnych, które przenoszą kluczowe cegiełki z błony wewnętrznej, gdzie są syntetyzowane, na powierzchnię. Jednym istotnym typem ładunku są lipoproteiny, które pomagają utrzymać integralność zewnętrznej powłoki oraz wspierają procesy takie jak pobór substancji odżywczych i oporność na antybiotyki. System transportowy zwany ścieżką Lol, a w szczególności pompa o nazwie LolCDE, wyciąga lipoproteiny z błony wewnętrznej i przekazuje je chaperonom, które dostarczają je na zewnętrzną powłokę. Ponieważ te kroki są niezbędne, stanowią atrakcyjne cele dla nowych antybiotyków.
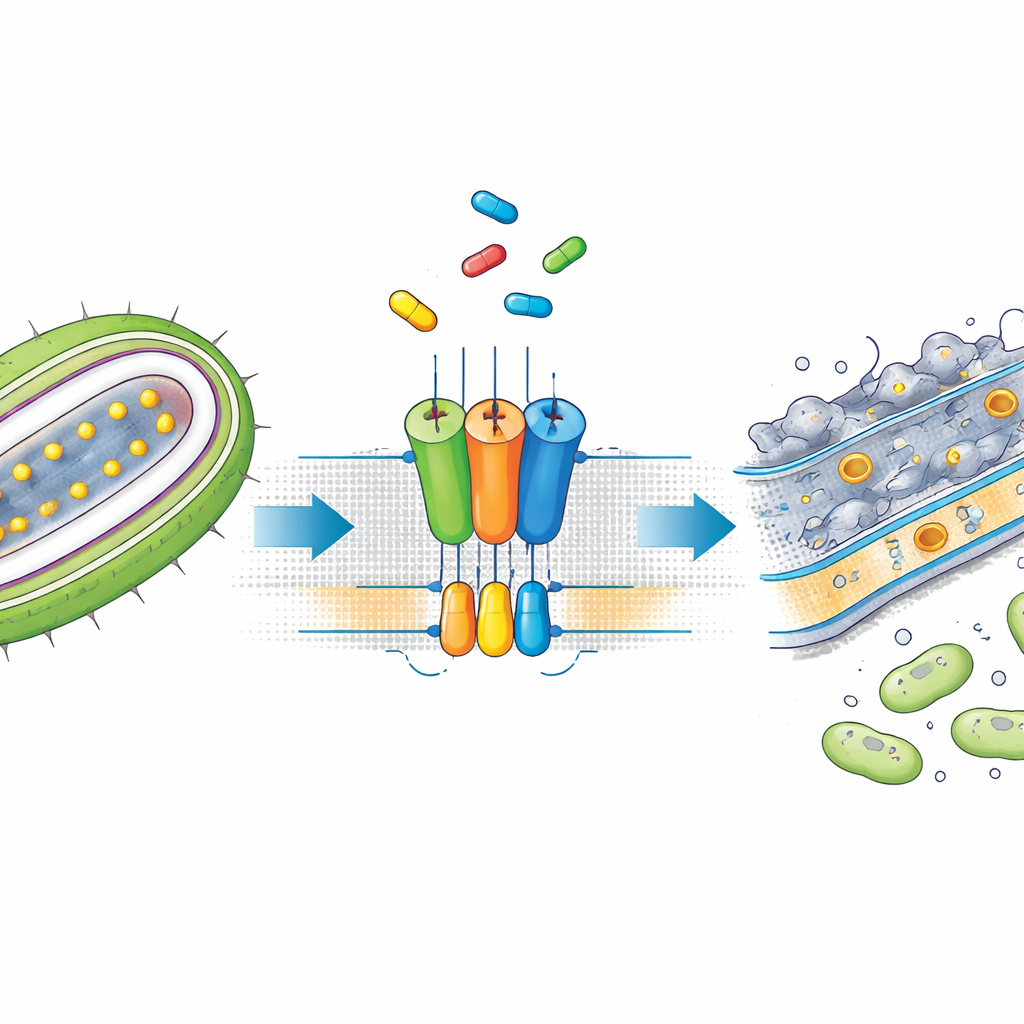
Małocząsteczkowy związek, który zatrzymuje taśmę produkcyjną
SMT-738 wyłonił się z wcześniejszych przesiewów jako silny bloker patogenów Gram-ujemnych należących do rodziny Enterobacteriaceae, w tym szczepów wieloopornych Escherichia coli i Klebsiella pneumoniae. Jednak jego dokładny mechanizm działania był niejasny. Autorzy najpierw pokazali, że SMT-738 uniemożliwia uwolnienie testowej lipoproteiny przez LolCDE w zmodyfikowanych bakteriach, potwierdzając, że lek rzeczywiście zatrzymuje etap transportu. Co ważne, gdy bakterie nosiły określone mutacje w genach kodujących kompleks LolCDE, stawały się odporne na SMT-738, co sugeruje, że związek działa poprzez bezpośrednie wiązanie się z tą pompą. Te obserwacje przygotowały grunt do strukturalnego, dogłębnego zbadania interakcji związku z transporterem.
Zacinanie pompy od środka
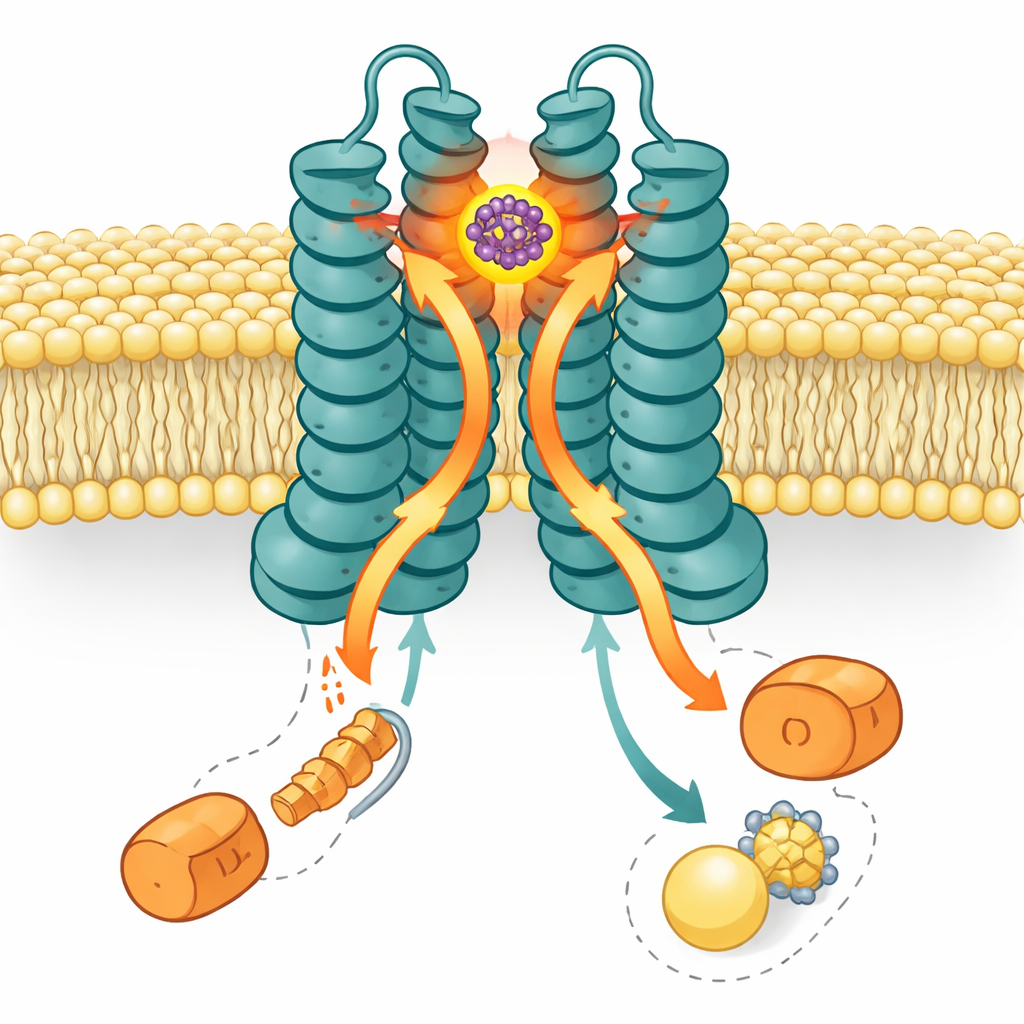
Wykorzystując wysokorozdzielczą krio‑elektronową mikroskopię, badacze uchwycili trójwymiarowy obraz LolCDE z zakotwiczonym SMT-738. Struktura pokazuje, że lek klinuje się w kieszeni na końcu periplazmatycznym — stronie skierowanej w przestrzeń między błoną wewnętrzną a zewnętrzną — pomiędzy dwoma głównymi podjednostkami, LolC i LolE. To miejsce pokrywa się z normalnym miejscem dokowania ładunku lipoprotein. Gdy SMT-738 zajmuje tę kieszeń, otaczające aminokwasy w LolC i LolE przemieszczają się o nawet około jednego nanometra. Te ruchy powodują kolizje steryczne z pozycjami, które normalnie zajmowałaby lipoproteina i jej ogony tłuszczowe, skutecznie blokując wejście ładunku do pompy. Mutacje wielu reszt wyściełających kieszeń osłabiały wiązanie leku lub nadawały bakteriom odporność, co ładnie odpowiada obserwowanej strukturze.
Wywołanie jednostronnego rozpadu
Historia nie kończy się na miejscu wiązania. LolCDE jest napędzany przez dwie kopie podjednostki motorowej zwanej LolD, które siedzą po stronie cytoplazmatycznej i spalają ATP, by napędzać transport. Co uderzające, w strukturze związanej z SMT-738 tylko jedna kopia LolD pozostaje przyłączona; partner LolD odpada. Żele biochemiczne i testy aktywności ATPazy potwierdziły, że związanie SMT-738 powoduje utratę jednej LolD i ostre zmniejszenie aktywności energetycznej pompy. Symulacje komputerowe transportera w błonie wzmocniły ten obraz: gdy SMT-738 osiadał w swojej kieszeni, zmiany konformacyjne rozchodziły się w dół, popychając helisy sprzężeniowe łączące LolC i LolE z LolD. Te przesunięcia wymusiły niekorzystną kolizję na LolD związanej z LolC, powodując jej odłączenie, podczas gdy LolD związana z LolE pozostała na miejscu. Wynikiem jest asymetryczna, „zablokowana” maszyna, która nie może już przemieszczać lipoprotein.
Dlaczego niektóre bakterie są trafione, a inne oszczędzone
SMT-738 ma pożądaną cechę: silnie atakuje oporne Enterobacteriaceae, a przy tym pozostawia wiele innych gatunków Gram‑ujemnych zasiedlających jelito w dużej mierze nietkniętych. Aby zrozumieć tę selektywność, zespół porównał sekwencje LolE z bakterii wrażliwych i opornych oraz skupił się na pozycjach mających kontakt ze SMT-738. Dwie reszty w LolE, zwłaszcza jedna odpowiadająca pozycji D264 w E. coli, wyróżniały się. W wrażliwych patogenach te pozycje odpowiadały wersji kontaktującej lek w E. coli, podczas gdy u wielu opornych komensali jelitowych były zastąpione innymi aminokwasami. Gdy badacze zaprojektowali E. coli z takimi substytucjami, bakterie stały się wysoce odporne na SMT-738, nadal jednak eksprymując LolCDE. Symulacje sugerowały, że te zmiany zmieniają lokalną elastyczność wokół kieszeni, zmniejszając zdolność SMT-738 do wiązania. Co ciekawe, inny inhibitor LolCDE, lolamicyna, opierał się na jedynie częściowo nakładających się punktach kontaktu i wykazywał inny wzorzec oporności, co sugeruje odrębne sposoby atakowania tej samej pompy.
Nowe plany na przyszłe antybiotyki
Łącząc obrazowanie strukturalne, skany mutacyjne, testy biochemiczne i symulacje komputerowe, praca pokazuje, że SMT-738 to nie tylko korek w kanale. Zamiast tego związek przyczepia się do strony periplazmatycznej pompy LolCDE, blokuje miejsce wejścia lipoprotein, a następnie wywołuje dalekosiężne przesunięcia, które zrzucają jedną z dwóch jednostek motorowych, zamrażając transporter w stanie nieczynnym. Ten mechanizm „allosterycznego zablokowania” reprezentuje nowy sposób unieruchamiania bakteryjnej maszyny i pomaga wyjaśnić, dlaczego SMT-738 może koncentrować się na groźnych patogenach, oszczędzając dużą część mikrobiomu. Szczegółowa mapa kieszeni wiążącej oraz kluczowa reszta selektywności w LolE oferują teraz racjonalny plan do projektowania kolejnej generacji antybiotyków, które wykorzystają tę samą słabość z jeszcze większą siłą i precyzją.
Cytowanie: Li, H., Zhu, X., Zhang, D. et al. Molecular mechanism of action of small molecule SMT-738 on bacterial lipoprotein transporter LolCDE. Nat Commun 17, 2540 (2026). https://doi.org/10.1038/s41467-026-69411-2
Słowa kluczowe: oporność na antybiotyki, bakterie Gram-ujemne, transport lipoprotein, inhibitor LolCDE, struktura cryo-EM