Clear Sky Science · pl
Melczan pochodzący od makrofagów napędza fenotypowe przebudowanie fibroblastów skóry przez MCT1-zainicjowaną laktacylację lizyny 23 w histonie H3 w bliznach przerostowych
Dlaczego niektóre blizny stają się grube i wypukłe
Większość skaleczeń i oparzeń z czasem blednie i zmienia się w cienkie, płaskie blizny. Jednak niektóre rany goją się z powstaniem grubych, wypukłych pasm tkanki zwanych bliznami przerostowymi, które mogą swędzieć, boleć i ograniczać ruch. To badanie ujawnia nieoczekiwanego kierowcę tych uporczywych blizn: powszechny produkt uboczny metabolizmu, kwas mlekowy (laktat), wytwarzany przez komórki odpornościowe w sztywnej, gojącej się skórze, który przeprogramowuje pobliskie komórki naprawcze, skłaniając je do zachowań sprzyjających bliznowaceniu.
Od normalnej naprawy do problematycznej blizny
W prawidłowym gojeniu ran komórki skóry współpracują, aby zamknąć uszkodzenie i odbudować tkankę. Fibroblasty, główne komórki naprawcze w głębszej warstwie skóry, przechodzą przejściowo w silniejszą postać produkującą kolagen — białkowy ruszt skórny. Gdy rana się zamyka, te komórki ponownie się wyciszają. W bliznach przerostowych fibroblasty jednak pozostają uwięzione w tej nadaktywnej formie, odkładając zbyt dużo kolagenu w grubych, nieuporządkowanych pęczkach. Autorzy zaczęli od porównania zdrowej skóry z tkanką bliznową i stwierdzili wyraźne przesunięcie metaboliczne: środowisko blizny sprzyjało szybkiej, cukrożernej chemii generującej duże ilości laktatu oraz wysokim poziomom białka transportowego MCT1, które przenosi laktat do wnętrza komórek. 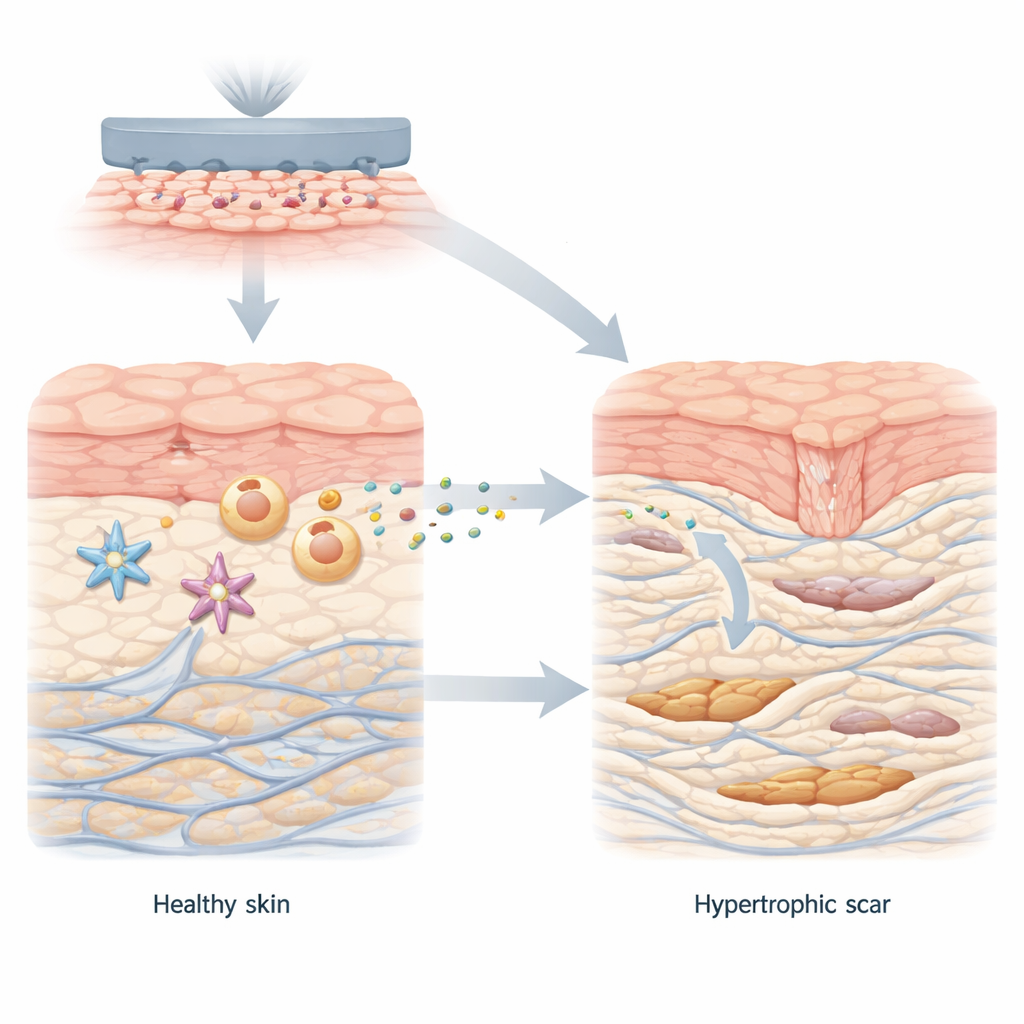
Komórki odpornościowe jako nieoczekiwane fabryki laktatu
Aby ustalić, skąd pochodzi cały ten laktat, zespół przebadał różne typy komórek z ludzkiej skóry i modeli mysich: makrofagi (komórki odpornościowe usuwające resztki i koordynujące gojenie), komórki naczyń krwionośnych oraz fibroblasty. Hodowali te komórki na miękkich lub sztywnych podłożach naśladujących normalną i zbliznowaciałą skórę. Na sztywnych powierzchniach tylko makrofagi przestawiały się na wysoce glikolityczny, „żerny” tryb metabolizmu i wypompowywały duże ilości laktatu, zarówno w hodowlach, jak i w rzeczywistej tkance bliznowej. Gdy makrofagi usunięto z gojących się ran myszy, poziomy laktatu w tkance spadły, a tworzenie blizn zmniejszyło się. Wyniki te wskazują na makrofagi, szczególnie te reagujące na sztywne środowisko, jako główne fabryki laktatu kształtujące mikrośrodowisko blizny.
Laktat jako sygnał przestawiający fibroblasty
Następnie badacze zapytali, jak nadmiar laktatu wpływa na fibroblasty. Gdy fibroblasty zanurzono w płynie bogatym w laktat pochodzący od makrofagów hodowanych na sztywnym podłożu, mnożyły się szybciej, poruszały się intensywniej i produkowały więcej kolagenu — wszystkie cechy agresywnego stanu miofibroblastycznego. Blokowanie transportera MCT1 na fibroblastach lub ograniczenie produkcji laktatu w makrofagach ostro zmniejszało te zmiany. Wewnątrz fibroblastów napływający laktat robił więcej niż tylko zasilał produkcję energii: wywoływał specyficzny znak chemiczny na białkach histonowych, które organizują DNA w jądrze komórkowym. Ten znacznik, zwany laktacylacją H3K23, był znacznie podwyższony w fibroblastach tworzących blizny w porównaniu z normalnymi i działał jak przełącznik włączający dwa kluczowe geny, HEY2 i COL11A1, które wspólnie wzmacniają sygnały sprzyjające bliznowaceniu.
Samo-wzmacniająca się pętla bliznowacenia
Białka uruchamiane przez ten znacznik histonowy tworzą silną pętlę sprzężenia zwrotnego. HEY2 zwiększa aktywność szlaku obejmującego YAP1 i SMAD2, który jest znany z popychania fibroblastów w stronę bardziej kurczliwej, produkującej kolagen postaci. COL11A1, białko strukturalne związane z kolagenem, wchodzi w fizyczną interakcję z transporterem MCT1 na fibroblastach, pomagając stabilizować go i uczynić pobór laktatu bardziej wydajnym. Innymi słowy, laktat wchodzący do komórki zmienia regulację genów w sposób, który dodatkowo zwiększa napływ laktatu i produkcję kolagenu, utrwalając fibroblasty w pro-bliznowej tożsamości. 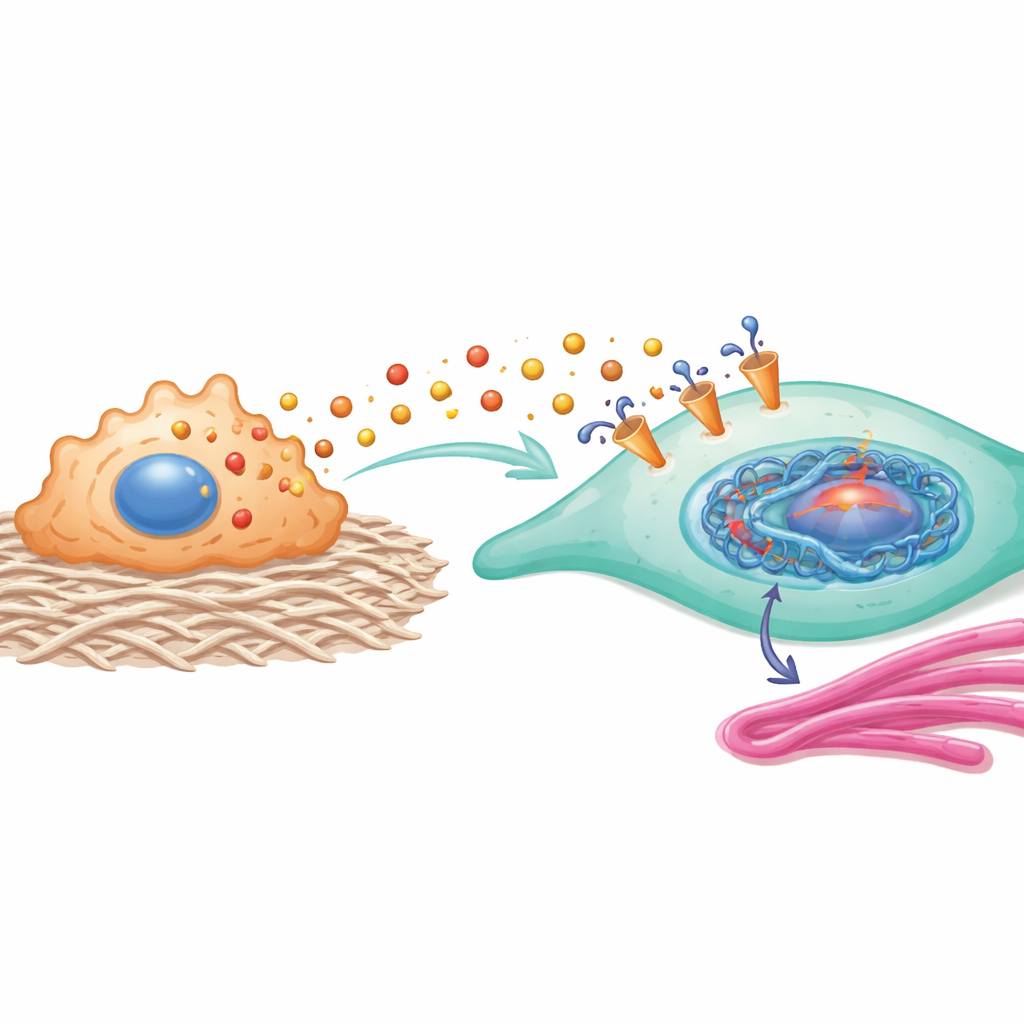
Przygaszenie pętli by poprawić gojenie
Aby sprawdzić, czy przerwanie tej pętli może poprawić gojenie, zespół użył myszy, u których MCT1 można było selektywnie usunąć z fibroblastów, oraz leku blokującego MCT1. W obu przypadkach rany zamykały się szybciej, nowo powstała skóra wyglądała bardziej uporządkowanie, a włókna kolagenowe były cieńsze i lepiej wyrównane, z mniejszą liczbą cech blizn przerostowych. Konkretny znacznik histonowy i jego geny podporządkowane również spadły. Odtłumienie makrofagów — głównego źródła laktatu — lub chemiczne obniżenie poziomu laktatu dało podobne efekty przeciwbliznowe. Te eksperymenty pokazują, że łańcuch: sztywna rana–makrofag–laktat–fibroblast nie jest jedynie korelacją, lecz kluczowym czynnikiem napędzającym patologiczne bliznowacenie.
Co to oznacza dla przyszłych terapii blizn
Praca ta przekształca postrzeganie laktatu z prostego odpadu metabolicznego w potężny przekaźnik łączący mechanikę, metabolizm i kontrolę genów w gojeniu ran. Pokazując, jak laktat pochodzący od makrofagów, transportowany przez MCT1, zmienia histony i uruchamia samo-wzmacniający program bliznowacenia w fibroblastach, badanie wskazuje kilka obiecujących celów terapeutycznych. Leki modulujące produkcję laktatu, blokujące MCT1 lub ingerujące w konkretną modyfikację histonową mogłyby kiedyś pomóc ranom goić się szybciej i pozostawiać płaskie, mniej widoczne blizny.
Cytowanie: Yuan, Y., Xiao, Y., Zou, J. et al. Lactate derived from macrophages drives skin dermal fibroblasts phenotypic remodeling via MCT1-primed histone H3 lysine 23 lactylation in hypertrophic scar. Nat Commun 17, 2694 (2026). https://doi.org/10.1038/s41467-026-69388-y
Słowa kluczowe: blizna przerostowa, sygnalizacja laktatem, komunikacja makrofag–fibroblast, laktacylacja histonów, terapia gojenia ran