Clear Sky Science · pl
Mioferlina jest składnikiem pęcherzyków transportujących vRNP w późnym etapie dla osłonkowych wirusów RNA
Dlaczego to ma znaczenie dla codziennego zdrowia
Sezonowa grypa i inne infekcje dróg oddechowych mogą wydawać się rutynowe, ale łącznie zabijają co roku miliony ludzi na całym świecie. Wiele z tych wirusów, w tym wirus grypy A i wirus syncytialny układu oddechowego (RSV), unika już szczepionek i leków przeciwwirusowych dzięki szybkim mutacjom. To badanie skupia się zamiast tego na czymś, czego wirusy nie mogą łatwo zmienić: na maszynerii komórkowej człowieka, którą przejmują, by wydostać się z zainfekowanych komórek. Odkrycie wspólnej słabości tej maszynerii wskazuje kierunek dla przyszłych leków, które mogłyby jednocześnie osłabić szerokie spektrum wirusów oddechowych.
Komórkowa droga dostawcza wykorzystywana przez wirusy
Komórki dróg oddechowych nieustannie ponownie wykorzystują fragmenty swojej błony zewnętrznej w procesie zwanym recyklingiem. Małe pęcherzyki błonowe przenoszą ładunek z wnętrza komórki z powrotem na powierzchnię, kierowane przez rodzinę białek znanych łącznie jako Rab11. Wirus grypy A, RSV i spokrewniony wirus Sendai wykorzystują tę trasę w późnym etapie zakażenia. Ładują swój materiał genetyczny, zapakowany jako kompleksy rybonukleoproteinowe, na pęcherzyki zawierające Rab11, które transportują je na stronę komórki zwróconą ku drogom oddechowym, gdzie powstają nowe cząstki wirusa i są uwalniane. Dotąd Rab11 był jedynym czynnikiem gospodarza wyraźnie wspólnym dla tych pęcherzyków transportowych, co pozostawiało duży brak w zrozumieniu, jak one powstają i funkcjonują.
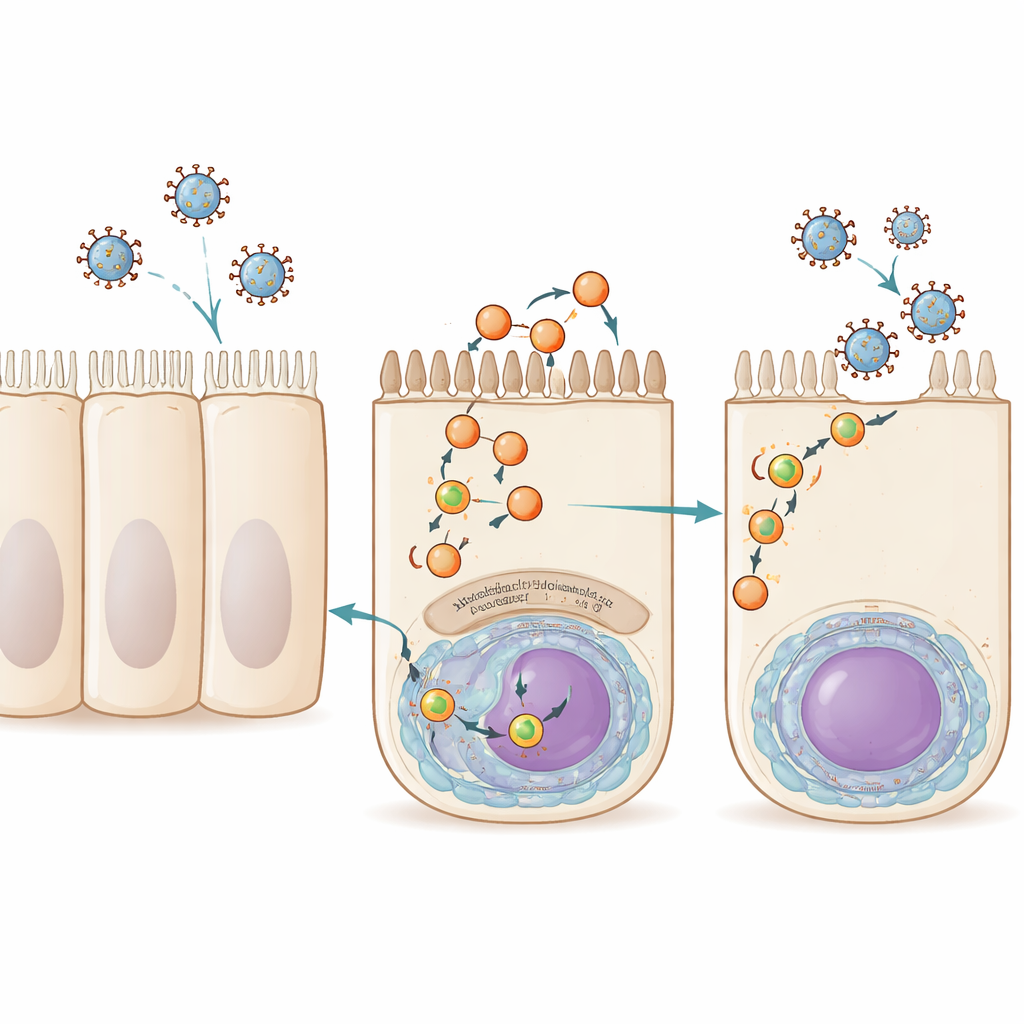
Odkrycie nowego uczestnika: mioferlina
Badacze zaczęli od pytania, które białka ludzkie fizycznie kojarzą się z maszynerią pakującą genom grypy w różnych momentach infekcji. Zmodyfikowali wirusa grypy A tak, żeby jego polimeraza niosła znak molekularny, a następnie użyli spektrometrii mas, by skatalogować ludzkie białka związane z tym kompleksem na wczesnych i późnych etapach zakażenia. Spośród setek kandydatów jeden wyróżniał się w późnych punktach czasowych: mioferlina, duże białko związane z błonami wcześniej powiązane z rozwojem mięśni, endocytozą i naprawą błon. Gdy zespół zmniejszył poziomy mioferliny w komórkach pochodzących z płuc przy użyciu małych interferujących RNA lub zablokował ją małocząsteczkowym inhibitorem, komórki dalej normalnie wytwarzały RNA wirusowe i białka wirusowe, ale uwalniały znacznie mniej zakaźnych cząstek grypy. Wskazywało to, że mioferlina nie jest potrzebna do replikacji genomu wirusowego, lecz jest kluczowa w późniejszych etapach, gdy nowe wirusy są składane i opuszczają komórkę.
Mioferlina podróżuje z ładunkiem wirusowym
Obrazowanie o wysokiej rozdzielczości ujawniło, gdzie mioferlina znajduje się podczas infekcji. W komórkach niezainfekowanych mioferlina w dużej mierze pokrywa się z pęcherzykami recyklingowymi pozytywnymi w kierunku Rab11, zarówno w pobliżu jądra, jak i na obrzeżach komórki, a utrata któregokolwiek z tych białek zaburza normalne rozmieszczenie drugiego. Podczas infekcji grypowej sieć Rab11 ulega dramatycznej przebudowie w powiększone, nieregularne pęcherzyki, które niosą wirusowe rybonukleoproteiny. Mioferlina utrzymuje się w tych przebudowanych pęcherzykach i wykazuje silną kolokalizację z materiałem genetycznym wirusa i Rab11. Kiedy zespół użył leku, który powoduje skupianie się kompleksów genomu wirusowego i ich nośników pęcherzykowych, mioferlina została wciągnięta do tych samych agregatów, co potwierdza, że jest wbudowanym składnikiem tych struktur transportowych w późnym etapie, a nie znajduje się tam przypadkowo.
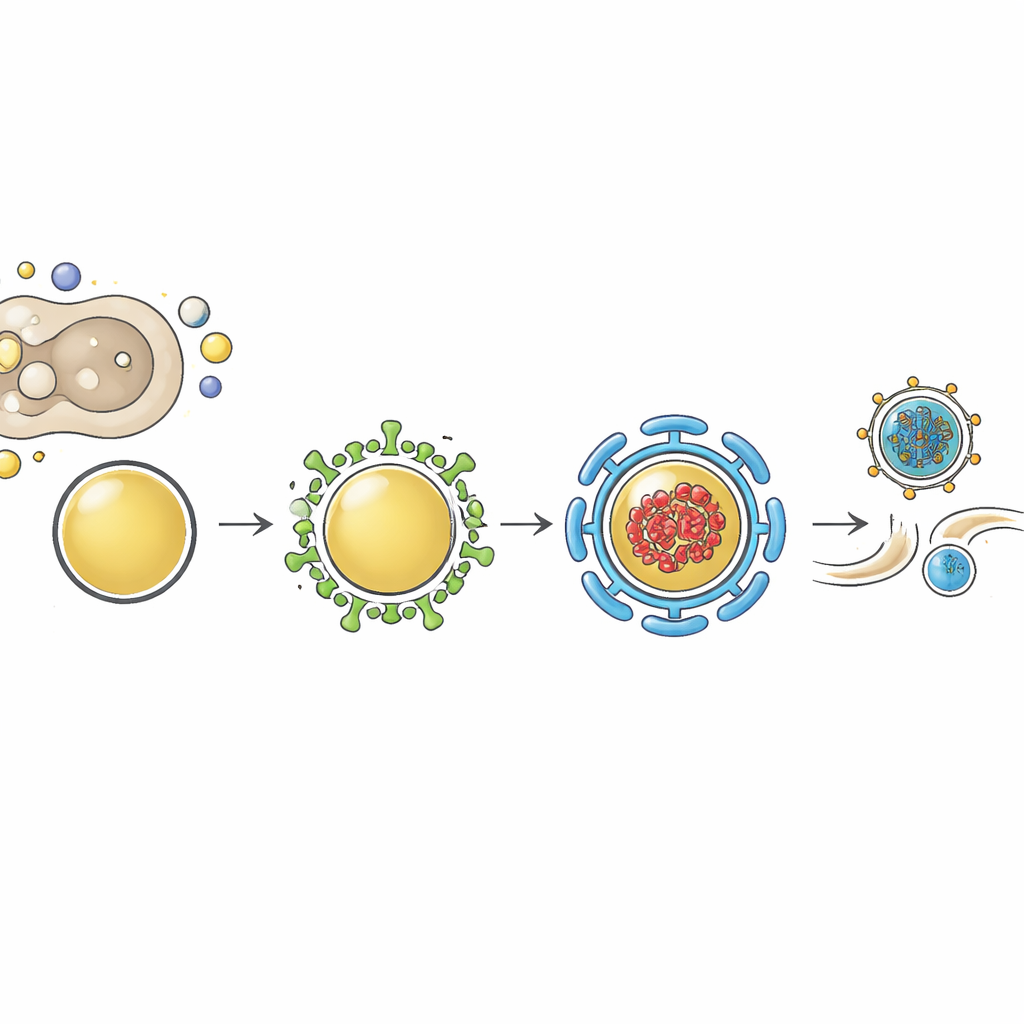
Wspólny węzeł dla wielu wirusów oddechowych
Następnie badanie sprawdziło, czy to uzależnienie od mioferliny jest specyficzne dla grypy, czy bardziej powszechne. Zmniejszenie ilości mioferliny w komórkach płucnych zainfekowanych RSV lub wirusem Sendai ponownie spowodowało wyraźny spadek uwalnianych zakaźnych wirusów, bez obniżenia poziomów RNA wirusowego. Mikroskopia pojedynczych cząsteczek wykazała, że genomy obu wirusów skupiają się razem z mioferliną i Rab11 w cytoplazmatycznych punktach, które prawdopodobnie reprezentują węzły transportowe, a nie fabryki replikacyjne. Ten wzór wspiera zjednoczoną wizję: różne osłonkowe wirusy RNA dróg oddechowych, pomimo różnorodnych sposobów życia, zbieżają się na tym samym systemie pęcherzyków Rab11–mioferlina, gdy nadchodzi czas przemieszczania ukończonych genomów w kierunku powierzchni komórki w celu zapakowania i uwolnienia.
Jak mioferlina kształtuje pęcherzyki niosące wirusy
Mioferlina zbudowana jest z wielu domen „C2”, które mogą wiązać błony i białka partnerskie. Wcześniejsze badania wykazały, że jedna z tych domen wchodzi w interakcję z rodziną białek remodelujących błony zwanych EHD. W tym badaniu fluorescencyjnie znakowane EHD1 i EHD2 znaleziono w tych samych przebudowanych pęcherzykach, które niosły genomy grypy i Rab11, zwłaszcza gdy pęcherzyki te były eksperymentalnie sklejane. Zmniejszenie poziomów EHD2, podobnie jak redukcja mioferliny, obniżało plony grypy bez wpływu na replikację genomu. Co więcej, usunięcie mioferliny spowodowało spadek poziomów białka EHD2, co sugeruje, że mioferlina pomaga stabilizować lub prawidłowo pozycjonować EHD2 na błonach. Autorzy proponują, że mioferlina osiada na pęcherzykach dodatnich w kierunku Rab11 i rekrutuje białka EHD, aby formować ich błony, kończąc tworzenie wyspecjalizowanych „nieregularnie pokrytych pęcherzyków”, zoptymalizowanych do transportu ładunku wirusowego na miejsca pączkowania.
Co to oznacza dla przyszłych strategii przeciw wirusom
Podsumowując, wyniki stawiają mioferlinę jako centralnego organizatora drogi recyklingowej gospodarza, na którą wiele osłonkowych wirusów oddechowych polega w krytycznym, późnym etapie. Ponieważ ukierunkowanie wyłącznie na białka wirusowe często prowadzi do szybkiego pojawienia się oporności, czynniki gospodarza wykorzystywane przez wiele wirusów są atrakcyjnymi celami leków. Zakłócenie funkcji mioferliny lub jej współpracy z Rab11 i białkami EHD mogłoby w zasadzie spowolnić lub zablokować rozprzestrzenianie się różnych patogenów, od grypy i RSV po inne wirusy zależne od Rab11, jak niektóre koronawirusy. Wciąż pozostaje wiele pracy, by przełożyć ten koncept na bezpieczne terapie, ale badanie dostarcza szczegółowej mapy wspólnej drogi ucieczki wirusów — i wskazuje mioferlinę jako obiecujący punkt zwężający na tej ścieżce.
Cytowanie: Bonazza, S., Turkington, H.L., Sukumar, S. et al. Myoferlin is a component of late-stage vRNP trafficking vesicles for enveloped RNA viruses. Nat Commun 17, 2507 (2026). https://doi.org/10.1038/s41467-026-69386-0
Słowa kluczowe: grypa, wirusy układu oddechowego, transport pęcherzykowy, czynniki gospodarza, mioferlina