Clear Sky Science · pl
Inżynierowane nanoweskule egzosomalne do dostarczania przeciwciał w leczeniu zapalnych chorób jelit
Nowa nadzieja na uporczywą chorobę jelit
Zapalenie jelit (IBD) może zamienić codzienne życie w ciągłą walkę z bólem, biegunką i zmęczeniem, a ponadto zwiększa długoterminowe ryzyko raka jelita grubego. Wiele obecnych leków łagodzi zaostrzenia, ale nie naprawia wadliwych reakcji układu odpornościowego leżących u podstaw choroby, dlatego objawy często wracają. W tym badaniu przedstawiono pomysłowo zaprojektowaną „inteligentną” nanocząstkę, która krąży we krwi, odnajduje zapalone fragmenty jelita i dostarcza dwuetapowe leczenie mające zarówno stłumić szkodliwy stan zapalny, jak i odbudować trwałą równowagę immunologiczną.
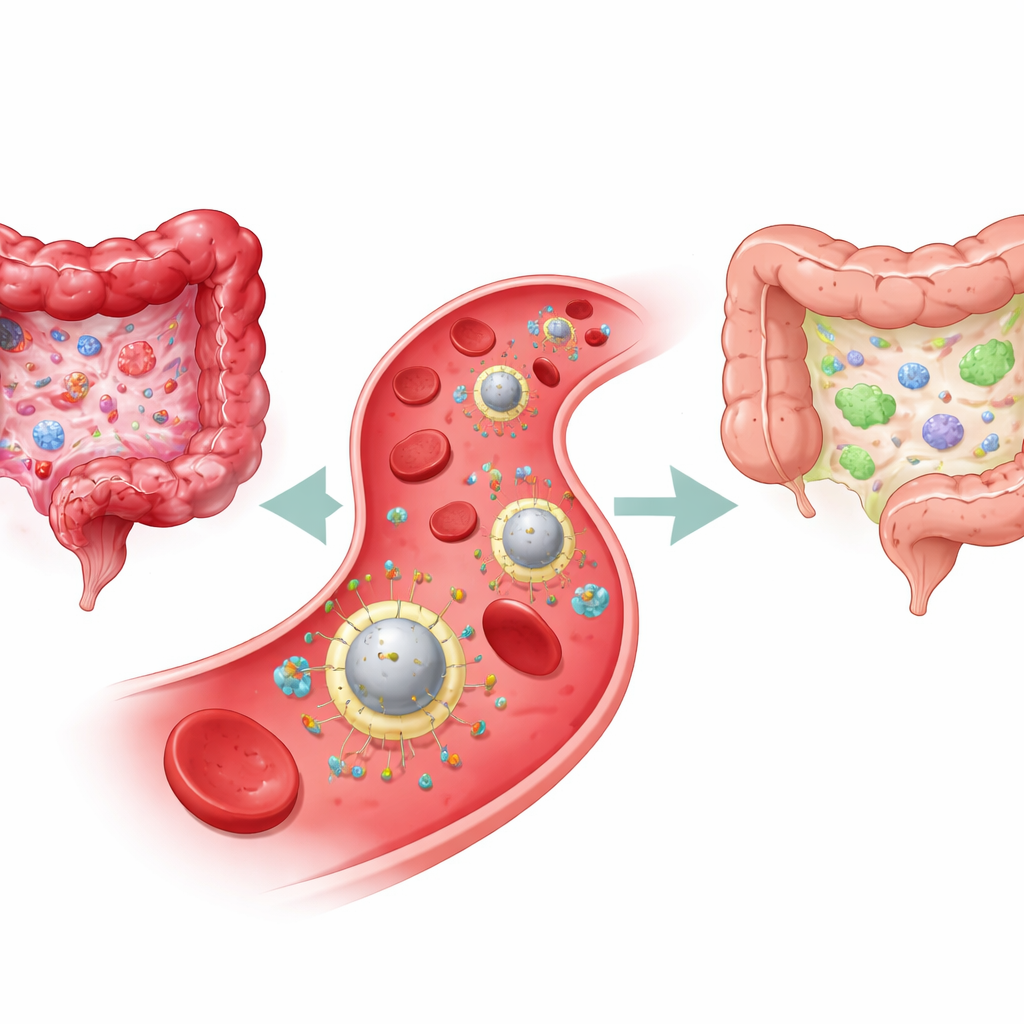
Dlaczego obecne terapie zawodzą
IBD, obejmujące chorobę Leśniowskiego–Crohna i wrzodziejące zapalenie jelita grubego, wynika z przewlekłego konfliktu w układzie odpornościowym jelit. Z jednej strony znajdują się agresywne komórki odpornościowe i cząsteczki zapalne, które uszkadzają błonę śluzową jelita; z drugiej — komórki regulacyjne, które normalnie powstrzymują tę reakcję. Standardowe terapie — takie jak sterydy, immunosupresanty i leki biologiczne — głównie próbują stłumić stan zapalny w całym organizmie. Mogą łagodzić objawy, ale często niewiele robią, by przywrócić podstawową równowagę immunologiczną, a szerokie tłumienie odporności może zwiększać ryzyko zakażeń. Nawet nowsze leki przeciwciałowe blokujące kluczowy sygnał zapalny zwany interleukiną‑23 (IL‑23) pomagają tylko części pacjentów i nadal krążą szeroko, a nie tylko tam, gdzie są potrzebne.
Budowanie leku, który trafia na miejsce i zmienia kształt
Naukowcy postanowili zaprojektować terapię, która zachowywałaby się bardziej jak żywa komórka niż prosty lek. Zaczęli od maleńkich pęcherzyków naturalnie uwalnianych przez limfocyty T regulatorowe — komórki odpornościowe sprzyjające tolerancji i utrzymujące porządek. Te pęcherzyki, zwane egzosomami, niosą białka i materiał genetyczny, które mogą nakłaniać inne komórki odpornościowe do stanu uspokojenia. Zespolili te egzosomy z fragmentami błony płytek krwi, wykorzystując zdolność płytek do przyczepiania się do uszkodzonych naczyń krwionośnych w zapalnej tkance. Na powierzchni tej hybrydowej otoczki przytwierdzili przeciwciała blokujące IL‑23 za pomocą molekularnej „nitki”, którą mogą przecinać enzymy (metaloproteinazy macierzowe) obecne głównie w zapalonym jelicie. Produkt, nazwany PrEXO‑a23, to nanoweskula, która krąży we krwi, przyczepia się do uszkodzonych naczyń jelitowych, a następnie uwalnia ładunek przeciwciał tylko tam, gdzie choroba jest aktywna.
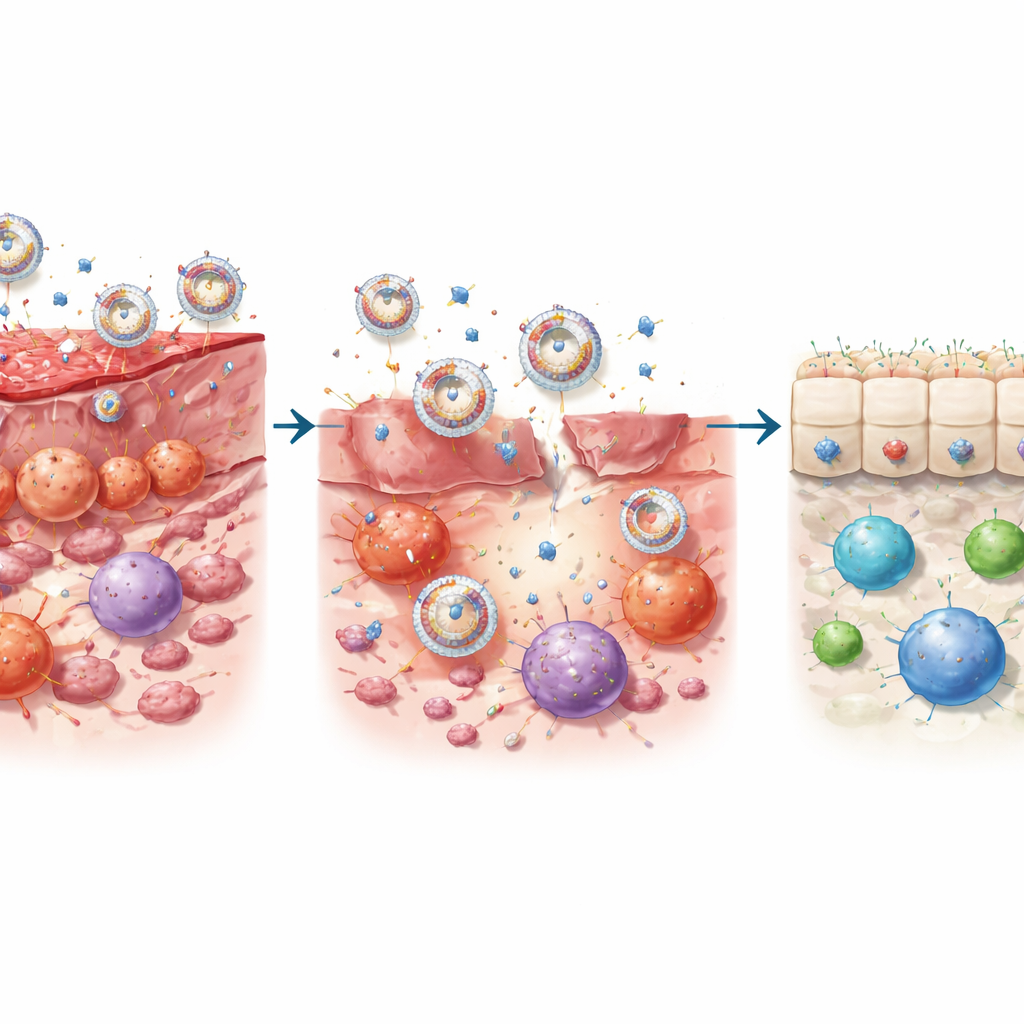
Przeprogramowywanie immunologicznego mikrośrodowiska jelita
W badaniach komórkowych PrEXO‑a23 przewyższał zarówno samo przeciwciało, jak i same egzosomy. Silnie zmniejszał powstawanie zapalnych komórek Th17 (pomocniczych typu 17) i uwalnianie szkodliwych cytokin niszczących wyściółkę jelita, jednocześnie chroniąc ludzkie komórki nabłonka jelitowego przed śmiercią. Równocześnie skłaniał komórki dendrytyczne — strażników instruujących limfocyty T — z aktywnego, prozapalnego stanu w kierunku stanu „tolerancyjnego”, który sprzyja rozwojowi komórek regulatorowych T. W modelach mysich z zapaleniem jelita nanoweskule trafiały efektywnie do zapalonych tkanek okrężnicy, były pobierane przez różne typy komórek odpornościowych i uwalniały przeciwciała w reakcji na lokalną aktywność enzymatyczną. To dwuetapowe działanie — blokowanie zapalenia napędzanego przez IL‑23 i wzmacnianie sygnałów sprzyjających tolerancji — zbliżyło markery zapalne do wartości prawidłowych i przywróciło zdrowszy skład typów limfocytów T.
Naprawa tkanek i zapobieganie długotrwałym uszkodzeniom
Myszy z chemicznie wywołanym zapaleniem wiązadła, które otrzymały PrEXO‑a23 traciły mniej masy ciała, miały dłuższe, zdrowsze okrężnice i wykazywały mniejsze powiększenie śledziony, co jest oznaką ogólnoustrojowego zapalenia. Badanie mikroskopowe ujawniło zachowaną architekturę jelita i szczelniejsze połączenia między komórkami nabłonka, co wskazuje na naprawioną barierę. Leczenie pomogło także przywrócić równowagę mikrobioty jelitowej, zwiększając rodziny związane ze zdrowiem jelit i ograniczając te powiązane z chorobą. W cięższym modelu, który naśladuje przejście od przewlekłego zapalenia do raka okrężnicy, PrEXO‑a23 nie tylko złagodził trwające zapalenie, ale całkowicie zapobiegł rozwojowi guzów i ograniczył pogrubienie oraz bliznowacenie ściany jelita charakterystyczne dla włóknienia. Analizy molekularne wskazały na przywrócenie ochronnego sygnalizowania p53 — centralnego strażnika przed rakiem — co okazało się istotne dla efektu przeciwnowotworowego.
W kierunku sprytniejszej, trwalszej opieki nad IBD
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że praca ta wykracza poza proste „przyciszanie” zapalenia. Łącząc ukierunkowane dostarczanie, uwalnianie przeciwciał na miejscu oraz uspokajający ładunek egzosomalny w jednym malutkim opakowaniu, PrEXO‑a23 zarówno łagodzi aktywną chorobę, jak i pomaga przeszkoleniu układu odpornościowego w kierunku trwałej tolerancji. U myszy doprowadziło to nie tylko do ulgi w objawach, ale także do ochrony przed bliznowaceniem i rakiem jelita grubego — dwoma z najbardziej przerażających powikłań długotrwałego IBD. Choć nadal potrzebne są liczne badania, zanim taka terapia mogłaby trafić do pacjentów, badanie pokazuje, jak inspirowana biologicznie nanomedycyna może pewnego dnia zaoferować bardziej precyzyjną i trwałą kontrolę złożonych zaburzeń immunologicznych, takich jak IBD.
Cytowanie: Cao, J., Luo, R., Miao, R. et al. Engineered exosome nanovesicles for delivery of antibodies to treat inflammatory bowel disease. Nat Commun 17, 2737 (2026). https://doi.org/10.1038/s41467-026-69382-4
Słowa kluczowe: zapalenie jelit, nanomedycyna, tolerancja immunologiczna, egzosomy, zapobieganie rakowi okrężnicy